
 (1)如图为金刚烧的空间结构(碳架)
(1)如图为金刚烧的空间结构(碳架)
分析 (1)金刚烷的一氯代物取决于氢原子的种类;金刚烷的结构可看做是由四个等同的六元环组成的空间构型,利用等效氢,先固定一个氯原子,再移动另一个氯原子,据此判断二氯代物的异构体数目;
(2)采用换元法,将氯原子代替氢原子,氢原子代替氯原子,从一氯化物有二种,就可得到七氯代物也有二种同分异构体;二噁英的二氯代物的同分异构体可以采用固定1个氯原子移动另1个Cl的方法进行确定.
解答 解:金刚烷分子中有两种氢原子,一种是次甲基氢( ),一种亚甲基氢(-CH2-),所以其一氯代物有2种;金刚烷分子中有两种氢原子,一种是次甲基氢(
),一种亚甲基氢(-CH2-),所以其一氯代物有2种;金刚烷分子中有两种氢原子,一种是次甲基氢( ),一种亚甲基氢(-CH2-),如图:
),一种亚甲基氢(-CH2-),如图: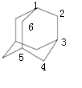 ,所以该物质的二氯代物有:在1、2号碳,1、3号碳,1、4号碳上3种,均在2号碳上一种,在2、4号碳,和2、5号碳上各有1种,总共6种;
,所以该物质的二氯代物有:在1、2号碳,1、3号碳,1、4号碳上3种,均在2号碳上一种,在2、4号碳,和2、5号碳上各有1种,总共6种;
故答案为:2;6;
(2)二噁英有8个H原子,其中1个H原子被1个氯原子取代形成二噁英的一氯代物,七氯代物可以看作二噁英中的8个氯原子,其中1个氯原子被1个氢原子代替形成,两者是等效的.二氯代物有二种同分异构体,可得到七氯代物也有二种同分异构体,则该物质的七溴代物共有二种;
二噁英的中H原子有2种: ,一氯化物有二种,所以该物质的二氯代物一个氯在1号碳上时,另一个氯原子共有7种位置:在1、2号碳,1、3号碳,在1、4号碳,1、5号碳,在1、6号碳,1、7号碳,在1、8号碳,此时二氯代物有7种;一个氯在2号碳上时,另一个氯原子共有3种位置:在2、3号碳,2、6号碳,在2、7号碳,此时二氯代物有3种;总共10种;
,一氯化物有二种,所以该物质的二氯代物一个氯在1号碳上时,另一个氯原子共有7种位置:在1、2号碳,1、3号碳,在1、4号碳,1、5号碳,在1、6号碳,1、7号碳,在1、8号碳,此时二氯代物有7种;一个氯在2号碳上时,另一个氯原子共有3种位置:在2、3号碳,2、6号碳,在2、7号碳,此时二氯代物有3种;总共10种;
故答案为:二;10.
点评 本题考查同分异构体的书写,难度中等,关键对空间结构有清晰的理解和取代产物的判断.


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 试剂 | 操作方法 |
| A | 除去CH4中的C2H4 | 高锰酸钾 | 洗气 |
| B | 除去工业酒精中的水 | CaO | 蒸馏 |
| C | 除去苯中的溴 | NaOH | 分液 |
| D | 从肥皂、甘油的混合液中分离出肥皂 | NaCl | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 据以上线索和下列反应事实,
据以上线索和下列反应事实, ,则该C7H14的结构简式是(CH3)2CHC(CH3)=CHCH3,名称是3,4-二甲基-2-戊烯
,则该C7H14的结构简式是(CH3)2CHC(CH3)=CHCH3,名称是3,4-二甲基-2-戊烯查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com