
用混有碳酸氢铵、硫酸钠的氯化钠固体配制纯净的氯化钠溶液,实验方案如下:
② ③
过量 过量
BaCl2 Na2CO3 过量
溶液 溶液 盐酸
↓ ↓ ↓

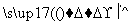

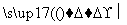
 ―→
―→
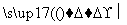

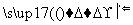

请回答下列问题
(1)操作①可除去________(填化学式)。
(2)操作②是否可改为硝酸钡溶液________(填“是”或“否”),原因__________________________________________________。
(3)操作③的目的是____________________________ ____________________________________________。
(4)操作④的目的是________________________________ ________________________________________。
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
(1)常温下将0.2mol/L HCl溶液与0.2mol/L MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
①混合溶液中由水电离出的c(H+) 0.2mol/LHCl溶液中由水电离出的c(H+);
(填“>”、“<”、或“=”)
②求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Cl-)-c(M+)= mol/L。
(2)常温下若将0.2mol/L MOH溶液与0.1mol/L HCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度 MCl的水解程度。
(填“>”、“<”、或“=”)
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH 。(填“>7”、“<7”、或“无法确定”)
(4)用0.1032mol/L HCl溶液滴定未知浓度的NaOH溶液,重复三次的实验数据如下所示
| 实验序号 | 0.1032mol/L HCl溶液体积/mL | 待测NaOH溶液体积/mL |
| 1 | 27.83 | 25.00 |
| 2 | 25.53 | 25.00 |
| 3 | 27.85 | 25.00 |
①待测NaOH溶液的物质的量浓度为 mol/L。(保留四位有效数字)
②下列情况可能引起测定结果偏高的是 。
A.酸式滴定管未用标准盐酸溶液润洗
B.锥形瓶未用待测液润洗
C.滴定前滴定管尖嘴中有一气泡,滴定后气泡消失了
D.滴定前,滴定管中的溶液液面最低点在“0”点以下
(5)滴定的方法有酸碱中和滴定、沉淀滴定、络合滴定等。沉淀滴定所用的指示剂本身就是一种沉淀剂。已知一些银盐的颜色和Ksp(20℃)如下,测定水体中氯化物的含量,常用标准硝酸银溶液进行滴定。
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 1.8×10-10 | 5.0×10-13 | 8.3×10-17 | 2.0×10-48 | 1.8×10-10 |
滴定时,你认为该滴定适宜选用的指示剂是下列中的 。
A. KBr B. KI C. K2S D. K2CrO4
查看答案和解析>>
科目:高中化学 来源: 题型:
已知金属钠和水反应的化学方程式为:2Na+2H2O===2NaOH+H2↑。将9.2 g金属钠投入到足量的重水D2O中,则产生的气体中含有( )
A.0.2 mol中子 B.0.4 mol电子
C.0.2 mol质子 D.0.4 mol分子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列根据实验现象所得出的结论不正确的是( )
A.无色溶液使紫色石蕊试液变蓝;结论:溶液一定呈碱性
B.无色溶液焰色反应呈紫色(透过蓝色钴玻璃观察),结论:溶液中一定含有K+
C.在无色溶液中加入Na2CO3溶液产生白色沉淀;结论:溶液中一定含有Ca2+
D.在无色盐溶液中加入NaOH溶液,加热产生的气体使湿润的红色石蕊试纸变蓝;结论:溶液一定含有NH
查看答案和解析>>
科目:高中化学 来源: 题型:
海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是( )
A.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2
B.海水蒸发制海盐的过程中只发生了化学变化
C.海水中含有镁元素,只需经过物理变化就可以得到镁单质
D.目前工业上直接由海水提取I2
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行氯、溴、碘的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是( )
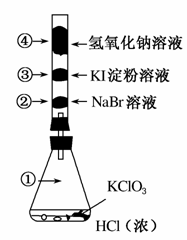
① ② ③ ④
A.黄绿色 橙色 蓝色 白色
B.无色 橙色 紫色 白色
C.黄绿色 橙色 蓝色 无色
D.黄绿色 无色 紫色 白色
查看答案和解析>>
科目:高中化学 来源: 题型:
不能用于判断金属失电子能力强弱的是
A.同主族金属元素原子半径大小
B.1 mol金属单质在反应中失去电子的多少
C.水溶液中金属间发生的置换反应
D.金属元素最高价氧化物对应水化物的碱性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
能在水溶液中大量共存的一组离子是( )
A.H+、I-、NO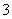 、SiO
、SiO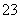
B.Ag+、Fe3+、Cl-、SO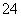
C.K+、SO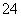 、Cu2+、NO
、Cu2+、NO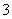
D.NH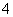 、OH-、Cl-、HCO
、OH-、Cl-、HCO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com