
”¾ĢāÄæ”æäå»ÆŃĒĶŹĒŅ»ÖÖ°×É«·ŪÄ©£¬²»ČÜÓŚĄäĖ®£¬ŌŚČČĖ®ÖŠ»ņ¼ū¹ā¶¼»į·Ö½ā£¬ŌŚæÕĘųÖŠ»įĀżĀżŃõ»Æ³ÉĀĢÉ«·ŪÄ©”£ÖʱøCuBrµÄŹµŃé²½ÖčČēĻĀ£ŗ
²½Öč1.ŌŚČēĶ¼ĖłŹ¾µÄČż¾±ÉÕĘæÖŠ¼ÓČė45gCuSO4”¤5H2O”¢19gNaBr”¢150mLÖ󷊹żµÄÕōĮóĖ®£¬60”ꏱ²»¶Ļ½Į°č£¬ŅŌŹŹµ±Į÷ĖŁĶØČėSO2 2Š”Ź±”£
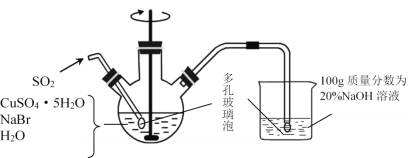
²½Öč2.ČÜŅŗĄäČ“ŗóĒćČ„ÉĻ²ćĒåŅŗ£¬ŌŚ±Ü¹āµÄĢõ¼žĻĀ¹żĀĖ”£
²½Öč3.ŅĄ“ĪÓĆČÜÓŠÉŁĮæSO2µÄĖ®”¢ČÜÓŠÉŁĮæSO2µÄŅŅ“¼”¢“æŅŅĆŃĻ“µÓ”£
²½Öč4.ŌŚĖ«²ćøÉŌļĘ÷£Ø·Ö±š×°ÓŠÅØĮņĖįŗĶĒāŃõ»ÆÄĘ£©ÖŠøÉŌļ3”«4h£¬ŌŁ¾ĒāĘųĮ÷øÉŌļ£¬×īŗó½ųŠŠÕęæÕøÉŌļ”£
£Ø1£©ŹµŃéĖłÓĆÕōĮóĖ®Šč¾Öó·Š£¬Öó·ŠÄæµÄŹĒ³żČ„ĘäÖŠĖ®ÖŠµÄ______________£ØŠ“»ÆѧŹ½£©”£
£Ø2£©²½Öč1ÖŠ£ŗ¢ŁČż¾±ÉÕĘæÖŠ·“Ӧɜ³ÉCuBrµÄĄė×Ó·½³ĢŹ½ĪŖ_______________£»
¢ŚæŲÖĘ·“Ó¦ŌŚ60”ę½ųŠŠ£¬ŹµŃéÖŠæɲÉČ”µÄ“ėŹ©ŹĒ_____________£»
¢ŪĖµĆ÷·“Ó¦ŅŃĶź³ÉµÄĻÖĻóŹĒ__________________”£
£Ø3£©²½Öč2¹żĀĖŠčŅŖ±Ü¹āµÄŌŅņŹĒ_______________”£
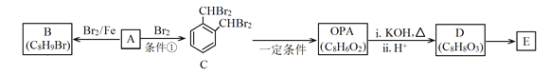
£Ø4£©²½Öč3ÖŠĻ“µÓ¼ĮŠč”°ČÜÓŠSO2”±µÄŌŅņŹĒ_____________________×īŗóČܼĮøÄÓĆŅŅĆѵÄÄæµÄŹĒ________________________________”£
£Ø5£©ÓūĄūÓĆÉĻŹö×°ÖĆÉÕ±ÖŠµÄĪüŹÕŅŗ£Ø¾¼ģ²āÖ÷ŅŖŗ¬Na2SO3”¢NaHSO3µČ£©ÖĘČ”½Ļ“æ¾»µÄNa2SO3”¤7H2O¾§Ģ唣Ēė²¹³äŹµŃé²½Öč£ØŠėÓƵ½SO2£ØÖü“ęŌŚøÖĘæÖŠ£©”¢20%NaOHČÜŅŗ”¢ŅŅ“¼£©
¢Ł_______________________________________________”£
¢Ś__________________________________________________”£
¢Ū¼ÓČėÉŁĮæĪ¬ÉśĖŲCČÜŅŗ£Øæ¹Ńõ¼Į£©£¬Õō·¢ÅØĖõ£¬ĄäČ“½į¾§”£
¢Ü__________________________________________________”£
¢Ż·ÅÕęæÕøÉŌļĻäÖŠøÉŌļ”£
”¾“š°ø”æO2 2Cu2+ + 2Br£+ SO2 + 2H2O ”ś 2CuBr”ż+SO42£+4H+ 60”ęĖ®Ō”¼ÓČČ ČÜŅŗĄ¶É«ĶźČ«ĶŹČ„ ·ĄÖ¹CuBr¼ū¹ā·Ö½ā ·ĄÖ¹CuBr±»Ńõ»Æ ³żČ„±ķĆęŅŅ“¼£¬²¢Ź¹¾§ĢåæģĖŁøÉŌļ ŌŚÉÕ±ÖŠ¼ĢŠųĶØČėSO2ÖĮ±„ŗĶ Č»ŗóĻņÉÕ±ÖŠ¼ÓČė100g 20%µÄNaOHČÜŅŗ ¹żĀĖ£¬ÓĆŅŅ“¼Ļ“µÓ2”«3“Ī
”¾½āĪö”æ
(1)äå»ÆŃĒĶÄܱ»ŃõĘųĀżĀżŃõ»Æ£¬ŅŖÅųżŃõĘųµÄøÉČÅ£»
(2)¢ŁČż¾±ÉÕĘæÖŠĶĄė×Ó±»¶žŃõ»ÆĮņ»¹Ō³ÉŃĒĶĄė×Ó£¬ÓėäåĄė×Ó·“Ӧɜ³ÉCuBr³Įµķ£»
¢ŚæŲÖĘ·“Ó¦ŌŚ60”ę½ųŠŠ£¬æÉŅŌÓĆ60”ęµÄĖ®Ō”¼ÓČČ£»
¢Ū45gCuSO45H2OĪŖ0.18mol£¬19gNaBrĪŖ0.184mol£¬ĖłŅŌNaBrÉŌ¹żĮ棬ĖłŅŌµ±ČÜŅŗÖŠµÄĶĄė×ÓĻūŗÄĶźŹ±·“Ó¦¼“Ķź³É£»
(3)äå»ÆŃĒĶ¼ū¹ā»į·Ö½ā£»
(4)äå»ÆŃĒĶŌŚæÕĘųÖŠ»įĀżĀż±»Ńõ»Æ£¬Ļ“µÓ¼ĮŠč”°ČÜÓŠSO2”±æÉŅŌ·ĄÖ¹CuBr±»Ńõ»Æ£¬ČܼĮøÄÓĆŅŅĆŃæÉŅŌ³żČ„±ķĆęŅŅ“¼£¬²¢Ź¹¾§ĢåæģĖŁøÉŌļ£»
(5)ÉÕ±ÖŠµÄĪüŹÕŅŗÖ÷ŅŖŗ¬Na2SO3”¢NaHSO3µČ£¬ÖĘČ”½Ļ“æ¾»µÄNa2SO37H2O¾§Ģ壬æÉŅŌŌŚÉÕ±ÖŠ¼ĢŠųĶØČėSO2ÖĮ±„ŗĶ£¬½«Na2SO3Éś³ÉNaHSO3£¬øł¾ŻÄĘŌŖĖŲŹŲŗćæÉÖŖ£¬“ĖŹ±ČÜŅŗÖŠNaHSO3µÄĪļÖŹµÄĮæĪŖ0.5mol£¬Č»ŗóĻņÉÕ±ÖŠ¼ÓČė100g 20%µÄNaOHČÜŅŗ£¬Ź¹NaHSO3Ē”ŗĆĶźČ«·“Ӧɜ³ÉNa2SO3£¬¼ÓČėÉŁĮæĪ¬ÉśĖŲCČÜŅŗ(æ¹Ńõ¼Į)£¬Õō·¢ÅØĖõ£¬ĄäČ“½į¾§£¬¹żĀĖ£¬ÓĆŅŅ“¼Ļ“µÓ2”«3“Ī£¬³żČ„±ķĆęæÉČÜŠŌŌÓÖŹ£¬·ÅÕęæÕøÉŌļĻäÖŠøÉŌļ£¬¾Ż“Ė“šĢā”£
(1)äå»ÆŃĒĶÄܱ»ŃõĘųĀżĀżŃõ»Æ£¬ÓƶžŃõ»ÆĮņ»¹ŌĶĄė×ÓÉś³Éäå»ÆŃĒĶŅŖÅųżŃõĘųµÄøÉČÅ£¬æÉŅŌĶعżÖ󷊵ķ½·Ø³żČ„ĘäÖŠĖ®ÖŠµÄO2£¬¹Ź“š°øĪŖ£ŗO2£»
(2)¢ŁČż¾±ÉÕĘæÖŠĶĄė×Ó±»¶žŃõ»ÆĮņ»¹Ō³ÉŃĒĶĄė×Ó£¬ÓėäåĄė×Ó·“Ӧɜ³ÉCuBr³Įµķ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ2Cu2++2Br+SO2+2H2O=2CuBr”ż+SO42+4H+£¬¹Ź“š°øĪŖ£ŗ2Cu2++2Br+SO2+2H2O=2CuBr”ż+SO42+4H+£»
¢ŚæŲÖĘ·“Ó¦ŌŚ60”ę½ųŠŠ£¬æÉŅŌÓĆ60”ęµÄĖ®Ō”¼ÓČČ£»¹Ź“š°øĪŖ£ŗ 60”ęĖ®Ō”¼ÓČČ£»
¢Ū45gCuSO45H2OĪŖ0.18mol£¬19gNaBrĪŖ0.184mol£¬ĖłŅŌNaBrÉŌ¹żĮ棬ĖłŅŌµ±ČÜŅŗÖŠµÄĶĄė×ÓĻūŗÄĶźŹ±·“Ó¦¼“Ķź³É£¬ĖłŅŌĖµĆ÷·“Ó¦ŅŃĶź³ÉµÄĻÖĻóŹĒČÜŅŗĄ¶É«ĶźČ«ĶŹČ„£¬¹Ź“š°øĪŖ£ŗČÜŅŗĄ¶É«ĶźČ«ĶŹČ„£»
(3)äå»ÆŃĒĶ¼ū¹ā»į·Ö½ā£¬ĖłŅŌ²½Öč2¹żĀĖŠčŅŖ±Ü¹ā£¬·ĄÖ¹CuBr¼ū¹ā·Ö½ā£¬¹Ź“š°øĪŖ£ŗ·ĄÖ¹CuBr¼ū¹ā·Ö½ā£»
(4)ŌŚæÕĘųÖŠ»įĀżĀż±»Ńõ»Æ£¬ĖłŅŌĻ“µÓ¼ĮŠč”°ČÜÓŠSO2”±æÉŅŌ·ĄÖ¹CuBr±»Ńõ»Æ£¬×īŗóČܼĮøÄÓĆŅŅĆŃæÉŅŌ³żČ„±ķĆęŅŅ“¼£¬²¢Ź¹¾§ĢåæģĖŁøÉŌļ£¬¹Ź“š°øĪŖ£ŗ·ĄÖ¹CuBr±»Ńõ»Æ£»³żČ„±ķĆęŅŅ“¼£¬²¢Ź¹¾§ĢåæģĖŁøÉŌļ£»
(5)ÉÕ±ÖŠµÄĪüŹÕŅŗÖ÷ŅŖŗ¬Na2SO3”¢NaHSO3µČ£¬ÖĘČ”½Ļ“æ¾»µÄNa2SO37H2O¾§Ģ壬æÉŅŌŌŚÉÕ±ÖŠ¼ĢŠųĶØČėSO2ÖĮ±„ŗĶ£¬½«Na2SO3Éś³ÉNaHSO3£¬øł¾ŻÄĘŌŖĖŲŹŲŗćæÉÖŖ£¬“ĖŹ±ČÜŅŗÖŠNaHSO3µÄĪļÖŹµÄĮæĪŖ0.5mol£¬Č»ŗóĻņÉÕ±ÖŠ¼ÓČė100g20%µÄNaOHČÜŅŗ£¬Ź¹NaHSO3Ē”ŗĆĶźČ«·“Ӧɜ³ÉNa2SO3£¬¼ÓČėÉŁĮæĪ¬ÉśĖŲCČÜŅŗ(æ¹Ńõ¼Į)£¬Õō·¢ÅØĖõ£¬ĄäČ“½į¾§£¬¹żĀĖ£¬ÓĆŅŅ“¼Ļ“µÓ23“Ī£¬³żČ„±ķĆęæÉČÜŠŌŌÓÖŹ£¬·ÅÕęæÕøÉŌļĻäÖŠøÉŌļ£¬¹Ź“š°øĪŖ£ŗŌŚÉÕ±ÖŠ¼ĢŠųĶØČėSO2ÖĮ±„ŗĶ£»Č»ŗóĻņÉÕ±ÖŠ¼ÓČė100g20%µÄNaOHČÜŅŗ£»¹żĀĖ£¬ÓĆŅŅ“¼Ļ“µÓ23“Ī”£


 ĶسĒѧµäĬŠ“ÄÜŹÖĻµĮŠ“š°ø
ĶسĒѧµäĬŠ“ÄÜŹÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪĀ¶ČĻĀ£¬Ģå»żŅ»¶ØµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠČēĻĀæÉÄę·“Ó¦£ŗX(g)+Y(g) ![]() Z(g)+W(s)£»”÷H >0
Z(g)+W(s)£»”÷H >0
ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A. ¼õÉŁÉŁĮæW£¬Äę·“Ó¦ĖŁĀŹ¼õŠ”
B. µ±ČŻĘ÷ÖŠĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæ²»±äŹ±£¬·“Ó¦“ļµ½Ę½ŗā
C. ½µµĶĪĀ¶Č£¬Ę½ŗāÕżĻņŅʶÆ
D. Ę½ŗāŗó¼ÓČėZ£¬ÉĻŹö·“Ó¦µÄ”÷H¼õŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°¢·üŁ¤µĀĀŽ³£ŹżæÉÓĆNA±ķŹ¾£¬ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£Ø £©
A.1mol H2OĖłŗ¬µÄŌ×ÓŹżĪŖNAøö
B.16g O2-ŗ¬ÓŠµÄµē×ÓŹżĪŖ10NAøö
C.³£ĪĀ³£Ń¹ĻĀ£¬11.2L Cl2Ėłŗ¬·Ö×ÓŹżĪŖ0.5NAøö
D.1L 1mol/L NaClOČÜŅŗÖŠŗ¬ClO-øöŹżĪŖNAøö
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ2010Äź£¬ÖŠ¹śŹ×“ĪÓ¦ÓĆĮłČ²»ł±½ŌŚĶʬ±ķĆęŗĻ³ÉĮĖŹÆÄ«Č²±”Ĥ(ĘäŗĻ³ÉŹ¾ŅāĶ¼ČēÓŅĶ¼ĖłŹ¾)£¬ĘäĢŲŹāµÄµē×Ó½į¹¹½«ÓŠĶū¹ć·ŗÓ¦ÓĆÓŚµē×Ó²ÄĮĻĮģÓņ”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ( )
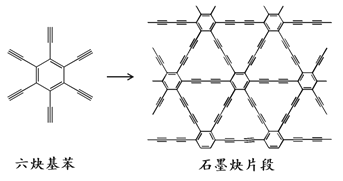
A.ĮłČ²»ł±½µÄ»ÆѧŹ½ĪŖC18H6
B.ĮłČ²»ł±½ŗĶŹÆÄ«Č²¶¼¾ßÓŠĘ½ĆęŠĶ½į¹¹
C.ĮłČ²»ł±½ŗĶŹÆÄ«Č²¶¼æÉ·¢Éś¼Ó³É·“Ó¦
D.ĮłČ²»ł±½ŗĻ³ÉŹÆÄ«Č²ŹōÓŚ¼Ó¾Ū·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪĀ¶ČĻĀ£¬ŌŚŅ»øö2 LµÄĆܱÕČŻĘ÷ÖŠ¼ÓČė4 mol AŗĶ2 mol B½ųŠŠČēĻĀ·“Ó¦£ŗ3A(g)£«2B(g)![]() 4C(s)£«D(g)£¬·“Ó¦2 minŗó“ļµ½Ę½ŗā£¬²āµĆÉś³É1.6 mol C£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
4C(s)£«D(g)£¬·“Ó¦2 minŗó“ļµ½Ę½ŗā£¬²āµĆÉś³É1.6 mol C£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. Ē°2 min£¬DµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.2 mol”¤L£1”¤min£1 B. “ĖŹ±£¬BµÄĘ½ŗā×Ŗ»ÆĀŹŹĒ40%
C. ÉżøßøĆĢåĻµµÄĪĀ¶Č£¬»ÆŃ§Ę½ŗā³£Źż²»±ä D. Ōö¼ÓC£¬ÄęĻņĖŁĀŹŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»īŠŌŃõ»ÆŠæŹĒŅ»ÖÖ¶ą¹¦ÄÜŠŌµÄŠĀŠĶĪŽ»ś²ÄĮĻ£®Ä³Š”×éŅŌ“ÖŃõ»ÆŠæ£Øŗ¬Ģś”¢ĶµÄŃõ»ÆĪļ£©ĪŖŌĮĻÄ£Äā¹¤ŅµÉś²ś»īŠŌŃõ»ÆŠæ£¬²½ÖčČēĻĀ£ŗ
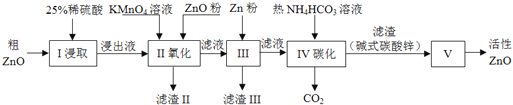
ŅŃÖŖø÷Ļą¹ŲĒāŃõ»ÆĪļ³ĮµķpH·¶Ī§ČēĻĀ±ķĖłŹ¾£ŗ
Zn£ØOH£©2 | Fe£ØOH£©2 | Fe£ØOH£©3 | Cu£ØOH£©2 | |
æŖŹ¼³ĮµķpH | 5.4 | 7.0 | 2.3 | 4.7 |
ĶźČ«³ĮµķpH | 8.0 | 9.0 | 4.1 | 6.7 |
Ķź³ÉĻĀĮŠĢīæÕ
£Ø1£©²½ÖčIÖŠĖłŠč25%Ļ”ĮņĖįæÉÓĆ98%ÅØĮņĖį£ØĆܶČĪŖ1.84g/mL£©ÅäÖĘ£¬ĖłŠčµÄŅĒĘ÷³ż²£Į§°ō”¢ÉÕ±Ķā£¬»¹ŠčŅŖ_______£ØŃ”Ģī±ąŗÅ£©
A£®µē×ÓĢģĘ½ B£®ĮæĶ² C£®ČŻĮæĘæ D£®½ŗĶ·µĪ¹Ü
£Ø2£©²½ÖčIIÖŠĶعż¼ÓČėKMnO4Ńõ»Æ£¬²¢ÓĆZnOµ÷½ŚpH£¬æÉŅŌ³żČ„ŗ¬ĢśŌÓÖŹ£®¼ģŃé³ĮµķŹĒ·ńĶźČ«µÄŹµŃé²Ł×÷ŹĒ_________£®µ÷½ŚpHµÄŹŹŅĖ·¶Ī§ŹĒ_________£®
£Ø3£©²½ÖčIIIÖŠ¼ÓČėZn·ŪµÄ×÷ÓĆŹĒ£ŗ¢Ł________£»¢Ś½ųŅ»²½µ÷½ŚČÜŅŗpH£®
£Ø4£©²½ÖčIVÖŠŹ¹ÓĆČČNH4HCO3ČÜŅŗÄÜ“Ł½ųZn2+×Ŗ»ÆĪŖ³Įµķ£¬µ«ĪĀ¶Č²»ŅĖ¹żøߣ¬ĘäŌŅņæÉÄÜŹĒ________£®
£Ø5£©²½ÖčVŌŚ_______£ØĢīŅĒĘ÷Ćū³Ę£©ÖŠ½ųŠŠ£¬ŅŃÖŖ¼īŹ½Ģ¼ĖįŠæµÄ»ÆѧŹ½ĪŖZn5£ØOH£©6£ØCO3£©2£¬ĒėŠ“³ö·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ________£®ÅŠ¶ĻŅŃ·Ö½āĶźČ«µÄ²Ł×÷ŹĒ________£®
£Ø6£©ÓĆČēĻĀ·½·Ø²ā¶ØĖłµĆ»īŠŌŃõ»ÆŠæµÄ“æ¶Č£ŗ
¢ŁČ”1.000g»īŠŌŃõ»ÆŠæ£¬ÓĆ15.00mL 1.000mol/LĮņĖįČÜŅŗĶźČ«Čܽā
¢ŚÓĆÅضČĪŖ0.500mol/LµÄ±ź×¼ĒāŃõ»ÆÄĘČÜŅŗµĪ¶ØŹ£ÓąĮņĖį£¬µ½“ļÖÕµćŹ±ĻūŗÄĒāŃõ»ÆÄĘČÜŅŗ12.00mL£®
¼ŁÉčŌÓÖŹ²»²ĪÓė·“Ó¦£¬ŌņĖłµĆ»īŠŌŃõ»ÆŠæµÄ“æ¶ČĪŖ_______£®ČōŌŚµĪ¶ØŹ±£¬Źµ¼Ź²Ł×÷ÖŠ¹żĮæ°ėµĪ£Ø1mLČÜŅŗĪŖ25µĪ£©£¬Ōņ±¾“ĪµĪ¶ØµÄĻą¶ŌĪó²īĪŖ_____£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æH2SO3Ė®ČÜŅŗÖŠ“ęŌŚµēĄėĘ½ŗāH2SO3![]() H++ HSO3£ ŗĶHSO3£
H++ HSO3£ ŗĶHSO3£![]() H++ SO32££¬Čō¶ŌH2SO3ČÜŅŗ½ųŠŠČēĻĀ²Ł×÷£¬Ōņ½įĀŪÕżČ·µÄŹĒ£ŗ£Ø £©
H++ SO32££¬Čō¶ŌH2SO3ČÜŅŗ½ųŠŠČēĻĀ²Ł×÷£¬Ōņ½įĀŪÕżČ·µÄŹĒ£ŗ£Ø £©
A.ĶØČėĀČĘų£¬ČÜŅŗÖŠĒāĄė×ÓÅضČŌö“ó
B.ĶØČė¹żĮæH2S£¬·“Ó¦ŗóČÜŅŗpH¼õŠ”
C.¼ÓČėĒāŃõ»ÆÄĘČÜŅŗ£¬Ę½ŗāĻņÓŅŅĘ¶Æ£¬pH±äŠ”
D.¼ÓČėĀČ»Æ±µČÜŅŗ£¬Ę½ŗāĻņÓŅŅĘ¶Æ£¬»į²śÉśŃĒĮņĖį±µ³Įµķ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŽĖ®ĮņĖįĶŌŚ¼ÓČČÖĮ650”ꏱæŖŹ¼·Ö½āÉś³ÉŃõ»ÆĶŗĶĘųĢ壮ij»ī¶ÆŠ”×éĶعżŹµŃ飬Ģ½¾æ²»Ķ¬ĪĀ¶ČĻĀĘųĢå²śĪļµÄ×é³É£®ŹµŃé×°ÖĆČēĻĀ£ŗ
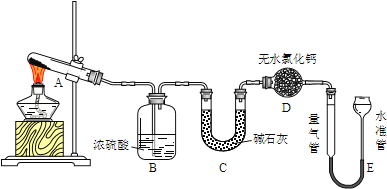
Ćæ“ĪŹµŃéŗó¾ł²ā¶ØB”¢CÖŹĮæµÄøıäŗĶEÖŠŹÕ¼Æµ½ĘųĢåµÄĢå»ż£®ŹµŃ鏿¾ŻČēĻĀ£ØEÖŠĘųĢåĢå»żŅŃÕŪĖćÖĮ±ź×¼×“æö£©£ŗ
ŹµŃé×鱚 | ĪĀ¶Č | ³ĘČ”CuSO4ÖŹĮæ/g | BŌöÖŲÖŹĮæ/g | CŌöÖŲÖŹĮæ/g | EÖŠŹÕ¼Æµ½ĘųĢå/mL |
¢Ł | T1 | 0.640 | 0.320 | 0 | 0 |
¢Ś | T2 | 0.640 | 0 | 0.256 | V2 |
¢Ū | T3 | 0.640 | 0.160 | Y3 | 22.4 |
¢Ü | T4 | 0.640 | X4 | 0.192 | 33.6 |
£Ø1£©ŹµŃé¹ż³ĢÖŠAÖŠµÄĻÖĻóŹĒ______£®DÖŠĪŽĖ®ĀČ»ÆøʵÄ×÷ÓĆŹĒ_______£®
£Ø2£©ŌŚ²āĮæEÖŠĘųĢåĢå»żŹ±£¬Ó¦×¢ŅāĻČ_______£¬Č»ŗóµ÷½ŚĖ®×¼¹ÜÓėĮæĘų¹ÜµÄŅŗĆęĻąĘ½£¬ČōĖ®×¼¹ÜÄŚŅŗĆęøßÓŚĮæĘų¹Ü£¬²āµĆĘųĢåĢå»ż______£ØĢī”°Ę«“ó”±”¢”°Ę«Š””±»ņ”°²»±ä”±£©£®
£Ø3£©ŹµŃé¢ŁÖŠBÖŠĪüŹÕµÄĘųĢåŹĒ_____£®ŹµŃé¢ŚÖŠEÖŠŹÕ¼Æµ½µÄĘųĢåŹĒ______£®
£Ø4£©ĶĘ²āŹµŃé¢ŚÖŠCuSO4·Ö½ā·“Ó¦·½³ĢŹ½ĪŖ£ŗ_______£®
£Ø5£©øł¾Ż±ķÖŠŹż¾Ż·ÖĪö£¬ŹµŃé¢ŪÖŠĄķĀŪÉĻCŌö¼ÓµÄÖŹĮæY3=_______g£®
£Ø6£©½įŗĻĘ½ŗāŅʶÆŌĄķ£¬±Č½ĻT3ŗĶT4ĪĀ¶ČµÄøßµĶ²¢ĖµĆ÷ĄķÓÉ________£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijÖÖÓŠ»ś»ÆŗĻĪļµÄ½į¹¹¼ņŹ½ČēĶ¼ĖłŹ¾”£ÓŠ¹ŲøĆĪļÖŹµÄĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £©
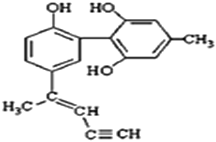
A.øĆĪļÖŹÓŠĖÄÖÖ¹ŁÄÜĶÅ£¬ĘäÖŠŅ»ÖÖĆū³ĘĪŖōĒ»ł
B.øĆ·Ö×ÓÖŠµÄĖłÓŠĢ¼Ō×Ó²»æÉÄܹ²Ę½Ćę
C.µĪČėĖįŠŌKMnO4ČÜŅŗÕńµ“£¬×ĻÉ«ĶŹČ„£¬ÄÜÖ¤Ć÷Ęä½į¹¹ÖŠ“ęŌŚĢ¼Ģ¼Ė«¼ü
D.1 moløĆĪļÖŹÓėH2·“Ó¦Ź±×ī¶ąĻūŗÄH2 9 mol
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com