
【题目】将一张滤纸剪成四等份,用铜片、锌片、发光二极管、导线在玻璃片上连接成如图所示的装置,在四张滤纸上滴入稀H2SO4直至全部润湿。下列叙述正确的是

A. 锌片为正极
B. 锌片上有气泡,铜片溶解
C. 电流都是从铜片经外电路流向锌片
D. 该装置至少有两种形式的能量转换
科目:高中化学 来源: 题型:
【题目】在好氧菌和厌氧菌作用下,废液中NH4+能转化为N2(g)和H2O(1),示意图如下:
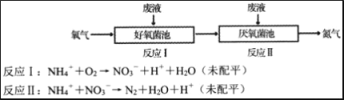
下列说法正确的是
A. 两池发生的反应中,氮元素只被氧化
B. 常温常压下,反应II中生成8.96 L N2时,转移电子数为1.5NA
C. 好氧菌池与厌氧菌池投入废液的体积之比为3:5时,NH4+能完全转化为N2
D. 反应Ⅱ中氧化剂与还原剂物质的量之比为5:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、X是中学化学中常见的物质。在一定条件下,它们之间的转化关系如下图所示(部分产物已略去)。
![]()
回答下列问题:
(1)若X是空气的主要成分之一,则A不可能是_____(填代号)。
a.Na b.C c.S d.Al
(2)若A常用作制冷剂,C为红棕色气体。写出由A生成B的化学方程式___________。
(3)若C可用于治疗胃酸过多,X是一种常见的温室气体。
①鉴别等浓度的B溶液和C溶液,可选用的试剂为______________(填化学式)。
②将A、B、C三种溶液混合,向45mL混合液中逐滴加入一定浓度的盐酸,生成气体的体积(标准状况)与加入盐酸的体积关系如下图所示。
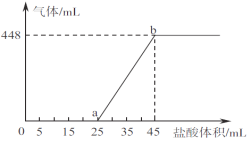
写出ab段所发生反应的离子方程式__________________________;b点对应溶液中溶质的物质的量浓度为___________(忽路溶液体积变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)若金属钠等活泼金属着火时,应该用_______________来灭火。将一小块钠投入盛有饱和石灰水的烧杯中,不可能观察到的现象是________。
a.有气体生成 b.钠熔化成小球并在液面上游动
c.烧杯底部有银白色的金属钙生成 d.溶液变浑浊
(2)Na2CO3和NaHCO3是两种常见的钠盐。下列关于Na2CO3和NaHCO3性质的说法中,正确的是______________。
a.常温下,Na2CO3在水中的溶解度比NaHCO3小
b.相同质量的Na2CO3和NaHCO3分别与足量盐酸反应,在相同条件下产生CO2前者多
c.可用Ca(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液
d. NaHCO3溶液中混有少量Na2CO3杂质可通入足量CO2除杂
(3)过氧化钠、过氧化镁都是重要的过氧化物。过氧化镁不溶于水,但易溶于稀酸,广泛用作胃药,治疗胃酸过多。试写出过氧化镁与胃酸反应的离子方程式:_____________。
(4)某无色稀溶液X中,可能含有Al3+、Cl-、Fe3+、Mg2+、NH4+中的某几种,向其中加入NaOH溶液时产生沉淀的物质的量(n)与加入NaOH溶液体积(V)的关系如下图所示。
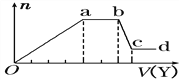
则X中一定含有的阳离子是_________,bc段反应的离子方程式为________。
(5)在1L某酸性溶液中离子浓度的分析结果如下表
离子 | Mg2+ | Al3+ | SO42 | Cl |
c/(mol/L) | 0.5×102 | 1.0×102 | 0.5×102 | 3.0×102 |
向该溶液中逐滴加入0.5 molL-1NaOH溶液至沉淀恰好不再溶解时,消耗NaOH体积为_____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以红土镍矿(主要含有Fe2O3、FeO、NiO、SiO2等)为原料,获取净水剂黄钠铁矾[NaFe3(SO4)2(OH)6]和纳米镍粉的部分工艺流程如下:

已知:Fe3+在pH约为3.7时可完全转化为Fe(OH)3,Fe2+在pH约为9时可完全转化为Fe(OH)2
(1)工业上常将“过滤Ⅰ”的滤液和滤渣洗涤液合并,其目的是____。
(2)“氧化”过程发生的离子方程式为___。
(3)“沉铁”过程中加入碳酸钠调节溶液的pH至2,碳酸钠过多会导致生成的沉淀由黄钠铁钒转变为_____(填化学式)。
(4)向“过滤Ⅱ”所得滤液(富含Ni2+)中加入N2H4·H2O,在不同浓度的氢氧化钠溶液中反应,含镍产物的XRD图谱如图所示(XRD图谱可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。欲制得高纯纳米镍粉最适宜的NaOH的浓度为____。写出该条件下制备纳米镍粉同时生成N2的离子方程式:_____。

(5)不同NaOH浓度下,产物Ni的含量不同,可能的原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是( )
A. 14C中含有 14个中子
B. 1H、2H、3H是同一种核素
C. 根据酸溶液中c(H+)大小,可将酸为强酸和弱酸
D. 根据分散质颗粒大小,可将分散系分为浊液、胶体和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒是一种熔点高、硬度大、无磁性的金属,广泛应用于钢铁、航空航天、能源等领域。工业上利用冶炼铝生成的固体废料——赤泥(主要成分为Fe2O3、Al2O3、V2O5及少量稀土金属氧化物)提取金属钒,其工艺流程图如下:

已知:钒有多种价态,其中+5价最稳定。钒在溶液中主要以![]() 和
和![]() 的形式存在,且存在平衡VO2++H2O
的形式存在,且存在平衡VO2++H2O![]() VO3-+2H+。下列说法正确的是
VO3-+2H+。下列说法正确的是
A. 工业生产中,碱浸步骤可选用较为廉价的氨水
B. 可以推测VO2Cl溶解度大于NH4VO3
C. 焙烧非磁性产品所得的固体产物加酸溶解时,应加入过量盐酸使其溶解完全
D. 将磁性产品加入稀硝酸溶解,取上层清液再加入KSCN溶液后未见红色,则磁性产品中一定不含铁元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类生产、生活、科研密切相关。下列有关说法正确的是( )
A.白酒中混有少量的塑化剂(易溶于酒精),可以通过过滤的方法除去
B.蚕丝的主要成分是蛋白质
C.向燃煤中加入生石灰的目的是减少温室气体的排放
D.油脂在人体内水解为氨基酸,才能被人体吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是( )

A. 反应CH4+H2O![]() 3H2+CO,每消耗1molCH4转移12mol 电子
3H2+CO,每消耗1molCH4转移12mol 电子
B. 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C. 电池工作时,CO32-向电极B移动
D. 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com