
| A. | 半导体行业中有一句话:“从沙滩到用户”计算机芯片的材料是二氧化硅 | |
| B. | “人造太阳”原理为:21H+31H→42He+10n,该过程不是化学变化 | |
| C. | “84”消毒液的有效成分是Ca(ClO)2 | |
| D. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 |
分析 A.硅晶体是半导体,用于计算机芯片的制备;
B.化学变化是分子、原子层次上研究的化学反应,此反应是核聚变反应;
C.氯气与氢氧化钠反应可得84消毒液;
D.碳纤维是由有机纤维经碳化及石墨化处理而得到的微晶石墨材料,不属于新型有机高分子材料.
解答 解:A.硅晶体是半导体,用于计算机芯片的制备,二氧化硅是光导纤维的成分,故A错误;
B.“人造太阳”原理为:21H+31H→42He+10n,该过程是核聚变,化学变化是分子、原子层次上研究的化学反应,所以此反应不是化学变化,故B正确;
C.氯气与氢氧化钠反应可得84消毒液,有效成分为NaClO,故C错误;
D.碳纤维是由有机纤维经碳化及石墨化处理而得到的微晶石墨材料,不属于新型有机高分子材料,故D错误;
故选B.
点评 本题考查了生活中常见物质的性质及用途,题目难度不大,熟悉物质的性质是解题关键.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.2mol | B. | 0.6mol | C. | 0.8mol | D. | 1.0mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
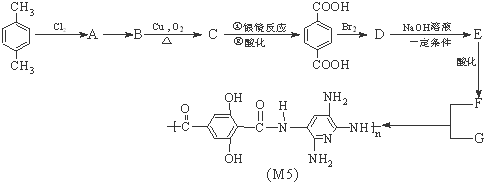
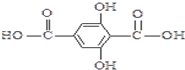 .
.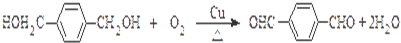 ,
,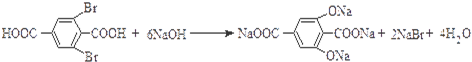 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
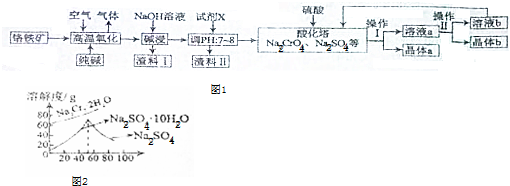
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
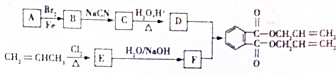
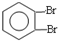 ,化合物E中所含的官能团名称为氯原子、碳碳双键.
,化合物E中所含的官能团名称为氯原子、碳碳双键.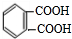 +2HOCH2CH=CH2$\stackrel{催化剂}{→}$
+2HOCH2CH=CH2$\stackrel{催化剂}{→}$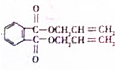 +2H2O,反应类型为酯化(取代)反应.
+2H2O,反应类型为酯化(取代)反应.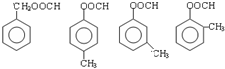 (其中一种).
(其中一种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 84% | B. | 8.4% | C. | 1.6% | D. | 16% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com