
���� ��1�����Ȼ�����ͭ��Ӧ�����Ȼ��������Ȼ�ͭ��ǿ������Һ����NaClO����Fe��OH��3���ɸ������ơ��Ȼ��ƺ���һ�ֳ�����������ݵ���غ㡢����ת���غ㡢ԭ���غ��֪��һ�ֳ��������ﺬ��HԪ�أ�ӦΪˮ���ݴ�д�����ӷ���ʽ��
��2��KClO3��H2SO4��������Na2SO3��Ӧ�Ƶ�ClO2����֪SO32-��������SO42-���ɵ��ӡ�����غ��֪�����ӷ�ӦΪ2ClO3-+SO32-+2H+�T2ClO2+SO42-+H2O�������ӷ�Ӧ��֪�÷�Ӧ�������뻹ԭ�����ʵ���֮�ȣ�
��3��������ʯ���鷴Ӧ�����Ȼ��ơ�������ƺ�ˮ��HClO����ǿ�����Ե��ᣬ�����DZ�̼�ỹ�����ᣬCa��ClO��2 ����ˮ�Ͷ�����̼�������ֽⷴӦ������CaCO3�� HClO�����ú������ȶ������ֽ�����HCl��O2���Ӷ�ʧȥƯ���ԣ�
��4��ʵ�����Ʊ�������������ķ����ǣ��ٽ����������ӵ�ˮ�⣬���ˮ�μӼ��α����Ȼ�����Һ�������������Һ�ʺ��ɫ����ֹͣ���ȣ�
��5���������������Ե��Ȼ���������Ӧ�����������Ӳμӣ�������������ˮ���ɣ�ClԪ�صĻ��ϼ۴�+5�۽��͵�-1�ۣ��õ�6�����ӣ���FeԪ�صĻ��ϼ۴�+2�����ߵ�+3�ۣ�ʧȥ1�����ӣ����ݵ�ʧ�����غ����ƽ����ʽ��
��� �⣺��1�����Ȼ�����ͭ��Ӧ�����Ȼ��������Ȼ�ͭ�����ӷ���ʽΪ��2Fe3++Cu=2Fe2++Cu2+��ǿ������Һ����NaClO����Fe��OH��3���ɸ������ơ��Ȼ��ƺ���һ�ֳ�����������ݵ���غ㡢����ת���غ㡢ԭ���غ��֪��һ�ֳ��������ﺬ��HԪ�أ�ӦΪˮ�����ӷ���ʽΪ2Fe��OH��3+3NaClO+4NaOH�T2Na2FeO4+3NaCl+5H2O���ʴ�Ϊ��2Fe3++Cu=2Fe2++Cu2+��2Fe��OH��3+3NaClO+4NaOH�T2Na2FeO4+3NaCl+5H2O��
��2��KClO3��H2SO4��������Na2SO3��Ӧ�Ƶ�ClO2����֪SO32-��������SO42-���ɵ��ӡ�����غ��֪�����ӷ�ӦΪ2ClO3-+SO32-+2H+�T2ClO2+SO42-+H2O��������ΪKClO3����ԭ��ΪNa2SO3�������ӷ�Ӧ��֪�÷�Ӧ�������뻹ԭ�����ʵ���֮��Ϊ2��1���ʴ�Ϊ��2��1��
��3��������ʯ���鷴Ӧ�����Ȼ��ơ�������ƺ�ˮ������ʽΪ2Cl2+2Ca��OH��2=CaCl2+2H2O+Ca��ClO��2��HClO����ǿ�����Ե��ᣬ�����DZ�̼�ỹ�����ᣬCa��ClO��2 ����ˮ�Ͷ�����̼�������ֽⷴӦ������CaCO3�� HClO����Ӧ���ӷ���ʽΪCa2++2ClO-+H2O+CO2=CaCO3 ��+2HClO��
��ˮ�еĴ��������ǿ�����ԣ����ú������ȶ������ֽ�����HCl��O2���Ӷ�ʧȥƯ���ԣ�����ʽΪ2HClO $\frac{\underline{\;����\;}}{\;}$2 HCl+O2����
�ʴ�Ϊ��2Cl2+2Ca��OH��2=CaCl2+2H2O+Ca��ClO��2��Ca2++2ClO-+H2O+CO2=CaCO3 ��+2HClO��2HClO $\frac{\underline{\;����\;}}{\;}$2 HCl+O2����
��4��ʵ�����Ʊ�������������ķ����ǣ������ձ��е�ˮ�����ڣ����ˮ�μӼ��α����Ȼ�����Һ�������������Һ�ʺ��ɫ����ֹͣ���ȣ�Ҫע��ʵ����̲����ò��������裬������Һ���ֻ��ǣ�����Ӧ��ϵ���ֺ��ɫ�����Ƶ������������壬Ӧ����ֹͣ���ȣ�����Ҳ���׳��ֻ��ǣ��������ɫ��������������������ˮ�еμӱ����Ȼ�����Һ����������У������˳�ʱ����ȣ���Ӧԭ��Ϊ��Fe3++3H2O$\frac{\underline{\;\;��\;\;}}{\;}$Fe��OH��3�����壩+3H+��
�ʴ�Ϊ�����ˮ�μӼ��α����Ȼ�����Һ�������������Һ�ʺ��ɫ����ֹͣ���ȣ�Fe3++3H2O$\frac{\underline{\;\;��\;\;}}{\;}$Fe��OH��3�����壩+3H+��
��5���������������Ե��Ȼ���������Ӧ�����������Ӳμӣ�������������ˮ���ɣ�ClԪ�صĻ��ϼ۴�+5�۽��͵�-1�ۣ��õ�6�����ӣ���FeԪ�صĻ��ϼ۴�+2�����ߵ�+3�ۣ�ʧȥ1�����ӣ����ݵ�ʧ�����غ㣬����������ӵ�ϵ��Ϊ1��Fe2+��ϵ��Ϊ6���������ӵ�ϵ��Ҳ��6�������ӵ�ϵ����1�����ݵ���غ㣬�������ӵ�ϵ����6��ˮ��ϵ����3����ƽ�����ӷ���ʽΪ��ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O��
�ʴ�Ϊ��1��6��6H+��6��1��3H2O��
���� ���⿼�����Ļ��������ʵ�Ӧ�á�������ԭ��Ӧ����ʽ����ƽ��Ư�۵�������ʵȣ���Ҫѧ���߱���ʵ�Ļ�������������Ѷȣ��Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ǡ��˴Ź����ǡ������Ƕ��������л�������ṹ�ķ��� | |
| B�� | ʯ�ͷ���ɻ����ϩ����ϩ�Ͷ���ϩ | |
| C�� | ͨ��ú��ֱ�ӻ���Һ�������Ի��ȼ���ͼ����ֻ���ԭ�� | |
| D�� | ά��������ϳ������أ�ͻ�����������л���Ľ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K+��Ca2+��HCO3-��Cl- | B�� | Cu2+��Na+��NO3-��Cl- | ||
| C�� | Na+��K+��Mg2+��SO42- | D�� | Mg2+��Fe3+��Cl-��OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X������һ������M�ģ�Y������һ������N�� | |
| B�� | ��Ϊ�÷�ӦΪ���ȷ�Ӧ������һ��Ҫ���ȷ�Ӧ���ܽ��� | |
| C�� | ���ѷ�Ӧ���еĻ�ѧ�����յ�����С���γ��������еĻ�ѧ���ų������� | |
| D�� | ��Ӧ��X��Y��������һ��С��������M��N�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �ڢۢ� | C�� | �ڢܢ� | D�� | �ܢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ���뷽��ʽΪ��NH3•H2O=NH4++OH- | |
| B�� | ��Һ���У�c��NH4+��+c��H+��=c��OH-�� | |
| C�� | ��Һ�У�c��NH3•H2O��=0.1mol/L | |
| D�� | ��������NaOH���壬��Һ�м�����ǿ��c��H+��•c��OH-���ij˻������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
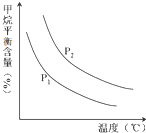 �ϳɰ������Ĵ����������˹��̵�����Ҫ;�������о�������ȷ������ָ�����ϳɰ���Ӧ��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ���£�
�ϳɰ������Ĵ����������˹��̵�����Ҫ;�������о�������ȷ������ָ�����ϳɰ���Ӧ��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ���£�| �� �ȣ��棩 | 360 | 440 | 520 |
| Kֵ | 0.036 | 0.010 | 0.0038 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2��D2��Ϊͬλ�� | B�� | 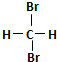 �� �� 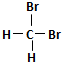 ��Ϊͬ���칹�� ��Ϊͬ���칹�� | ||
| C�� | ��������춡����ͬϵ�� | D�� | 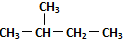 �� �� 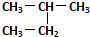 ��ͬһ������ ��ͬһ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com