
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
B. 标准状况下,11.2L苯中含有分子的数目为0.5NA
C. 2L0.5mol·L-1硫酸钾溶液中阴离子所带电荷数为NA
D. 标准状况下,22.4L氨水含有NA个NH3分子
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】“低碳生活,绿色出行”已经成为很多人的生活理念。CO2的捕捉和利用也成为了科学家们积极探索的热门领域。回答下列问题:
(1)用CO2催化加氢可制取乙烯,其能量关系如图1,写出该反应的热化学方程式____________。

(2)以硫酸作电解质溶液,利用太阳能电池将CO2转化为乙烯的工作原理如图2。则A为电池的___极,N极的电极反应式为_________________________。
(3)用CO2催化加氢制取二甲醚的反应为:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
在恒容密闭容器中,均充入2mol.CO2和6molH2,分别以Ir和Ce作催化剂,反应进行相同的时间后测得的CO2的转化率a(CO2)随反应温度的变化情况如图3。

①用Ir和Ce作催化剂时,反应的活化能更低的是_______。
②a、b、c、d和e五种状态,反应一定达到平衡状态的是__________,反应的△H ___0(填“>”、“=”或“<”)。
③从状态a到c,CO2转化率不断增大的原因是________________________________。
④状态e时,a(CO2)= 50%,若保持容器容积为10L,则此时的平衡常数K=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钠在制革工业、印刷工业、电镀工业等有重要用途,制备重铬酸钠(Na2Cr2O7)的方案1的流程图如图,铬铁矿的主要成分可表示为FeO·Cr2O3,还含有Al2O3、Fe2O3、SiO2等杂质。

除此外工厂还有相关改进工艺,制备重铬酸钠(Na2Cr2O7)的方案2如图,采用电化学原理如图所示的装置(电极为石墨),通过电解提高阳极区溶液的酸性,实现Na2CrO4转化为Na2Cr2O7。

(1)在方案2中请指明哪端是阴极? ___________(填“左”或“右”)。写出阳极的电极方程式:______________________。
(2)方案1中煅烧前应将铬铁矿充分粉碎,其目的是______________________。灼烧是中学化学中常用的操作方法,如在实验室中将铬铁矿和碳酸钠固体混合物灼烧,下列各实验仪器中不需要的是___________(填序号)。
a.陶瓷坩埚 b.铁坩埚 c.三脚架 d.泥三角
转窑中发生的主要反应除了下面的两个反应外,还有其他反应。
①Na2CO3+Al2O3![]() 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
②_____FeO·Cr2O3+______Na2CO3+______O2![]() ______Na2CrO4+______Fe2O3+______。
______Na2CrO4+______Fe2O3+______。
请配平反应②的化学方程式。
请写出其他主要反应方程式:_________________________________。
(3)固体Y的化学式为___________、___________。
(4)向母液中加入浓硫酸,把铬酸钠转化为重铬酸钠,经两次蒸发,主要是除去___________(填化学式),冷却至30-40℃得到产品晶体。洗涤该晶体的溶剂最好是___________(填序号)。
a.蒸馏水 b无水乙醇 c.75%乙醇溶液
(5)为了测定实验制得的产品中Na2Cr2O7,的含量,称取样品0.140g置于锥形瓶中,加50mL水;再加入2gKI(过量)及稍过量的稀硫酸溶液,摇匀,暗处放置10min;然后加入150mL蒸馏水并加入3mL0.5%淀粉溶液;用0.1000mol/L Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液30.00mL。(假定杂质不参加反应,已知:Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,I2+2S2O32-===2I-+S2O62-)
①终点实验现象是_______________________________________________________。
②该产品中Na2Cr2O7的纯度为______________________。(以质量分数表示)
③若滴定管在滴定前俯视读数,滴定结束后仰视读数,测得样品的纯度将___________(填“偏高”或“偏低”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数的值,下列说法中正确的是
①该氯原子的相对原子质量为12a/b
②该氯原子的摩尔质量是aNA g
③m g该氯原子的物质的量为m/(aNA)mol
④a g该氯原子所含的电子数为17 mol
A. ①③ B. ②④ C. ①② D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要分离下列四组混合物
①饱和食盐水与沙子 ②从KNO3和NaCl的混合溶液中获得KNO3
③水和汽油的混合物 ④CCl4液体与甲苯液体的混合物
(已知CCl4与甲苯互溶,沸点分别为76.75℃和110.6 ℃)
(1)分离①、②的操作分别为________、________。
(2)分离③时所使用仪器中有一种在其他组分分离时无需使用,这种仪器是________。
(3)上述四组分离时需使用酒精灯的有________和________(填序号)。
(4)为除去粗盐中的MgCl2、CaCl2、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
![]()
①第Ⅰ步操作的名称是____________。
②若第Ⅱ、Ⅳ步顺序颠倒,是否会对实验结果产生影响?________(填“有影响”或“无影响”)。
③第Ⅴ步操作所需玻璃仪器的名称是__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甲醚(CH3OCH3)是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,写出甲醚燃烧的热化学方程式_____;已知H2(g)和C(s)的燃烧热分别是285.8kJmol﹣1、393.5kJmol﹣1;计算反应4C(s)+6H2(g)+O2(g)═2CH3OCH3(g)的反应热△H=______;
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
若用标准状况下4.48L CH4还原NO2至N2,整个过程中转移的电子总数为________(阿伏加德罗常数用NA表示),放出的热量为________ kJ。
(3)在25 ℃、101 kPa时,1.00 g C6H6(l)燃烧生成CO2(g)和H2O(l),放出41.8 kJ的热量,则表示C6H6燃烧热的热化学方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
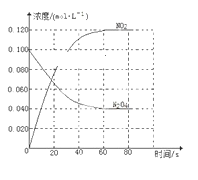
【题目】在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
回答下列问题:
(1)反应的ΔH________(填“大于”或“小于”)0;100 ℃时,体系中各物质浓度随时间变化如下图所示。在0~60 s时段,反应速率v(N2O4)为________mol·L-1·s-1。
(2)100 ℃时达平衡后,改变反应温度为T,c(N2O4)以0.002 0 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。
a.T________(填“大于”或“小于”)100 ℃,判断理由是________________________________。
b.温度T时反应的平衡常数K2=____________________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向________(填“正反应”或“逆反应”)方向移动,判断理由是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是常温下向20.0 mL的盐酸中,逐滴加入0.10 mol·L-1 NaOH溶液时,溶液的pH随 NaOH溶液的体积V(mL)变化的曲线,根据图像所得的下列结论中正确的是

A. 原盐酸的浓度为0.10 mol·L-1
B. x的值为2.0
C. 当pH=12时,V值为20.4
D. 原盐酸的浓度为1.0 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是( )
A.2mol水的摩尔质量和1mol水的摩尔质量
B.20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度
C.64g二氧化硫中氧原子数和标准状况下22.4L一氧化碳中氧原子数g
D.200mL1mol/L氯化钙溶液中c(Cl-)和200mL1mol/L氯化钾溶液中c(Cl-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com