
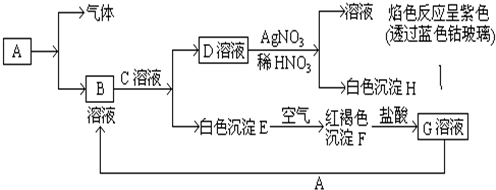
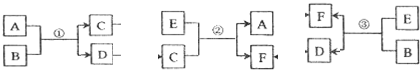
分析 D与硝酸银、硝酸反应得到的溶液,进行焰色反应显紫色,说明D溶液中含有K元素,D能和硝酸银溶液反应生成白色沉淀H为AgCl,所以D是KCl.白色沉淀E在空气中转化为红褐色沉淀F,则E是Fe(OH)2、F是Fe(OH)3,G为FeCl3.B和C反应生成氯化钾和氢氧化亚铁,所以B、C分别是KOH、FeCl2中的一种,G能和A反应生成B,所以A是Fe,B是FeCl2,C是KOH,Fe与盐酸反应得到FeCl2与氢气.
解答 解:D与硝酸银、硝酸反应得到的溶液,进行焰色反应显紫色,说明D溶液中含有K元素,D能和硝酸银溶液反应生成白色沉淀H为AgCl,所以D是KCl.白色沉淀E在空气中转化为红褐色沉淀F,则E是Fe(OH)2、F是Fe(OH)3,G为FeCl3.B和C反应生成氯化钾和氢氧化亚铁,所以B、C分别是KOH、FeCl2中的一种,G能和A反应生成B,所以A是Fe,B是FeCl2,C是KOH,Fe与盐酸反应得到FeCl2与氢气.
(1)由上述分析可知,B为FeCl2,D为KCl,E为Fe(OH)2,F为Fe(OH)3,
故答案为:FeCl2;KCl;Fe(OH)2;Fe(OH)3;
(2)用KSCN鉴别FeCl3溶液的离子方程式:Fe3++3SCN-═Fe(SCN)3,
向FeCl3溶液加入Fe的有关离子反应方程式:2Fe3++Fe═3Fe2+,
故答案为:Fe3++3SCN-═Fe(SCN)3;2Fe3++Fe═3Fe2+.
点评 本题考查无机物推断,试题综合性强,难易适中,焰色反应、反应现象等是推断突破口,侧重对学生基础知识的巩固与训练,熟练掌握元素化合物知识.


 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案科目:高中化学 来源: 题型:选择题
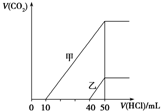
| A. | 原NaOH溶液的物质的量浓度为0.5 mol•L-1 | |
| B. | 当0<V(HCl)<10 mL时,甲溶液中发生反应的离子方程式为:OH-+H+═H2O | |
| C. | 乙溶液中含有的溶质是NaOH、NaHCO3 | |
| D. | 乙溶液中滴加盐酸后产生CO2体积的最大值为112 mL(标准状况) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝的导热性能较好,应大力提倡用铝炊具 | |
| B. | 铝制器具不宜盛放食品较长时间(如放入冰箱中过夜等) | |
| C. | 明矾可用于饮用水的杀菌消毒 | |
| D. | 小孩可以食用含铝较多的食物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
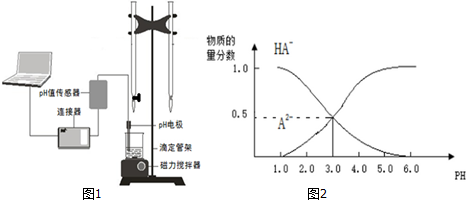
| A. | pH=4.0时,图中n(HA-)约为0.0091mol | |
| B. | 该实验应将左边的酸式滴定管换成右边碱式滴定管并加酚酞作指示剂 | |
| C. | 常温下,等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0 | |
| D. | 0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH固体 | B. | NH4Cl固体 | C. | NaNO3固体 | D. | CH3COONa固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
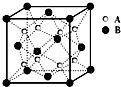 某晶体中晶体结构最小的重复单元如图:A在正方体内,B分别在顶点和面心,则该晶体的化学式为( )
某晶体中晶体结构最小的重复单元如图:A在正方体内,B分别在顶点和面心,则该晶体的化学式为( )| A. | B2A | B. | BA2 | C. | B7A4 | D. | B4A7 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;反应③的化学方程式为2CO2+2Na2O2=2Na2CO3+O2.
;反应③的化学方程式为2CO2+2Na2O2=2Na2CO3+O2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com