
 һ����������ϵ�д�
һ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� | �� | �� | �� | �� | �� | |
| ԭ�Ӱ뾶��10-10m�� | 1.30 | 0.82 | 0.99 | 1.11 | 0.90 | 1.18 |
| �����ͻ��ϼ� | +2 | +3 | +7 | +4 | +2 | +3 |
| -1 | -4 |
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
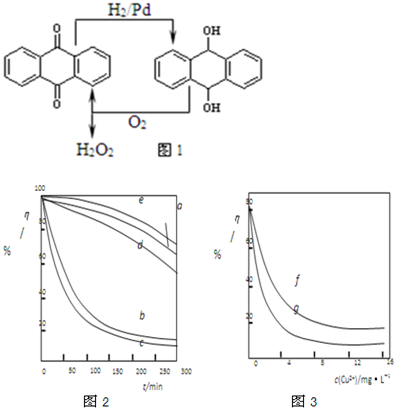
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ������ʡʦ���и߶���ѧ�����п��Ի�ѧ�Ծ����������� ���ͣ������
��8�֣����в��ֶ�����Ԫ�ص����ʻ�ԭ�ӽṹ���±���
| Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
| T | M������2�ԳɶԵ��� |
| X | �����������Ǵ�����������2�� |
| Y | �����µ���Ϊ˫ԭ�ӷ��ӣ����⻯��ˮ��Һ�ʼ��� |
| Z | Ԫ����������ǣ�7�� |
 ��YH
��YH ���ӵĽṹʽΪ ��
���ӵĽṹʽΪ ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�긣��ʡ�����и�����ѧ����ĩ������ѧ�Ծ��������棩 ���ͣ������
���û�ѧ��Ӧԭ���о��⡢�����ȡ���ȵ��ʼ��仯����ķ�Ӧ����Ҫ����
��1����֪��25��ʱKSP��AgCl��=1.6��l0��10 KSP��AgI��=1.5��l0��16
��ˮ�к��д�����Ԫ�أ�����Ԫ�����ȣ���Ԫ����⣬���ں�ˮ�о��Ի���̬���ڡ���25���£���0.1L0.002mol��L��l��NaCl��Һ�м���0.1L0.002mol��L��l��������Һ���а�ɫ�������ɣ�����������ԭ���ǣ�ͨ������ش� ����Ӧ��Ļ���Һ�м�������0.1L0.002mol��L��1��NaI��Һ�������������� �������������ԭ���ǣ������ӷ���ʽ��ʾ�� ��
��2������������Ʊ������ܶ࣬���з�����ԭ����������ߵ��� ������ţ���
A��BaO2 + H2SO4�� BaSO4 �� + H2O2
B��2NH4HSO4 (NH4)2S2O8 +
H2��
(NH4)2S2O8 +
H2��
(NH4)2S2O8 + 2H2O �� 2NH4HSO4 + H2O2
C��CH3CHOHCH3 + O2�� CH3COCH3 + H2O2
D���һ�����������ͼ
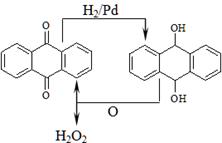
��3��ij���ױ����˲�ͬ�������Ӽ���Ũ�ȶ�˫��ˮ�������⺣��������Һ��Ӧ���ʵ�Ӱ�죬ʵ������ͼ1��ͼ2��ʾ��
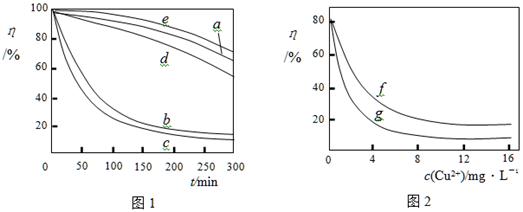
ע������ʵ������¶�Ϊ20�桢w(H2O2)��0.25%��pH��7.12������������ҺŨ��Ϊ8mg��L�D1�������½��С�ͼ1������a��H2O2��b��H2O2+Cu2+��c��H2O2+Fe2+��d��H2O2+Zn2+��e��H2O2+Mn2+��ͼ2������f����Ӧʱ��Ϊ1h��g����Ӧʱ��Ϊ2h����ͼ�е��������������������Һ��ճ�ȣ���������Ũ������Һճ������أ���
��������Ϣ��֪����������������� ������ţ���
A����������ʹ�ý��ⷴӦ���ʼ���
B���������ӶԸý��ⷴӦ�Ĵ�Ч�ʱ�ͭ���ӵ�
C������������Һճ�ȵı仯�����ɷ�ӳ���併�ⷴӦ���ʵĿ���
D��һ�������£�ͭ����Ũ��һ��ʱ����Ӧʱ��Խ��������������ҺŨ��ԽС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013������ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��8�֣����в��ֶ�����Ԫ�ص����ʻ�ԭ�ӽṹ���±���
|
Ԫ�ر�� |
Ԫ�����ʻ�ԭ�ӽṹ |
|
T |
M������2�ԳɶԵ��� |
|
X |
�����������Ǵ�����������2�� |
|
Y |
�����µ���Ϊ˫ԭ�ӷ��ӣ����⻯��ˮ��Һ�ʼ��� |
|
Z |
Ԫ����������ǣ�7�� |
��1��Ԫ��T��ԭ������㹲��______�ֲ�ͬ�˶�״̬�ĵ��ӡ�Ԫ��X��һ��ͬλ�ؿɲⶨ�������������ͬλ�صķ�����_________��
��2��Ԫ��Y����Ԫ�ؿ��γ�����YH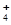 ��YH
��YH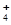 ���ӵĽṹʽΪ
��
���ӵĽṹʽΪ
��
��3��Ԫ��Z��T��ȣ��ǽ����Խ�ǿ����_______����Ԫ�����ƣ������б�������֤����һ��ʵ����________��
a.������Z�ĵ��ʺ�T�ĵ���״̬��ͬ
b.Z���⻯���T���⻯���ȶ�
c.һ��������Z��T�ĵ��ʶ���������������Һ��Ӧ
d.Z������H2����
e.Z��T�����������ϣ���Fe����Z���ɵĻ������м�̬����
��4��д������������ij����Ԫ����ɵķǼ��Է��ӵĽṹʽ
�� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com