
| A. | 2CH3CH2OH+2Na-→2CH3CH2ONa+H2↑ | |
| B. | CH3COOCH2CH3+H2O$?_{△}^{稀硫酸}$CH3COOH+CH3CH2OH | |
| C. | CH2═CH2+Br2-→CH2BrCH2Br | |
| D. | 2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH |
分析 A.乙醇中-OH与Na反应生成氢气;
B.乙酸乙酯水解生成乙醇和乙酸;
C.乙烯中含碳碳双键,与溴发生加成反应;
D.-CHO转化为-COOH,加氧去氢的反应为氧化反应.
解答 解:A.2CH3CH2OH+2Na-→2CH3CH2ONa+H2↑为置换反应,故A不选;
B.CH3COOCH2CH3+H2O$?_{△}^{稀硫酸}$CH3COOH+CH3CH2OH为取代反应,故B不选;
C.CH2═CH2+Br2-→CH2BrCH2Br为加成反应,故C选;
D.2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH,为氧化反应,故D不选;
故选C.
点评 本题考查有机物的结构与性质,为高考常见题型和高频考点,侧重于学生的分析能力和应用能力的考查,注意把握有机物官能团与性质及有机反应,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将乙酸和乙醇的混合液注入浓硫酸中制备乙酸乙酯 | |
| B. | 将铜丝在酒精灯外焰上加热变黑后再移至内焰,铜丝恢复原来的红色 | |
| C. | 在试管中注入2 mL CuSO4溶液,再滴几滴NaOH溶液后,加入乙醛溶液即有红色沉淀生成 | |
| D. | 向苯酚溶液中滴加几滴稀溴水出现白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 降低温度能减慢反应速率 | |
| B. | 单质碳的颗粒变小能加快反应速率 | |
| C. | 增大H2O蒸气的浓度能加快反应速率 | |
| D. | 加入足量的C能使H2O反应完全 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上利用电解法冶炼铝和铁 | |
| B. | 生产和生活中常用可溶性铝盐和铜盐净水 | |
| C. | 工业合成氨的反应属于能自发进行的反应,故能迅速发生 | |
| D. | 热的纯碱溶液清洗带油污的餐具与盐类和酯类的水解均有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
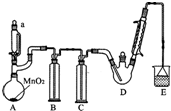 某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:
某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂 | B. | 还原剂 | C. | 催化剂 | D. | 吸附剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com