
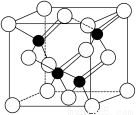
LED照明是我国制造业为人类做出的一大贡献。目前市售LED晶片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如下图。试回答:
(1)镓的基态原子的电子排布式是__________。
(2)砷化镓晶胞中所包含的砷原子(白色球)个数为__________,与同一个镓原子相连的砷原子构成的空间构型为__________。
(3)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是__________。(用氢化物分子式表示)
(4)砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为__________。
(5)比较二者的第一电离能:As__________Ga(填“<”、“>”或“=”)。
(6)下列说法正确的是__________(填字母)。
A.砷化镓晶胞结构与NaCl相同
B.GaP与GaAs互为等电子体
C.电负性:As>Ga
D.砷化镓晶体中含有配位键
(1)1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1)
(2)4 正四面体 (3)NH3>AsH3>PH3 (4)sp2 (5)> (6)BCD
【解析】(1)镓是31号元素,电子排布式为1s22s22p63s23p63d104s24p1。(2)砷化镓晶胞中砷原子8个在立方体顶角,6个在面上,该晶胞所包含砷原子数为8×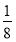 +6×
+6×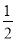 =4,而镓原子周围是4个均匀分布的砷原子为正四面体型。(3)NH3分子间有氢键沸点最高,其它分子按分子量大小排列,NH3>AsH3>PH3。(4)镓原子与3个甲基结合,且镓的价电子都成键,所以为sp2杂化。(5)砷的非金属性强,第一电离能大。(6)砷化镓晶胞与NaCl不同,A项错误。GaP与GaAs原子个数比相同,但电子总数不同,B项错误。As非金属性强,电负性也强,C正确。镓有3个价电子,但形成4个共价键,说明有一个配位键。D正确。
=4,而镓原子周围是4个均匀分布的砷原子为正四面体型。(3)NH3分子间有氢键沸点最高,其它分子按分子量大小排列,NH3>AsH3>PH3。(4)镓原子与3个甲基结合,且镓的价电子都成键,所以为sp2杂化。(5)砷的非金属性强,第一电离能大。(6)砷化镓晶胞与NaCl不同,A项错误。GaP与GaAs原子个数比相同,但电子总数不同,B项错误。As非金属性强,电负性也强,C正确。镓有3个价电子,但形成4个共价键,说明有一个配位键。D正确。


科目:高中化学 来源:2014高考化学苏教版总复习 专题3从矿物到基础材料练习卷(解析版) 题型:选择题
下列说法正确的是( )
A.硅材料广泛应用光纤通讯
B.工艺师利用盐酸刻蚀石英制作艺术品
C.水晶项链和餐桌上的瓷盘都是硅酸盐制品
D.粗硅制备单晶硅不涉及氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题1化学家眼中的物质世界练习卷(解析版) 题型:选择题
下列对非金属元素(除稀有气体元素外)的相关判断正确的是 ( )
①非金属元素都是主族元素
②单质在反应中都只能作氧化剂
③氢化物常温下都是气态,所以都叫气态氢化物
④氧化物常温下都可以与水反应生成酸
⑤非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价
A.②⑤ B.①③⑤ C.②③④ D.①⑤
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题13化学与技术练习卷(解析版) 题型:选择题
化学与生产、生活、环境保护等密切相关。下列叙述正确的是( )
A.用二氧化碳生产肥料可以缓解温室效应
B.处理废水时加入明矾作为消毒剂可以除去水中的杂质
C.为防止电池中的重金属污染,废旧电池应作深埋处理
D.SiO2制成的玻璃纤维,因导电能力强而用于制造通讯光缆
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题13化学与技术练习卷(解析版) 题型:选择题
化学与科学、技术、社会、环境密切相关。下列有关说法中不正确的是( )
A.食用的蛋白质、淀粉和脂肪都可发生水解反应
B.海轮外壳上镶入铅块,可减缓船体的腐蚀速率
C.大力开发和应用氢能源有利于实现“低碳经济”
D.工业上,用电解熔融MgCl2的方法制得金属镁
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题12物质结构与性质练习卷(解析版) 题型:选择题
不能说明元素X的电负性比元素Y的大的是( )
A.与H2化合时X单质比Y单质容易
B.X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强
C.X原子的最外层电子数比Y原子的最外层电子数多
D.X单质可以把Y从其氢化物中置换出来
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题12物质结构与性质练习卷(解析版) 题型:选择题
下列说法正确的是( )
A.离子化合物的熔点一定比共价化合物的高
B.二氧化碳分子中存在共价键和分子间作用力
C.非极性键也可以存在于化合物中
D.甲烷、氨和水都是由极性键结合而成的极性分子
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题11有机化学基础练习卷(解析版) 题型:选择题
分析下表中各项的排布规律,按此规律排布第26项应为( )
1 | 2 | 3 | 4 | 5 |
C2H4 | C2H6 | C2H6O | C2H4O2 | C3H6 |
6 | 7 | 8 | 9 | 10 |
C3H8 | C3H8O | C3H6O2 | C4H8 | C4H10 |
A.C7H16 B.C7H14O2 C.C8H18 D.C8H18O
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师高考模拟演练练习卷(A)(解析版) 题型:填空题
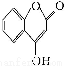 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成
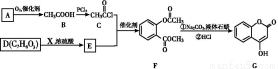
已知:F变成G相当于在F分子中去掉1个X分子。
请回答下列问题:
(1)B→C的反应类型是 。
(2)A与银氨溶液反应生成银镜的化学方程式为 。
(3)G中含有的官能团为碳碳双键、 、 ;1 mol G 最多能与 mol NaOH反应。
(4)G分子中有 种不同环境的氢原子。
(5)写出E→F的化学方程式: 。
(6)含苯环、酯基与D互为同分异构体的有机物有 种,写出其中任意一种有机物的结构简式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com