
科目:高中化学 来源: 题型:选择题
| A. | 馒头在咀嚼过程中产生甜味 | |
| B. | 三氯化铁溶液长期放置产生红褐色固体 | |
| C. | 蛋白质溶液中加入饱和硫酸铵溶液,析出沉淀 | |
| D. | 植物油长期放置发生“酸败产生刺激性气味” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡与盐酸溶液反应 | B. | 葡萄糖在人体内氧化分解 | ||
| C. | 石灰石在高温下的分解反应 | D. | 锌粒与稀H2SO4反应制取H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 粒子代号 | A | B | C | D | E | F | G |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 电荷数 | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
 ,G的化学式是CH4.
,G的化学式是CH4.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑥ | B. | ④⑥ | C. | ③④⑥ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正丁烷的稳定性大于异丁烷 | |
| B. | 异丁烷分子中的碳氢键比正丁烷的多 | |
| C. | 等物质的量的正丁烷能量大于异丁烷能量 | |
| D. | 异丁烷转化为正丁烷的过程是一个放热过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
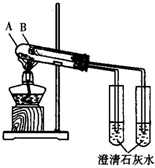 研究Cl2、SO2、CO2、NH3等气体的性质对生产和生活与重要的意义.
研究Cl2、SO2、CO2、NH3等气体的性质对生产和生活与重要的意义.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
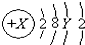 .则下列说法正确的是( )
.则下列说法正确的是( )| A. | 3p能级上的电子数只能为6 | |
| B. | 3d能级上的电子数可能为1-10 | |
| C. | Y可只能为3-8 | |
| D. | 2p,3p能级上的电子数可以相同,也可以不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com