
【题目】已知化学反应①:Fe(s)+CO2(g)![]() FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)![]() FeO(s)+H2(g),其化学平衡常数为K2,在温度973 K和1173 K的情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其化学平衡常数为K2,在温度973 K和1173 K的情况下,K1、K2的值分别如下:
温度 | K1 | K2 |
973 K | 1.47 | 2.38 |
1 173 K | 2.15 | 1.67 |
(1)通过表格中的数值可以推断:反应①是_______(填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g)![]() CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=______。
CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=______。
(3)根据反应①与②可推导出K1、K2与K3之间的关系式为__________,据此关系式及上表数据,能推断出反应③是________(填“吸热”或“放热”)反应。
(4)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有______ 、_____ (填写字母序号)。
A.缩小反应容器的容积 B.扩大反应容器的容积
C.升高温度 D.使用合适的催化剂
E.设法减小平衡体系中的CO的浓度
(5)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:

①图甲中t2时刻发生改变的条件是__________。
②图乙中t2时刻发生改变的条件是__________。
【答案】吸热 ![]() K3=K1/K2 吸热 CE 增大压强或使用催化剂 降低温度或设法分离出H2
K3=K1/K2 吸热 CE 增大压强或使用催化剂 降低温度或设法分离出H2
【解析】
(1)根据表中数据可知,升高温度,K1是增大的,说明升高温度平衡向正反应方向进行,所以反应①是吸热反应。
(2)平衡常数是在一定条件下,可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据方程式可知,平衡常数表达式是K3=![]() 。
。
(3)根据盖斯定律可知,①-②即得到反应③,所以K3=K1/K2;升高温度,K1增大,K2增减小,所以K3是增大,因此正反应是吸热反应。
反应③是体积不变的、吸热的可逆反应,所以要使平衡向正反应方向移动,则可以升高温度,或降低生成物的浓度等,但压强和催化剂不能改变平衡状态,答案选CE。
(5)①图甲中t2时刻正逆反应速率都增大,但平衡不移动,所以改变的条件是增大压强或使用催化剂。
②图乙中t2时刻CO2的浓度增大,而CO的浓度降低,即平衡向逆反应方向进行,所以改变的条件是降低温度或从体系中分离出H2。


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
【题目】血液中的葡萄糖称为血糖,空腹血糖是筛査糖尿病的常用指标,正常范围在3.9-6.1mmol/L(注:1m mol/L= 1×10-3 mol/L);该体检指标表示的是
A.物质的量(n)B.物质的量浓度(c)C.质量分数(ω)D.摩尔质量(M)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是CO和水蒸气发生反应生成CO2和H2的途径和三个状态的能量,该反应为吸热反应,试问:
E1:CO+H2O![]() E2:C+2H+2O
E2:C+2H+2O![]() E3:CO2+H2
E3:CO2+H2
(1)步骤1、2分别是吸热过程还是放热过程?
步骤1:______,步骤2:______。
(2)比较E1、E3的大小______。
(3)已知,25℃时,C(石墨)+1/2O2(g) ═ CO(g) ΔH1=-111 kJ/mol;
H2(g)+1/2O2(g) ═ H2O(g) ΔH2=-242 kJ/mol;
C(石墨)+O2(g) ═ CO2(g) ΔH3=-394 kJ/mol。
则CO和H2O(g)反应的热化学方程式为:______。
(4)含1 mol Ba(OH)2的稀溶液与足量稀盐酸反应放出114.6 kJ的热量,写出该反应中和热的热化学方程式:______。
(5)在C2H2(g)完全燃烧生成CO2和液态水的反应中,每转移5NA个电子放出a kJ的热量。则表示C2H2的燃烧热的热化学方程式为:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙是元素周期表中同一主族的两种元素,若甲的原子序数为 x,则乙的原子序数不可能是
A. x﹣2 B. x+4 C. x+8 D. x+18
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列说法正确的是
A. 162g淀粉和纤维素混合物中氧原子的数目为5NA
B. 常温时,pH=5的盐酸中水电离的OH-数目为10-9NA
C. 5mol的CH3COONa固体溶于水所得溶液中CH3COO-数目为5NA
D. 22.4L Cl2与足量的铁反应,转移的电子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol
CO(g)+1/2O2(g)=CO2(g)△H=-282.9kJ/mol
某H2与CO的混合气体完全燃烧放出113.74kJ热量,同时生成3.6g液态水,则原混合气体中H2与CO的物质的量之比是( )
A. 1:1 B. 1:3 C. 1:4 D. 2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO(g)与H2O(g)反应的能量变化如图所示,有关两者反应的说法正确的是( )

A. 该反应为吸热反应
B. 该反应不需要加热就能进行
C. 1 molCO(g)和1mol H2O(g)具有的总能量大于1 molCO2(g)和1 molH2(g)具有的总能量
D. 1 molCO2(g)和1 molH2(g)反应生成1 molCO(g)和1mol H2O(g)要放出41 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时N电极的质量减少,请回答下列问题:
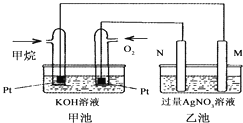
(1)M电极的材料是________,其电极反应式为:________N的电极名称是________,电极反应式为:________
(2)通入甲烷的铂电极的电极反应式为________.
(3)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为________ L(标准状况下)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com