
|
有标准状况下的H2、Cl2混合气a L,经光照反应后,所得气体恰好能使b mol NaOH完全转变成盐.那么a和b的关系不可能是 | |
| [ ] | |
A. |
b= |
B. |
b< |
C. |
b> |
D. |
b≥ |
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
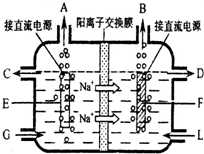 四川盛产井盐,由井盐提取的食盐是日常生活必需品,也是重要的化工原料.
四川盛产井盐,由井盐提取的食盐是日常生活必需品,也是重要的化工原料.2- 4 |
| 加入试剂 |
| 过滤 |
| 适量盐酸 |
| 蒸发、结晶、烘干 |
2- 4 |
| ||
| ||
| ||
ρV1-
|
| ||
ρV1-
|
查看答案和解析>>
科目:高中化学 来源: 题型:


| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
A.b=![]() B.b<
B.b<![]() C.b>
C.b>![]() D.b≥
D.b≥![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com