
【题目】生物燃料电池(BFC)是以有机物为燃料,直接或间接利用酶作为催化剂的一类特殊的燃料电池,其能量转化效率高,是一种真正意义上的绿色电池,其工作原理如图所示。
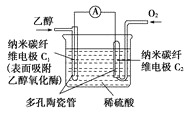
已知C1极的电极反应式为:C2H5OH+3H2O-12e-=2CO2+12H+,下列有关说法不正确的是( )
A. C1极为电池负极,C2极为电池正极
B. 电子由C2极经外电路导线流向C1极
C. C2极的电极反应式为O2+4H++4e-=2H2O
D. 该生物燃料电池的总反应式为:C2H5OH+3O2=2CO2+3H2O
【答案】B
【解析】
在乙醇燃料电池中总反应为C2H5OH+3O2=2CO2+3H2O。其中燃料被氧化,其在原电池的负极上发生氧化反应,负极反应为:C2H5OH+3H2O-12e-=2CO2+12H+;助燃剂(氧气)在正极上发生还原反应,正极反应为O2+4H++4e-=2H2O。以此解题。
A.根据题给电极反应式知,C1极为电池负极,C2极为电池正极,A项正确;
B. 电子由负极C1经外电路流向正极C2极,B项错误;
C.C2极为电池正极,电极反应式为O2+4H++4e-=2H2O,C项正确;
D. 该生物燃料电池为乙醇燃料电池,其总反应式为:C2H5OH+3O2=2CO2+3H2O,D项正确;
答案应选B。


科目:高中化学 来源: 题型:
【题目】室温下,某容积固定的密闭容器由可移动的活塞隔成左、右两室,左室充入等物质的量的氢气和氧气,右室充入一氧化碳和氧气的混合气。同时引燃左右两室的混合气,反应后恢复到室温。反应前后活塞位置如下图所示,则右室混合气体中一氧化碳和氧气的物质的量之比可能是(液态水的体积忽略不计)

①1:1 ②1:2 ③1:3 ④3:1
A. ①② B. ②④ C. ①④ D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】薄荷油中含有少量的α非兰烃和β非兰烃,两者互为同分异构体,其相对分子质量为136。根据如下转化,回答相关问题:
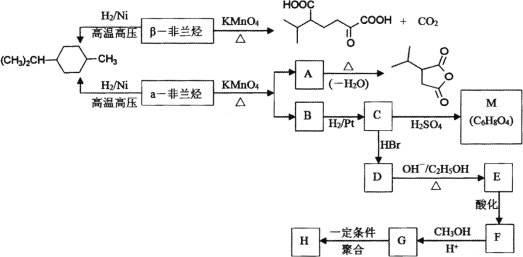
已知:
![]()
![]()
![]() +RCHO
+RCHO
![]()
![]()
![]() +CO2
+CO2
2CH3COOH![]()
![]()
(1) 写出α非兰烃中官能团名称________,β非兰烃的结构简式________。
(2) 下列有关说法正确的是________。
A.α非兰烃与等物质的量的Br2进行加成反应,产物共有3种
B.C→D和E→F反应类型相同
C.聚合物H易溶于水
D.C→M反应过程中有高分子聚合物等副产物产生
(3) 写出F→G的化学方程式________。
(4) 写出符合下列条件的A的同分异构体________。
①含有4个-CH3;②1 mol此同分异构体在碱性条件下水解需2 mol NaOH。
(5) 以甲苯和丙烯为基本原料合成![]() (用流程图表示,其他无机试剂任选)________。
(用流程图表示,其他无机试剂任选)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 已知4℃时四种化合物在水中和液氨中的溶解度如下表:
AgNO3 | Ba(NO3)2 | AgCl | BaCl2 | |
H2O(液) | 170g | 9.2g | 1.5×10-4g | 33. 3g |
NH3(液) | 86g | 97.2g | 0.8g | 0g |
上述四种物质在水中形成复分解反应的离子方程式为_____________________,在液氨中形成复分解反应的化学方程式为______________________________。
II. 现有下列十种物质:①H2 ②铝 ③CaO ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦ 红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质之间可发生离子反应:H++OH-![]() H2O,该离子反应对应的化学方程式为 _____________________________________________
H2O,该离子反应对应的化学方程式为 _____________________________________________
(2)⑩在水中的电离方程式为 ____________________________________
(3)少量的④通入⑥的溶液中反应的离子方程式为_____________________________
过量的④通入⑥的溶液中反应的离子方程式为_______________________________
(4)⑥与过量的碳酸氢钠溶液反应离子方程式:_________________________________
(5)②与⑨发生反应的化学方程式为:Al + 4HNO3 = Al(NO3)3 + NO↑ + 2H2O,
用双线桥标明电子转移的方向和数目__________________________________________,
当有5.4g Al发生反应时,转移电子的数目为 ____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸亚铁([CH3CH(OH)COO]2Fe3H2O,Mr=288)是一种食用的补铁剂,吸收效果比无机铁好,易溶于水,几乎不溶于乙醇,受热易分解,可通过乳酸与碳酸亚铁反应制得。
CH3CH(OH)COOH+FeCO3+2H2O=[CH3CH(OH)COO]2Fe3H2O+CO2↑
FeCO3不溶于水,易被氧化,4FeCO3+6H2O+O2=4Fe(OH)3+4CO2
Ⅰ.乳酸亚铁的制备:
某兴趣小组用FeCl2和NH4HCO3制备FeCO3的装置示意图如图:
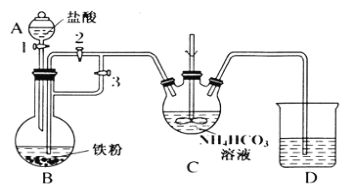
回答下列问题:
(1)C装置中涉及的主要反应的离子方程式_________。
(2)待D处的气体纯净后,将生成的FeCl2溶液和NH4HCO3溶液混合时的操作是_____。
(3)将制得的FeCO3加入到足量乳酸溶液中,再加入少量铁粉,75℃下搅拌反应。加入少量铁粉的作用是_______。
(4)反应结束后,无需过滤,除去过量铁粉的方法是_________。
(5)从所得溶液中获得乳酸亚铁晶体的方法是:________,冷却结晶,过滤, 用适量乙醇洗涤,干燥。
Ⅱ.乳酸亚铁晶体纯度的测量:
(6)该兴趣小组用KMnO4滴定法测定样品中亚铁含量进而计算产品中乳酸亚铁的质量分数,发现产品的质量分数总是大于100%,其原因可能是___。
(7)经查阅文献后,该兴趣小组改用铈(Ce)量法测定产品中Fe2+的含量,滴定反应如下:Ce4++Fe2+=Ce3++Fe3+。取1.440g产品配成100mL溶液,每次取20.00mL,进行必要处理,用0.0500molL-1Ce(SO4)2标准溶液滴定至终点,记录数据如表。
滴定次数 | 滴定前读数(mL) | 滴定后读数(mL) |
1 | 0.20 | 19.95 |
2 | 0.10 | 21.65 |
3 | 0.95 | 20.60 |
则产品中乳酸亚铁的质量分数为________%。(小数点后保留一位数字)
(8)请设计实验证明你购买的乳酸亚铁补铁剂中含Fe2+:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:![]() 在恒温恒容密闭容器中反应,达到平衡状态的标志是
在恒温恒容密闭容器中反应,达到平衡状态的标志是
![]() 单位时间内生成n
单位时间内生成n![]() 的同时消耗2n
的同时消耗2n![]() ;
;
![]() 单位时间内生成n
单位时间内生成n![]() 的同时消耗2nmolNO;
的同时消耗2nmolNO;
![]() 混合气体的颜色不再改变的状态;
混合气体的颜色不再改变的状态;
![]() 混合气体中
混合气体中![]() 不变;
不变;
![]() 的消耗速率与NO的生成速率相等;
的消耗速率与NO的生成速率相等;
![]() 容器内压强不随时间变化而变化。
容器内压强不随时间变化而变化。
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠和碳酸氢钠广泛的应用于我们的生产和生活中。请回答下列问题。
(1)NaHCO3是膨松剂必不可少的成分,受热时能使面胚在焙烧过程中变得松软、多孔。写出受热时NaHCO3发生反应的化学方程式___。
(2)请根据厨房中的物质,设计一实验鉴别某白色粉末是食盐还是食用碱(主要成分为Na2CO3)___。
(3)如图是某兴趣学习小组设计的验证Na2CO3比NaHCO3热稳定性强的实验装置。

①乙处盛放固体药品的化学式是___;②变浑浊的是___烧杯中的澄清石灰水。
(4)兴趣学习小组为研究膨松剂在加热情况下放出气体的量,即:根据单位质量膨松剂产生CO2气体的量来判定其膨胀效果,设计了以下实验,并按如图装置连接(气密性良好,各装置中试剂均过量)。已知:浓硫酸常用于吸收水蒸气;碱石灰是固体氢氧化钠和氧化钙的混合物。回答下列问题:

①装置A中的作用为___。装置E的作用是___,
②如果去掉装置C,该实验会造成测定结果___(“偏大”、“不变”、“偏小”)
③加热前先通入一段时间的空气,再连接D装置,目的是___;停止加热后,还要继续通入一段时间的空气,这样做的目的是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应m A(g)+n B(g) ![]() p C(g)在密闭容器中进行,下图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )
p C(g)在密闭容器中进行,下图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )

A.T1<T2 p1>p2 m+n>p 放热反应B.T1>T2 p1<p2 m+n>p 吸热反应
C.T1<T2 p1>p2 m+n<p 放热反应D.T1>T2 p1<p2 m+n<p 吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有短周期主族元素X、Y、Z、R、T,R原子的最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Y与T同主族。五种元素原子半径与原子序数之间的关系如图所示。下列推断正确的是( )

A. 离子半径:Y<Z
B. 氢化物的沸点:Y<T
C. 最高价氧化物对应水化物的酸性:T<R
D. 由X、Y、Z、R四种元素组成的常见化合物中含有离子键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com