
| A. | 1molCO2 | |
| B. | 标准状况下44.8LH2 | |
| C. | 32gO2 | |
| D. | 1L 1mol/L的碳酸钠溶液中含有的溶质 |
分析 先根据n=$\frac{V}{{V}_{m}}$=$\frac{m}{M}$=cV分别将各选项中的量转化成物质的量,然后对计算结果进行比较即可.
解答 解:A.1molCO2;
B.标准状况下44.8L氢气的物质的量为:$\frac{44.8L}{22.4L/mol}$=2mol;
C.32g氧气的物质的量为:$\frac{32g}{32g/mol}$=1mol;
D.1L 1mol/L的碳酸钠溶液中含有的溶质为:1mol/L×1L=1mol;
根据分析可知,物质的量最大的为B,
故选B.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、物质的量浓度、气体摩尔体积之间的关系为解答关键,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:实验题
 天然气(主要成分甲烷)含有少量含硫化合物[硫化氢、羰基硫(COS)等],可以用氢氧化钠溶液洗涤除去.羰基硫用氢氧化钠溶液处理的过程如下(部分产物已略去):
天然气(主要成分甲烷)含有少量含硫化合物[硫化氢、羰基硫(COS)等],可以用氢氧化钠溶液洗涤除去.羰基硫用氢氧化钠溶液处理的过程如下(部分产物已略去): .反应I除生成两种正盐外,还有水生成,其化学方程式为COS+4NaOH=Na2S+Na2CO3+2H2O.
.反应I除生成两种正盐外,还有水生成,其化学方程式为COS+4NaOH=Na2S+Na2CO3+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘化钾溶液遇淀粉变蓝 | |
| B. | 油脂在酸性条件下水解可以制肥皂 | |
| C. | 苯在溴化铁的催化下能与溴水反应 | |
| D. | 加热时葡萄糖能与新制氢氧化铜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NO3-、AlO2-、K+、Na+ | B. | Ba2+、NH4+、Cl-、NO3- | ||
| C. | Mg2+、SO42-、K+、NO3- | D. | Fe2+、Al3+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题


查看答案和解析>>
科目:高中化学 来源: 题型:推断题
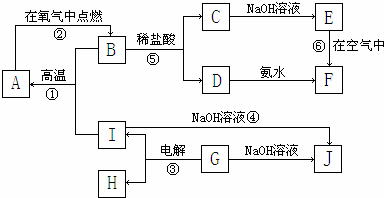
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 2010年12月,一个小学生关于对漂白蘑菇的调查再次引发了人们对滥用漂白剂漂白食品的担忧.曾有不良商贩用过氧化氢漂白食品的记录.下列有关过氧化氢(图是过氧化氢的分子结构)的说法,正确的是( )
2010年12月,一个小学生关于对漂白蘑菇的调查再次引发了人们对滥用漂白剂漂白食品的担忧.曾有不良商贩用过氧化氢漂白食品的记录.下列有关过氧化氢(图是过氧化氢的分子结构)的说法,正确的是( )| A. | 过氧化氢是离子化合物 | |
| B. | 过氧化氢分子既含有非极性键又含有极性键 | |
| C. | 过氧化氢分子只含有极性键 | |
| D. | 过氧化氢分子只含有非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,则该有机物核磁共振氢谱有3个峰.
,则该有机物核磁共振氢谱有3个峰.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌是负极,发生还原反应 | B. | 锌是负极,发生氧化反应 | ||
| C. | 铜是负极,发生还原反应 | D. | 铜是负极,发生氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com