
| A. | 用溶解度数据,可判断煮沸Mg(HCO3)2溶液所得产物是Mg(OH)2还是MgCO3 | |
| B. | 用沸点数据,可推测能否将一些液体混合物用分馏的方法分离开来的可能性 | |
| C. | 用反应热数据的大小,可判断不同反应的反应速率的快慢 | |
| D. | 用原子半径数据,可推断某些原子氧化性或还原性的强弱 |
分析 A.根据的Mg(HCO3)2性质和Mg(OH)2的溶解性分析;
B.沸点相差较大的液体混合物可用分馏的方法分离;
C.反应热的大小取决于反应物与生成物的总能量大小关系,反应速率与物质的自身性质以及外界条件有关;
D.根据原子核对最外层电子的吸引力比较得失电子难易.
解答 解:A.Mg(HCO3)2加热时易分解,一般情况下生成MgCO3,但在解热时分解生成Mg(OH)2沉淀,说明Mg(OH)2比MgCO3溶解度更小,故A正确;
B.由于分馏是利用液体沸点不同分离液体混合物的一种方法,故可以用沸点数据推测两种液体混合物用分馏方法分离开来的可能性,故B正确;
C.反应热的大小取决于反应物与生成物的总能量大小关系,反应速率与物质的自身性质以及外界条件有关,不能用反应热数据的大小判断不同反应的反应速率的快慢,但可用来比较相似反应的快慢,故C错误;
D.原子(或离子)半径越大,原子核对最外层电子的吸引力越小,原子(或离子)越易失去电子,还原性越强,则离子的氧化性越弱,故D正确;
故选C.
点评 本题考查较为综合,涉及难溶电解质的溶解平衡、物质的分离、反应热以及物质的性质等问题,本题难度不大,注意化学中的数据与物质的性质的关系,多积累.


科目:高中化学 来源: 题型:选择题
| A. | m=2 | |
| B. | 两次平衡的平衡常数相同 | |
| C. | X与Y的平衡转化率之比为1:1 | |
| D. | 第二次平衡时,Z的浓度为0.4mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可由石油裂解制取 | B. | 通过加聚反应可制得保鲜膜 | ||
| C. | 通过加成反应可制得氯乙烯 | D. | 能使溴水和酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
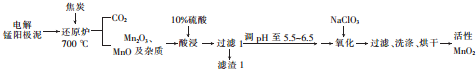
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:K+、Cr2O72-、C6H5OH、CO32- | |
| B. | c(H+)=1×10-13mol/L的溶液中:Cu2+、Na+、Cl-、SO42- | |
| C. | 0.1 mol/L NH4HCO3溶液中:K+、Na+、Cl-、NO3- | |
| D. | 0.1 mol/L Na2SiO3溶液中:K+、Cl-、NO3-、CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
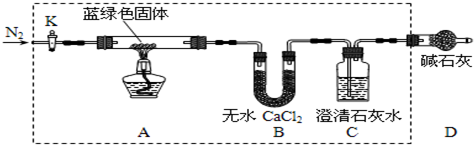
| 溶解度(S)/g | 溶度积(Ksp) | 摩尔质量(M)/g•mol-1 | |||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 | 100 | 197 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
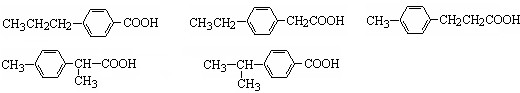 中任意两种.
中任意两种.

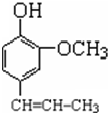 +CH3CH2Cl$\stackrel{一定条件下}{→}$
+CH3CH2Cl$\stackrel{一定条件下}{→}$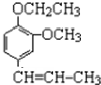 +HCl;
+HCl;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com