
| Ģõ¼žX | ±äĮæY | |
| a | Ń¹Ēæ | ·“Ó¦µÄĘ½ŗā³£Źż |
| b | ĪĀ¶Č | COµÄĘ½ŗāÅØ¶Č |
| c | ĪĀ¶Č | N2µÄĢå»ż·ÖŹż |
| d | “߻ƼĮ | NOµÄĘ½ŗā×Ŗ»ÆĀŹ |
·ÖĪö £Ø1£©ŅŃÖŖ£ŗ¢ŁN2£Øg£©+O2£Øg£©=2NO£Øg£©”÷H=+180.5kJ•mol-1£»
¢Ś2H2£Øg£©+O2£Øg£©=2H2O£Øg£©”÷H=-483.6kJ•mol-1£»
¢ŪN2£Øg£©+3H2£Øg£©=2NH3£Øg£©”÷H=-92.4kJ•mol-1£®
øł¾ŻøĒĖ¹¶ØĀÉ£¬¢Ś”Į3+¢Ł”Į2-¢Ū”Į2æÉµĆ£ŗ4NH3£Øg£©+5O2£Øg£©=4NO£Øg£©+6H2O£Øg£©£»
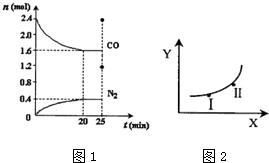
£Ø2£©¢ŁÓÉĶ¼æÉÖŖ£¬20minµ½“ļĘ½ŗā£¬Ę½ŗāŹ±Éś³ÉµŖĘųĪŖ0.4mol£¬ÓÉ·½³ĢŹ½æÉÖŖĻūŗÄNOĪŖ0.4mol”Į2=0.8mol£¬×Ŗ»ÆĀŹ=$\frac{ĪļÖŹµÄĮæ±ä»ÆĮæ}{ĘšŹ¼ĪļÖŹµÄĮæ}$”Į100%£¬øł¾Żv=$\frac{”÷c}{”÷t}$¼ĘĖćv£ØNO£©£»
Čō±£³Ö·“Ó¦ĪĀ¶Č²»±ä£¬ŌŁĻņČŻĘ÷ÖŠ³äČėCO”¢N2ø÷0.8mol£¬ÓÉĘ½ŗā³£Źż±ķ“ļŹ½æÉÖŖ£¬ÅضČÉĢQc£¾K£¬Ę½ŗāÄęĻņŅĘ¶Æ£»
¢Śa£®Ę½ŗā³£ŹżĖęĪĀ¶Č±ä»Æ£¬²»ĖęŃ¹Ēæ±ä»Æ£»
b£®ĪĀ¶ČÉżøߣ¬Ę½ŗāÄęĻņ½ųŠŠ£»
c£®ĪĀ¶ČÉżøߣ¬Ę½ŗāÄęĻņ½ųŠŠ£»
d£®“߻ƼĮøı䷓ӦĖŁĀŹ£¬²»Ó°ĻģĘ½ŗāŅĘ¶Æ£»
£Ø3£©ŅŌN2”¢H2ĪŖµē¼«·“Ó¦Īļ£¬ŅŌHCl-NH4ClČÜŅŗĪŖµē½āÖŹČÜŅŗÖĘŌģŠĀŠĶČ¼ĮĻµē³Ų£¬µŖĘųŌŚÕż¼«µĆµ½µē×Ó·¢Éś»¹Ō·“Ó¦£¬µē¼«·“Ó¦ĪŖN2+8H++6e-ØT2NH4+£»
a£®·Åµē¹ż³ĢÖŠ£¬øŗ¼«µē¼«·“Ó¦ĪŖ£ŗH2-2e-=2H+£¬Õż¼«µē¼«·“Ó¦N2+8H++6e-ØT2NH4+£¬øł¾Żµē×ÓŹŲŗćæÉÖŖ¹ż³ĢÖŠĻūŗÄĒāĄė×Ó£»
b£®Õż¼«Éś³Éļ§øłĄė×Ó£¬ČÜŅŗÖŠµÄNH4ClÅضČŌö“󣬵«Cl-Ąė×ÓÅØ¶Č²»±ä£»
c£®µē¼«·“Ó¦Īļ±»Ńõ»ÆµÄŹĒĒāĘų£¬øł¾Żµē×ÓŹŲŗć¼ĘĖćĒāĘųµÄĮ棬ŌŁøł¾ŻV=nVm¼ĘĖćĒāĘųĢå»ż£»
d£®Ōµē³Ų¹¤×÷¹ż³ĢÖŠĻūŗÄĒāĄė×Ó£®
½ā“š ½ā£ŗ£Ø1£©ŅŃÖŖ£ŗ¢ŁN2£Øg£©+O2£Øg£©=2NO£Øg£©”÷H=+180.5kJ•mol-1£»
¢Ś2H2£Øg£©+O2£Øg£©=2H2O£Øg£©”÷H=-483.6kJ•mol-1£»
¢ŪN2£Øg£©+3H2£Øg£©=2NH3£Øg£©”÷H=-92.4kJ•mol-1£®
øł¾ŻøĒĖ¹¶ØĀÉ£¬¢Ś”Į3+¢Ł”Į2-¢Ū”Į2æÉµĆ£ŗ4NH3£Øg£©+5O2£Øg£©=4NO£Øg£©+6H2O£Øg£©”÷H=-905kJ/mol£¬
¹Ź“š°øĪŖ£ŗ4NH3£Øg£©+5O2£Øg£©=4NO£Øg£©+6H2O£Øg£©”÷H=-905kJ/mol£»
£Ø2£©¢ŁÓÉĶ¼æÉÖŖ£¬20minµ½“ļĘ½ŗā£¬Ę½ŗāŹ±Éś³ÉµŖĘųĪŖ0.4mol£¬ÓÉ·½³ĢŹ½æÉÖŖĻūŗÄNOĪŖ0.4mol”Į2=0.8mol£¬NO×Ŗ»ÆĀŹ=$\frac{0.8mol}{2.8mol}$”Į100%=28.57%£¬v£ØNO£©=$\frac{\frac{0.8mol}{2L}}{20min}$=0.02mol/£ØL•min£©£¬
Čō±£³Ö·“Ó¦ĪĀ¶Č²»±ä£¬ŌŁĻņČŻĘ÷ÖŠ³äČėCO”¢N2ø÷0.8mol£¬ÓÉĘ½ŗā³£Źż±ķ“ļŹ½K=$\frac{c£Ø{N}_{2}£©”Į{c}^{2}£ØC{O}_{2}£©}{{c}^{2}£ØNO£©”Į{c}^{2}£ØCO£©}$æÉÖŖ£¬ÅضČÉĢQc£¾K£¬Ę½ŗāÄęĻņŅĘ¶Æ£»
¹Ź“š°øĪŖ£ŗ28.57%£»0.02mol/£ØL•min£©£»Ļņ×ó£»
¢Ś2NO£Øg£©+2CO£Øg£©?N2£Øg£©+2CO2£Øg£©”÷H£¼0£¬·“Ó¦ŹĒĘųĢåĢå»ż¼õŠ”µÄ·ÅČČ·“Ó¦£¬Ķ¼ĻóÖŠXĖęYŌö“ó¶ųŌö“ó£»
a£®Ę½ŗā³£ŹżĖęĪĀ¶Č±ä»Æ£¬²»ĖęŃ¹Ēæ±ä»Æ£¬¹Źa²»·ūŗĻ£»
b£®ĪĀ¶ČÉżøߣ¬Ę½ŗāÄęĻņ½ųŠŠ£¬Ņ»Ńõ»ÆĢ¼ÅضČŌö“󣬹Źb·ūŗĻ
c£®ĪĀ¶ČÉżøߣ¬Ę½ŗāÄęĻņ½ųŠŠ£¬µŖĘųŗ¬Įæ¼õŠ”£¬¹Źc²»·ūŗĻ£»
d£®“߻ƼĮøı䷓ӦĖŁĀŹ£¬²»Ó°Ļģ»ÆŃ§Ę½ŗā£¬NO×Ŗ»ÆĀŹ²»±ä£¬¹Źd²»·ūŗĻ£»
¹Ź“š°øĪŖ£ŗb£»
£Ø3£©ŅŌN2”¢H2ĪŖµē¼«·“Ó¦Īļ£¬ŅŌHCl-NH4ClČÜŅŗĪŖµē½āÖŹČÜŅŗÖĘŌģŠĀŠĶČ¼ĮĻµē³Ų£¬µŖĘųŌŚÕż¼«µĆµ½µē×Ó·¢Éś»¹Ō·“Ó¦£¬µē¼«·“Ó¦ĪŖN2+8H++6e-ØT2NH4+£»
a£®·Åµē¹ż³ĢÖŠ£¬øŗ¼«µē¼«·“Ó¦ĪŖ£ŗH2-2e-=2H+£¬Õż¼«µē¼«·“Ó¦N2+8H++6e-ØT2NH4+£¬øł¾Żµē×ÓŹŲŗćæÉÖŖ¹ż³ĢÖŠĻūŗÄĒāĄė×Ó£¬µē½āÖŹČÜŅŗPHÉżøߣ¬¹Źa“ķĪó£»
b£®Õż¼«Éś³Éļ§øłĄė×Ó£¬ČÜŅŗÖŠµÄNH4ClÅضČŌö“󣬵«Cl-Ąė×ÓÅØ¶Č²»±ä£¬¹ŹbÕżČ·£»
c£®Ćæ×ŖŅĘ6.02”Į1023øöµē×Ó£¬¼“×ŖŅʵē×ÓĪŖ1mol£¬µē¼«·“Ó¦Īļ±»Ńõ»ÆµÄŹĒĒāĘų£¬øł¾Żµē×ÓŹŲŗć£¬ĒāĘų±»Ńõ»ÆµÄĪļÖŹµÄĮæĪŖ0.5mol£¬Ōņ±ź×¼×“æöĻĀĒāĘųĢå»żĪŖ11.2L£¬¹ŹcÕżČ·£»
d£®Ōµē³Ų¹¤×÷¹ż³ĢÖŠĻūŗÄĒāĄė×Ó£¬ĪŖ±£³Ö·ÅµēŠ§¹ū£¬µē³ŲŹ¹ÓĆŅ»¶ĪŹ±¼äŠčøü»»µē½āÖŹČÜŅŗ£¬¹ŹÕżČ·£¬
¹Ź“š°øĪŖ£ŗN2+8H++6e-ØT2NH4+£» bcd£®
µćĘĄ ±¾Ģāæ¼²éøĒĖ¹¶ØĀÉÓ¦ÓĆ”¢»ÆŃ§Ę½ŗāµÄÓŠ¹Ų¼ĘĖćÓėÓ°ĻģŅņĖŲ”¢Ōµē³ŲŌĄķµČ£¬»ÆŃ§Ę½ŗā³£ŹżµÄÓŠ¹Ų¼ĘĖćŹĒ½ü¼øÄźøßæ¼ČČµć£¬ÕĘĪÕĘ½ŗā³£ŹżÓ¦ÓĆ£¬ĢāÄæÄѶČÖŠµČ£®


 ѧŅµ²āĘĄŅ»æĪŅ»²āĻµĮŠ“š°ø
ѧŅµ²āĘĄŅ»æĪŅ»²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £¬
£¬²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
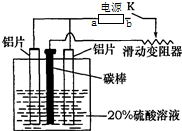 ĀĮµÄŃō¼«Ńõ»Æ£¬ŹĒŅ»ÖÖ³£ÓĆµÄ½šŹō±ķĆꓦĄķ¼¼Źõ£¬ĖüÄÜŹ¹ĀĮµÄ±ķĆęÉś³ÉŅ»²ćÖĀĆܵÄŃõ»ÆĤ£®Ä³»Æѧъ¾æŠ”×éŌŚŹµŃéŹŅÖŠ°“ĻĀĮŠ²½ÖčÄ£ÄāøĆÉś²ś¹ż³Ģ£¬×°ÖĆČēĶ¼£®ĢīŠ“ĻĀĮŠæÕ°×£ŗ
ĀĮµÄŃō¼«Ńõ»Æ£¬ŹĒŅ»ÖÖ³£ÓĆµÄ½šŹō±ķĆꓦĄķ¼¼Źõ£¬ĖüÄÜŹ¹ĀĮµÄ±ķĆęÉś³ÉŅ»²ćÖĀĆܵÄŃõ»ÆĤ£®Ä³»Æѧъ¾æŠ”×éŌŚŹµŃéŹŅÖŠ°“ĻĀĮŠ²½ÖčÄ£ÄāøĆÉś²ś¹ż³Ģ£¬×°ÖĆČēĶ¼£®ĢīŠ“ĻĀĮŠæÕ°×£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
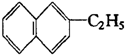 ŹōÓŚŻĮµÄĶ¬ĻµĪļ£¬ŌņŻĮŗĶŻĮµÄĶ¬ĻµĪļ·Ö×Ó×é³ÉĶØŹ½ĪŖCnH2n-12 £Øn”Ż10£©£®
ŹōÓŚŻĮµÄĶ¬ĻµĪļ£¬ŌņŻĮŗĶŻĮµÄĶ¬ĻµĪļ·Ö×Ó×é³ÉĶØŹ½ĪŖCnH2n-12 £Øn”Ż10£©£® ¢Ś±ūµÄ½į¹¹¼ņŹ½ĪŖ
¢Ś±ūµÄ½į¹¹¼ņŹ½ĪŖ £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com