
【题目】25℃时,向500 mL0.2 mol/L NaOH溶液中通入SO2气体(忽略反应过程中溶液的体积变化),设反应过程中![]() =x,已知H2SO3的电离平衡常数:Ka1=1.2×10-2,Ka2=5.6×10-8。下列说法正确的是( )
=x,已知H2SO3的电离平衡常数:Ka1=1.2×10-2,Ka2=5.6×10-8。下列说法正确的是( )
A. x=1时,c(SO32-)+c(HSO3-)=0.2 mol/L
B. x<1时,溶液可能为酸性
C. x=![]() 时,c(SO32-)+c(HSO3-)+c(OH-)=c(Na+)+c(H+)
时,c(SO32-)+c(HSO3-)+c(OH-)=c(Na+)+c(H+)
D. x<![]() 时,随通入SO2量增大,
时,随通入SO2量增大,![]() 逐渐减小
逐渐减小
科目:高中化学 来源: 题型:
【题目】已知p(A)=-lg c(A)。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是( )
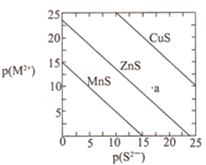
A.a点无ZnS沉淀生成
B.可用MnS除去MnCl2溶液中混有的少量ZnCl2
C.CuS和MnS共存的悬浊液中,c(Cu2+)/c(Mn2+)=10-20
D.向CuS悬浊液中加入少量水,平衡向溶解的方向移动,c(S2-)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅作为一种新型能源被广泛开发利用,关于其有利因素下列说法中,你认为不正确的是( )
A.硅燃烧产物对环境产生的污染,容易得到有效控制
B.从Si(s)+O2(g)![]() SiO2(s) ΔH=-858.6 kJ·mol-1可知,硅燃烧放出的热量多
SiO2(s) ΔH=-858.6 kJ·mol-1可知,硅燃烧放出的热量多
C.自然界中硅的贮存量丰富,可以从自然界直接获得单质硅
D.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中一定量的A、B气体混合发生反应:xA(g) +yB(g)![]() zC(g),平衡时测得A的浓度为0.50mol·L-1。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.20 mol·L-1。下列判断不正确的是
zC(g),平衡时测得A的浓度为0.50mol·L-1。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.20 mol·L-1。下列判断不正确的是
A.x+y<zB.平衡向正反应方向移动
C.B的转化率降低D.C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯,反应装置如图。下列对该实验的叙述错误的是
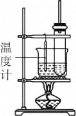
A.长玻璃管起冷凝回流作用
B.水浴加热其优点是受热均匀,便于控制温度
C.粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤
D.洗涤后,用无水CaCl2干燥,然后过滤,得到纯硝基苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)常温下,将m mol·L-1的CH3COOH溶液和n mol·L-1NaOH溶液等体积混合后,溶液的pH=7,则m与n的大小关系是m____n(填“>”、“<”或“=”,下同),原酸中c(H+)与碱中c(OH-)的大小关系是c(H+)____c(OH-)。
(2)常温下,将浓度均为0.1mol·L-1的CH3COONa、CH3COOH溶液等体积混合后,溶液呈酸性。则混合溶液中各离子浓度由大到小排序为_____。关于该混合溶液的说法不正确的是___(填代号)。
a.此溶液一定有c(Na+)+c(H+)=c(OH-)+c(CH3COO-)
b.此溶液一定有c(Na+)=c(CH3COOH)+c(CH3COO-)
c.此溶液中水的电离程度一定大于纯水的电离程度
d.向此溶液中加少量氢氧化钠或盐酸,溶液pH变化不大
(3)用0.1000 mol·L-1NaOH溶液滴定20.00mL某浓度的CH3COOH溶液,滴定曲线如右图所示。其中点①所示溶液中c(CH3COO-)=1.7c(CH3COOH),点③所示溶液中c(CH3COO-)+c(CH3COOH)=c(Na+)。列式并计算醋酸的电离常数_____,CH3COOH的物质的量浓度为____ mol·L-1。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组采用碘量法测定河水中的溶解氧。实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2,实现氧的固定。
Ⅱ.酸化、滴定
将固氧后的水样酸化,MnO(OH)2被I还原为Mn2+,在暗处静置5 min,然后用标准Na2S2O3溶液滴定生成的I2(2![]() +I2 = 2I+
+I2 = 2I+![]() )。
)。
回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是_____。
(2)“氧的固定”中发生反应的化学方程式为___________。
(3)Na2S2O3能水解,则滴定时Na2S2O3溶液应装在_____(填下图中的仪器编号)。请补充润洗该仪器的操作方法:从滴定管____加入3~5mL所要盛装的溶液,__________,然后,一手控制活塞(酸式滴定管轻轻转动活塞;碱式滴定管轻轻挤压玻璃球),将液体从滴定管__放入预置的烧杯中。
甲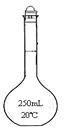 乙
乙 丙
丙![]() 丁
丁![]()
(4)某次滴定前滴定管液面如图所示,读数为________mL。
![]()
(5)量取100.00 mL水样经固氧、酸化后,从中取20.00 mL放入锥形瓶,用a mol·L1Na2S2O3溶液滴定,以淀粉溶液作指示剂,终点现象为________________;若消耗Na2S2O3溶液的体积为b mL,则水样中溶解氧的含量为__mg·L1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:2H2(g)+O2(g) ![]() 2H2O(l) H= -571.6 kJ·mol-1,2CH3OH(l)+3O2(g)
2H2O(l) H= -571.6 kJ·mol-1,2CH3OH(l)+3O2(g) ![]() 2CO2(g)+4H2O(l) H= -1452 kJ·mol-1,H+(aq)+OH-(aq)
2CO2(g)+4H2O(l) H= -1452 kJ·mol-1,H+(aq)+OH-(aq) ![]() H2O(l) H= -57.3 kJ·mol-1。据此判断下列说法正确的是
H2O(l) H= -57.3 kJ·mol-1。据此判断下列说法正确的是
A. CH3OH的燃烧热为1452 kJ·mol-1
B. 2H2(g)+O2(g) ![]() 2H2O(g) H > -571.6 kJ·mol-1
2H2O(g) H > -571.6 kJ·mol-1
C. CH3COOH(aq)+NaOH(aq) ![]() H2O(l)+CH3COONa(aq) H= -57.3 kJ·mol-1
H2O(l)+CH3COONa(aq) H= -57.3 kJ·mol-1
D. 2CH3OH(l)+O2(g) ![]() 2CO2(g)+4H2(g) H= -880.4 kJ·mol-1
2CO2(g)+4H2(g) H= -880.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚氨酯类高分子材料PU用途广泛,其合成反应为:
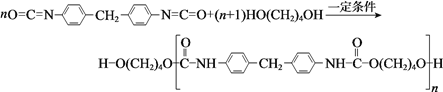
下列说法不正确的是
A. HO(CH2)4OH的沸点高于CH3CH2CH2CH3
B. 高分子材料PU在强酸、强碱中能稳定存在
C. 合成PU的两种单体的核磁共振氢谱中均有3个吸收峰
D. 以1,3-丁二烯为原料,可合成HO(CH2)4OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com