
| A. | 亚硫酸钠 | B. | 酒精 | C. | 氢氧化钾 | D. | 氯化氢 |
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:解答题

 ;
;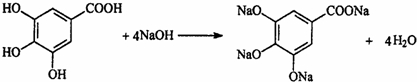 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| J | ||||
| R | T |
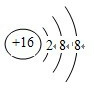 .
.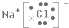 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
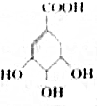 是从烹调香料“八角”提取的一种有机物,是合成抗禽流感药物的基本原料,1mol莽草酸与足量的Na和NaOH反应,消耗的Na和NaOH的物质的量之比为( )
是从烹调香料“八角”提取的一种有机物,是合成抗禽流感药物的基本原料,1mol莽草酸与足量的Na和NaOH反应,消耗的Na和NaOH的物质的量之比为( )| A. | 4:1 | B. | 1:1 | C. | 3:1 | D. | 1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com