
| A. | Al2O3既不是氧化剂也不是还原剂 | B. | Cl2被还原 | ||
| C. | 每生成1 mol CO2转移2 mol电子 | D. | CO2为氧化产物 |
分析 反应2Al2O3+3C+6Cl2$\frac{\underline{\;高温\;}}{\;}$4AlCl3+3CO2中,氯气得到电子生成氯化铝,氯气为氧化剂,C在反应中失去电子被氧化成二氧化碳,C为还原剂,据此进行解答.
解答 解:反应2Al2O3+3C+6Cl2$\frac{\underline{\;高温\;}}{\;}$4AlCl3+3CO2中,氯气得到电子生成氯化铝,氯气为氧化剂,C在反应中失去电子被氧化成二氧化碳,C为还原剂,
A.Al2O3中各元素的化合价不变,既不是氧化剂也不是还原剂,故A正确;
B.氯气为氧化剂,在反应中被还原,故B正确;
C.生成3mol二氧化碳转移12mol电子,则每生成1 mol CO2转移4 mol电子,故C错误;
D.C在反应中从0价生成+4价的二氧化碳,反应中失去电子,所以CO2为氧化产物,故D正确;
故选C.
点评 本题考查氧化还原反应,题目难度不大,明确氧化还原反应的特征为解答关键,转移掌握氧化剂与还原剂、氧化反应与还原反应的概念及判断方法,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
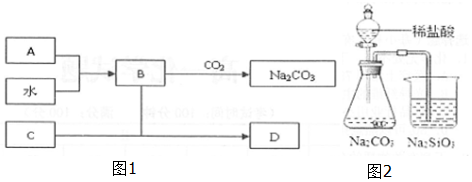
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验及现象 | 结论 |
| A | 将湿润红色石蕊试纸靠近试管口 | 反应中有NH3产生 |
| B | 收集产生的气体并点燃,火焰呈淡蓝色 | 反应中有H2产生 |
| C | 收集气体的同时测得溶液的pH为8.0 | 生成Mg(OH)2使溶液呈弱碱性 |
| D | 向NH4Cl溶液中加锌,也有大量气泡产生 | 活泼金属可促进NH4+水解 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2溶液 | B. | NaOH溶液 | C. | 氨水 | D. | 硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C8H10中只有3种属于芳香烃的同分异构体 | |
| B. | 苯与溴水混合振荡,水层颜色变浅 | |
| C. | 煤经过气化和液化等物理变化可转化为清洁燃料 | |
| D. | 油脂、蛋白质、纤维素均属于高分子化合物,可以发生水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
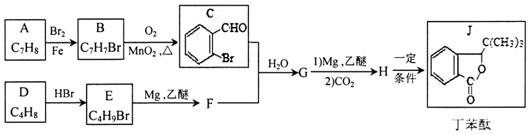
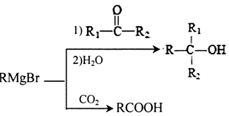
 .H发生缩聚反应生成的高分子化合物的结构简式为
.H发生缩聚反应生成的高分子化合物的结构简式为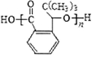 .
.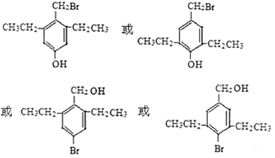 .
.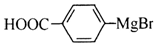 能与CO2反应生成有机物M.符合下列条件的M的同分异构体共有10种.
能与CO2反应生成有机物M.符合下列条件的M的同分异构体共有10种.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com