
向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
(1)写出反应的离子方程式___________________________
(2)下列三种情况下,离子方程式与(1)相同的是________(填序号).
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO 恰好完全沉淀
恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
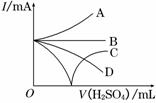
(3)若缓缓加入稀H2SO4直至过量,整个过程中混合溶液中的导电能力(用电流强度I表示)可近似地用右图中的曲线表示是________(填序号).
(4)若向装有Ba(OH)2溶液烧杯里缓缓滴入KAl(SO4)2溶液至Ba2+恰好完全反应.则反应的离子方程式是 _________________________________.
【知识点】离子方程式、元素化合物B1C5
【答案解析】(1)Ba2++2OH-+2H++SO ===BaSO4↓+2H2O (2)A (3)C
===BaSO4↓+2H2O (2)A (3)C
(4) 2Ba +4OH+Al
+4OH+Al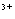 +2SO
+2SO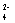 =2BaSO ↓ + AlO+2HO
=2BaSO ↓ + AlO+2HO
解析:⑴Ba(OH)2溶液中逐滴加入稀硫酸生成水和硫酸钡沉淀,离子反应为Ba2++2OH-+2H++SO ===BaSO4↓+2H2O
===BaSO4↓+2H2O
⑵A的离子反应分别是Ba2++2OH-+2H++SO ===BaSO4↓+2H2O,B、C的离子反应是Ba2++OH-+H++SO
===BaSO4↓+2H2O,B、C的离子反应是Ba2++OH-+H++SO ===BaSO4↓+H2O,选A。
===BaSO4↓+H2O,选A。
⑶随着H2SO4的加入至二者刚好反应时,溶液的导电能力逐渐减弱至不导电,随后硫酸过量,溶液的导电能力逐渐增强,选C。
⑷若向装有Ba(OH)2溶液烧杯里缓缓滴入KAl(SO4)2溶液至Ba2+恰好完全反应,此时二者物质的量比为2:1,则OH-与Al3+的物质的量比为4:1,Al3+全部变为AlO2-,即
2Ba +4OH+Al
+4OH+Al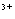 +2SO
+2SO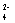 =2BaSO ↓ + AlO+2HO。
=2BaSO ↓ + AlO+2HO。
【思路点拨】本题⑷的离子方程式的书写可采取目标法:1molBa2+恰好完全反应,则需KAl(SO4)20.5mol,而OH-与Al3+的物质的量比则为4:1,Al3+全部变为AlO2-。


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.臭氧(O3)是一种有鱼腥味、氧化性极强的淡蓝色气体,可用作自来水的消毒剂
B.人造纤维可利用竹子、棉花、麻类的纤维材料制成,而合成纤维是利用自然界的非纤维材料(如石油、煤)通过化学合成方法得到
C.铝及其合金是电气、工业、家庭广泛使用的材料,是因为铝的冶炼方法比较简单
D.有机玻璃是以有机物A(甲基丙烯酸甲酯)为单体,通过加聚反应得到,合成A的一种途经是:CH3C≡CH+CO+CH3OH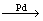
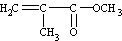 ,其过程符合绿色化学的原则
,其过程符合绿色化学的原则
查看答案和解析>>
科目:高中化学 来源: 题型:
关于下列各实验装置的叙述中,不正确的是( )
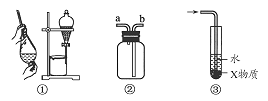
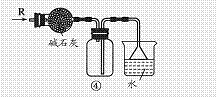
A.装置①可用于分离C2H5OH和H2O的混合物
B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体
C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸
D.装置④可用于干燥、收集NH3,并吸收多余的NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
在“绿色化学”工艺中,理想状态是反应中原子全部转化为欲制的产物,即原子利用率为100%。以下反应最符合绿色化学原子经济要求的是
A. 乙烯聚合为聚乙烯高分子材料 B. 甲烷与氯气制备一氯甲烷
C. 以铜和浓硝酸为原料生产硝酸铜 D. 用二氧化硅制备高纯硅
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组中,不管以何种比例混合,只要总质量一定,充分燃烧后生成的二氧化碳物质的量不变的是
A.乙烯(C2H4)和乙炔(C2H2) B.乙醇和丙醇(CH3CH2CH2OH)
C.乙醇和乙醚(C2H5OC2H5) D.甲醛( HCHO)和乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ、(1)若烧杯中溶液为稀硫酸,则观察到的现象是___________________
 负极反应式为:______________________________。
负极反应式为:______________________________。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为________(填Mg或Al),总反应化学方程式为____________________________________。
Ⅱ、由Al、Cu、浓硝酸组成原电池,其正极的电极反应式为
 Ⅲ、中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。
Ⅲ、中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。
①该电池工作时,b口通入的物质为_______,
c口通入的物质为______。
②该电池负极的电极反应式为:_______
③工作一段时间后,当12.8 g甲醇完全反应生成CO2时,有______________NA个电子转移。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中有CO、H2、O2共16.5g和足量的Na2O2,用电火花引燃,使其完全反应,Na2O2增重7.5g,则原混合气体中O2的质量分数是
A. 54.5% B.40% C.36% D.33.3%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com