
【题目】下列物质的保存方法,与其化学性质无关的是( )
A.金属钠保存在煤油中
B.浓盐酸需密闭保存
C.新制氯水密闭存放于棕色瓶中
D.过氧化钠需保持干燥密闭保存
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】已知反应2HI(g)![]() H2(g) +I2(g)的能量变化如图所示。下列说法正确的是
H2(g) +I2(g)的能量变化如图所示。下列说法正确的是

A. 常温下,向体积为VL的容器中充入2mol HI(g)充分反应,可吸收12.5kJ的热量
B. 加入催化剂,分子的能量不变,但单位体积活化分子数增多,速率加快
C. 其他条件不变,升高温度,反应速率加快,HI分解率不变
D. H2(g) +I2(g)![]() 2HI(g)的活化能Ea为12.5kJ·mol1
2HI(g)的活化能Ea为12.5kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,试回答:
①增加Fe的量,其反应速率____(填“增大”、“不变”或“减小”,下同)。
②将容器的体积缩小一半,其反应速率____。
③保持体积不变,充入He,其反应速率____。
④保持压强不变,充入He,其反应速率_____。
(2)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和NH3,在一定条件下发生反应:6NO(g)+4NH3(g)![]() 5N2(g)+6H2O(g)。
5N2(g)+6H2O(g)。
①能说明该反应已达到平衡状态的标志是____(填字母序号)
a.反应速率5v(NH3)=4v(N2)
b.单位时间里每生成5mol N2,同时生成4mol NH3
c.容器内N2的物质的量分数不再随时间而发生变化
d.容器内n(NO):n(NH3):n(N2):n(H2O)=6:4:5:6
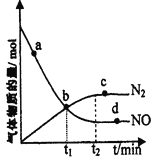
②某次实验中测得容器内NO及N2的物质的量随时间变化如图所示,图中v(正)与v(逆)相等的点为_____(选填字母)。
(3)298K时,若已知生成标准状况下2.24LNH3时放出热量为4.62kJ。写出合成氨反应的热化学方程式____。
(4)一定条件下,在2L密闭容器内,反应2NO2(g)=N2O4(g)△H=-180kJ·mol-1,n(NO2)随时间变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)/mol | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
用NO2表示0~2s内该反应的平均速度____。在第5s时,NO2的转化率为____。根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)可用作催化剂、杀菌剂、媒染剂、脱色剂。CuCl是一种白色粉末,微溶于水、不溶于乙醇,在潮湿的空气中易被氧化。实验室采用如图装置和下列步骤制备氯化亚铜。

步骤1:在三颈烧瓶中加入20%盐酸、食盐、铜屑,加热至60~70℃,开动搅拌器,同时从c口缓慢通入氧气,制得Na[CuCl2]溶液。
步骤2:反应完全后,冷却,过滤,滤液用适量的水稀释,析出CuCl。
步骤3:过滤,分别用盐酸、乙醇洗涤滤出的固体。
步骤4:在真空干燥器中60~70 ℃干燥2h,冷却后得到产品。
回答下列问题:
(1)质量分数为20%的盐酸密度为1.1g/cm3,物质的量浓度为___________;配制20%盐酸需要的玻璃仪器有:__________、烧杯、玻璃棒、胶头滴管。
(2)步骤1中制得Na[CuCl2]的化学方程式为________________________________。
(3)根据“步骤2中用水稀释滤液能得到CuCl”推测,滤液中存在的平衡是____________。
(4)析出的CuCl晶体不用水而用盐酸、乙醇分别洗涤的目的是__________________。
(5)测定产品中氯化亚铜的质量分数,实验过程如下:
准确称取制备的氯化亚铜产品0.25 g,将其置于足量的FeCl3溶液中,待样品全部溶解后,加入适量稀硫酸,用0.10 mol/L的硫酸铈[Ce(SO4)2]标准溶液滴定到终点,消耗硫酸铈溶液24.50 mL,反应中Ce4+被还原为Ce3+。(已知:CuCl+FeCl3=CuCl2+FeCl2)
①硫酸铈标准溶液应盛放在________(填“酸”或“碱”)式滴定管中。
②产品中氯化亚铜的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在元素周期表中,元素性质随原子序数的递增呈现周期性变化的本质原因是( )
A.中子数逐渐增多
B.相对原子质量逐渐增大
C.核外电子排布呈现周期性变化
D.元素化合价呈现周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了清理路面积雪,人们常使用一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54mol电子。
(1)该融雪剂的化学式是____,该物质中化学键类型是______,电子式是______。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是__________;D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8e-稳定结构,该分子的结构式为_________,电子式为_______,化学键类型为_________(填“离子键”“非极性共价键”或“极性共价键”)。
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中反应时有两种产物:不加热时生成____,其化学键类型为___;加热时生成_____,其化学键类型为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AOH为弱碱,已知:2AOH(aq)+H2SO4(aq)===A2SO4(aq)+2H2O(l) ΔH1=-24.2 kJ·mol-1;H+(aq)+OH-(aq)===H2O(l) ΔH2=-57.3 kJ·mol-1。则AOH在水溶液中电离的ΔH为( )
A. +33.1 kJ·mol-1 B. +45.2 kJ·mol-1 C. -81.5 kJ·mol-1 D. -33.1 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积为2 L的固定密闭容器中通入2mol X气体,在一定温度下发生如下反应:2X(g) ![]() Y(g)+3Z(g)ΔH=+92.0kJ· mol-1。经5 min 后反应达到平衡,此时测得容器内的压强为起始时的1.5倍。
Y(g)+3Z(g)ΔH=+92.0kJ· mol-1。经5 min 后反应达到平衡,此时测得容器内的压强为起始时的1.5倍。
(1)用Y表示的化学反应速率为_____,X的转化率为______,平衡时反应吸收的热量为_________。
(2)在定温,定容的条件下向平衡体系中再充入1mol X(g)气体,平衡______(填“正向”“不”“逆向”)移动, X(g)的转化率______(填“增大”“减小”“不变”),Y(g)的质量分数______(填“增大”“减小”“不变”)。
(3)在相同温度,相同容积的密闭容器中起始时充入0.8molX(g),0.6molY(g),1.8molZ(g),此时V正______V逆(填“大于”、“小于”或“等于”);平衡时X(g)的百分含量______ (填“大于”、“小于”或“等于”)原平衡。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、M的原子序数依次增大,其中X、Y、Z 三种元素中,可形成含二种元素的10电子微粒m、n、p、q,且有反应m+n![]() p
p![]() +q;M的最高价氧化物对应的水化物为最强酸。则下列说法正确是
+q;M的最高价氧化物对应的水化物为最强酸。则下列说法正确是
A. 原子半径X<M<Z<Y B. 非金属性X <M<Z<Y
C. X、Y、Z三种元素组成的化合物的水溶液一定呈酸性 D. MZ2可用于自来水的杀菌消毒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com