
һ�ֻ�϶����������Էֱ��õ綯������ȼ�����߶��߽���ƶ����֡��������»����ʱ���綯���ṩ�ƶ������������͵����ģ���ɲ��������ʱ��ȼ���ṩ�ƶ�����ʹ�綯�����ڳ��״̬��Ŀǰ��ȼ��������Ϊȼ�ϣ��綯��һ��ʹ�������أ�KOH�����Һ����
�Է����ش��������⣺
��1����֪������ɲ��������ʱ�����������缫��Ӧ�ֱ�Ϊ��
�缫��M+H2O+e-��MH+OH-��MΪ����Ͻ�MHΪ��������ԭ�ӵĴ���Ͻ�
�ҵ缫��Ni��OH��2+OH--e����NiOOH+H2O
������һ�����мס������缫�����Ʒֱ��ǣ��ף� ���ң� ��
��2�����������»����ʱ�����������缫��Ӧ�ֱ�Ϊ��
�缫�� ���ҵ缫�� ��
�缫��Χ��Һ��pH�仯�ǣ�ѡ������䡱��С"����ͬ���� ���� ��
��3����ȼ������ʱ��Ϊ�������Ͳ���ȫȼ�ջ������Ⱦ������CO����֪�ڳ��³�ѹ�£�
C8 H18��1��+25��2 O2��g��=8CO2��g��+9 H2O��g������H=-5121.9kJ��mol
2CO��g��+O2��g��=2CO2��g������H=-566.0kJ��mol
H2 O��g��=H2 O��1������H=-44.0kJ��mol
д�����Ͳ���ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ�� ��
��4��Ϊ��������β���е�һ����̼��Ũ�ȣ��ɲ�ȡ��������������������һ����ȼ����ͨ�����з�Ӧ��ʵ��ת����
2 CO��g��+O2��g��= 2CO2��g��
��֪���¶�ΪT�������£�����ȼ���л�ѧ��Ӧ���ʣ�����=v���棩ʱ��������Ũ�ȴ������к㶨��ϵ��
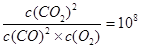
���¶�ΪT�������£���ij�������˲�ȼ����CO��CO2��Ũ�ȷֱ�Ϊ1.0��10-5mol��L-1��1.01��10-4mol��L-1��Ҫ�ڸ��¶���ʹ����β����CO��Ũ�Ƚ�Ϊ1.0��10-6mol��L-1����ȼ����Ӧ���ϲ���O2����ʹO2Ũ�ȱ����� mol��L-1��
 ��ĩ���ƾ�ϵ�д�
��ĩ���ƾ�ϵ�д� ���ɿ��ñ���ϵ�д�
���ɿ��ñ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| 17 |
| 2 |
| 17 |
| 2 |
| c(CO2)2 |
| c(CO)2��c(O2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
һ�ֻ�϶����������Էֱ��õ綯������ȼ�����߶��߽���ƶ����֡��������»����ʱ���綯���ṩ�ƶ������������͵����ģ���ɲ��������ʱ��ȼ���ṩ�ƶ�����ʹ�綯�����ڳ��״̬��Ŀǰ��ȼ��������Ϊȼ�ϣ��綯��һ��ʹ�������أ�KOH�����Һ����
�Է����ش��������⣺
��1����֪������ɲ��������ʱ�����������缫��Ӧ�ֱ�Ϊ��
�缫��M+H2O+e-��MH+OH-��MΪ����Ͻ�MHΪ��������ԭ�ӵĴ���Ͻ�
�ҵ缫��Ni��OH��2+OH--e����NiOOH+H2O
������һ�����мס������缫�����Ʒֱ��ǣ��ף� ���ң� ��
��2�����������»����ʱ�����������缫��Ӧ�ֱ�Ϊ��
�缫�� ���ҵ缫�� ��
�缫��Χ��Һ��pH�仯�ǣ�ѡ������䡱��С"����ͬ���� ���� ��
��3����ȼ������ʱ��Ϊ�������Ͳ���ȫȼ�ջ������Ⱦ������CO����֪�ڳ��³�ѹ�£�
C8 H18��1��+25��2 O2��g��=8CO2��g��+9 H2O��g������H=-5121.9kJ��mol
2CO��g��+O2��g��=2CO2��g������H=-566.0kJ��mol
H2 O��g��=H2O��1������H=-44.0kJ��mol
д�����Ͳ���ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ�� ��
��4��Ϊ��������β���е�һ����̼��Ũ�ȣ��ɲ�ȡ��������������������һ����ȼ����ͨ�����з�Ӧ��ʵ��ת����
2 CO��g��+O2��g��= 2CO2��g��
��֪���¶�ΪT�������£�����ȼ���л�ѧ��Ӧ���ʣ�����=v���棩ʱ��������Ũ�ȴ������к㶨��ϵ��
���¶�ΪT�������£���ij�������˲�ȼ����CO��CO2��Ũ�ȷֱ�Ϊ1.0��10-5mol��L-1��1.01��10-4mol��L-1��Ҫ�ڸ��¶���ʹ����β����CO��Ũ�Ƚ�Ϊ1.0��10-6mol��L-1����ȼ����Ӧ���ϲ���O2����ʹO2Ũ�ȱ����� mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ���Ĵ�ʡ�˱��и��и����ڶ�������Բ��ԣ����ۣ���ѧ���� ���ͣ������
��16�֣�һ�ֻ�϶����������Էֱ��õ綯������ȼ�����߶��߽���ƶ����֡��������»����ʱ���綯���ṩ�ƶ������������͵����ģ���ɲ��������ʱ��ȼ���ṩ�ƶ�����ʹ�綯�����ڳ��״̬��Ŀǰ��ȼ��������Ϊȼ�ϣ��綯��һ��ʹ�������أ�KOH�����Һ����
�Է����ش��������⣺
��1����֪������ɲ��������ʱ�����������缫��Ӧ�ֱ�Ϊ��
�缫��M+H2O+e-��MH+OH��MΪ����Ͻ�MHΪ��������ԭ�ӵĴ���Ͻ�
�ҵ缫��Ni��OH��2+OH--e����NiOOH+H2O
������һ�����мס������缫�����Ʒֱ��ǣ��ף� ���ң� ��
��2�����������»����ʱ�����������缫��Ӧ�ֱ�Ϊ��
�缫�� ���ҵ缫�� ��
�缫��Χ��Һ��pH�仯�ǣ�ѡ������䡱��С"����ͬ���� ���� ��
��3����ȼ������ʱ��Ϊ�������Ͳ���ȫȼ�ջ������Ⱦ������CO����֪�ڳ��³�ѹ�£�
C8 H18��1��+25��2 O2��g��=8CO2��g��+9 H2O��g������H=-5121.9kJ��mol
2CO��g��+O2��g��=2CO2��g������H=-566.0kJ��mol
H2 O��g��=H2 O��1������H=-44.0kJ��mol
д�����Ͳ���ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ�� ��
��4��Ϊ��������β���е�һ����̼��Ũ�ȣ��ɲ�ȡ��������������������һ����ȼ����ͨ�����з�Ӧ��ʵ��ת����2 CO��g��+O2��g��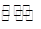 2CO2��g��
2CO2��g��
��֪���¶�ΪT�������£�����ȼ���л�ѧ��Ӧ����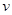 ������=v���棩ʱ��������Ũ�ȴ������к㶨��ϵ��
������=v���棩ʱ��������Ũ�ȴ������к㶨��ϵ��
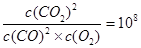
���¶�ΪT�������£���ij�������˲�ȼ����CO��CO2��Ũ�ȷֱ�Ϊ1.0��10-5mol��L-1��1.01��10-4mol��L-1��Ҫ�ڸ��¶���ʹ����β����CO��Ũ�Ƚ�Ϊ1.0��10-6mol��L-1����ȼ����Ӧ���ϲ���O2����ʹO2Ũ�ȱ����� mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011���Ĵ�ʡ�˱��д������߿���ѧ�����Ծ��������棩 ���ͣ������
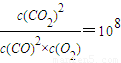
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com