
 ����Cu2O���ھ��������Ĵ����ܶ��ܵ���ѧ�о��IJ��Ϲ�ע���±�Ϊ��ȡCu2O�����ַ�����
����Cu2O���ھ��������Ĵ����ܶ��ܵ���ѧ�о��IJ��Ϲ�ע���±�Ϊ��ȡCu2O�����ַ�����| ������ | ��̿���ڸ��������»�ԭCuO | ||||
| ������ | ��ⷨ����ӦΪ2Cu+H2O
| ||||
| ������ | ���£�N2H4����ԭ���Ƶ�Cu ��OH��2 |
| 0.112L |
| 22.4L/mol |
| ||
| ||
|
| 10-14 |
| 2��10-9 |


 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д� ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.15mol/L |
| B��0.3mol/L |
| C��0.225mol/L |
| D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���Ȼ�����Һ�м��������ˮ��Al3++3NH3?H2O�TAl��OH��3��+3NH4+ |
| B���ռ���Һ�е�������ͬ���ʵ���Ũ�ȵ��Ȼ�����Һ Al3++4OH-�TAlO2-+2H2O |
| C����̼������Һ�еμ�������ϡ���CO32-+2H+�TCO2��+H2O |
| D�����������������Fe��OH��3+3H+�TFe3++3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
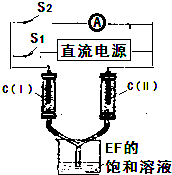 ��A��B��C��D��E��F��G����ǰ������Ԫ�أ�ԭ���������������������Ϣ�����
��A��B��C��D��E��F��G����ǰ������Ԫ�أ�ԭ���������������������Ϣ�����| Ԫ�� | Ԫ�ص������Ϣ |
| A | ���ڶ��ֺ��أ�����һ�ֺ���û������ |
| B | ��������Ų�ʽ�����ܼ��ϵĵ�������ͬ |
| C | ���һ�����ܱ�ͬ��������Ԫ�صĵ�һ�����ܶ��� |
| D | �������������ڲ������������Ԫ�� |
| E | ���ʻ��仯�����ڻ�������ʱ������ʻ�ɫ |
| F | λ�ڵ������ڢ�A�� |
| G | δ�ɶԵ��������ĸ���Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���õ�����KI��Һ���ü������ |
| B������м����ˮ����������屽 |
| C���õ���ȥ����ƾ����Ƿ�ˮ |
| D����ͭ˿�ھƾ��Ƽ��Ⱥ�����������ˮ�Ҵ��У�ͭ˿�ָ���ԭ���ĺ�ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ����� | �Լ� | ���뷽�� | |
| A | �������ӣ� | Ũ��ˮ | ���� |
| B | ��ˮ��ˮ�� | ������ | ��ȡ |
| C | �屽���壩 | NaOH��Һ | ��Һ |
| D | ��������Һ���Ȼ�����Һ�� | ����ˮ | ���� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ֻ����� | B������ֽ |
| C���л����� | D��ˮ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com