
����Ŀ�������й�������ȷ����(����)
A. H��(aq)��OH��(aq)===H2O(l)����H����a kJ�� mol��1����1 mol NaOH������������ϡ���ᷴӦ���ų�����Ϊa kJ
B. �����£���10 mL pH��a��������100 mL pH��b��Ba(OH)2��Һ��Ϻ�ǡ���кͣ���a��b��13
C. ��п�ֹ����������ӦʽΪFe��2e��===Fe2��
D. ��̼��������Һ�������գ����õ��Ĺ��������̼������
���𰸡�B
��������A. H��(aq)��OH��(aq)===H2O(l)����H����a kJ�� mol��1��NaOH��������ˮ���ȣ���1 mol NaOH������������ϡ���ᷴӦ���ų���������a kJ����A����B. �����£�pH��a��������c(H��)= 10-amol/L�� pH��b��Ba(OH)2��Һ��c(OH-)=![]() =
=![]() mol/L =10b-14mol/L����10 mL pH��a��������100 mL pH��b��Ba(OH)2��Һ��Ϻ�ǡ���кͣ�10��10-amol/L=100��10b-14mol/L����a��b��13����B��ȷ��C. ��п�ֹ�������γ�ԭ��أ��ϻ��ý���п��������������ӦʽΪZn��2e��===Zn2������C����D. ̼�����������ֽ⣬2NaHCO3
mol/L =10b-14mol/L����10 mL pH��a��������100 mL pH��b��Ba(OH)2��Һ��Ϻ�ǡ���кͣ�10��10-amol/L=100��10b-14mol/L����a��b��13����B��ȷ��C. ��п�ֹ�������γ�ԭ��أ��ϻ��ý���п��������������ӦʽΪZn��2e��===Zn2������C����D. ̼�����������ֽ⣬2NaHCO3![]() Na2CO3+H2O+CO2������̼��������Һ�������գ����õ��Ĺ��������̼���ƣ���D����ѡB��
Na2CO3+H2O+CO2������̼��������Һ�������գ����õ��Ĺ��������̼���ƣ���D����ѡB��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��19.2g SO2�ڱ�״���µ����Ϊ___________�����к���ԭ�ӵ����ʵ���Ϊ_____��
��2����һ���¶��£���mg��Է�������ΪM�Ŀ��������ܽ���VmLˮ�У�ˮ���ܶ�Ϊ1g��cm-3����ǡ���γɱ�����Һ���ܶ�Ϊpg��cm-3���������Һ�����ʵ����ʵ���Ũ����________mol��L-1��
��3��19 g ACl2�к���0.4 mol Cl-������Ȼ����Ħ��������______��A�����ԭ��������______��
��4��SO2��O2�Ļ�������У���Ԫ�ص���������Ϊ70%����SO2��O2�����ʵ���֮����________�����ֻ��������ܶ���ͬ��ͬѹ�������ܶȵ�_____����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ijǿ������Һ������������ԭ��Ӧ�����ܴ����������������
A.K����Fe2����Cl-��NO3-B.Al3+��NH4����OH-��NO3--
C.Na����H����Cl-��CO32-D.Mg2+��Ba2����SO42-��Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Լ״�ȼ�ϵ�أ����õ�ⷨ���������Ժ�����ˮ����Ҫ����Cr2O72��ʱ��ʵ����������ͼװ��ģ��÷���
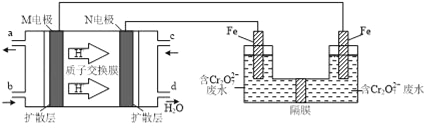
��1��N�缫�ĵ缫��ӦʽΪ______________________��
��2������ɵ�����Cr2O72ת��ΪCr3+�����ӷ�Ӧ����ʽ��______________
Cr2O72+����Fe2++�����T����Cr3++����Fe3++�� ��
��3��������ˮʱ�����Cr3+��Cr��OH��3��ʽ��ȥ����c��Cr3+��=1��105molL��1 ʱ��Cr3+������ȫ����ʱ��Һ��pH=_______�� ����֪��Ksp=6.4��1031��lg2=0.3��
��4����ȼ�ϵ�ظ���KOH��Һ���������Һ����M���ĵ缫��ӦʽΪ��____________________
��5����֪H2B����Һ�еĵ��뷽��ʽ��H2B=H++HB����HB��H++B2������������һ����ȷ������____��
A��Na2B��Һ����H2B B��NaHB��Һһ���Լ���
C��NaHB��Һһ�������� D��NaHB��Һ��ϡ���ᷴӦ�����ӷ���ʽ��HB��+H+=H2B
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ�����ӵ���������ֵ�������й�������ȷ���ǣ��� ����
��1mol���к��е�̼̼˫����Ϊ3NA
��6.2g�����ƺ�7.8g�������ƵĻ�����к��е���������Ϊ0.6NA
��3.4gNH3�к�N��H����ĿΪ0.2NA
�ܳ�����1L 0.5mol/L NH4Cl��Һ��2L 0.25mol/L NH4Cl��Һ����NH4+����Ŀ��ͬ
�ݳ�����4.6gNO2��N2O4�������������ԭ������Ϊ0.3NA
�������Ũ�Ⱦ�Ϊ1mol/L����������ᣬ���������������֮��Ϊ3��1
��1mol������1mol�����г��ȼ�գ�ʧȥ�ĵ�����Ϊ3NA
������£�16.8g Fe������ˮ������ȫ��Ӧʧȥ0.8NA�����ӣ�
A. �٢ܢݢ� B. �ڢݢ� C. �ڢܢݢߢ� D. �ݢޢߢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���ij��Һ�м�ˮϡ��ʱ��c(OH��)/c(H��)��ֵ���������ڸ���Һ���ܴ�������������������� ����
��Al3����Na����NO![]() ��AlO
��AlO![]() �� ��K����Fe2����I����SO
�� ��K����Fe2����I����SO![]()
��Ba2����I����NO![]() ��Na���� ��Na����Ca2����Mg2+��Cl��
��Na���� ��Na����Ca2����Mg2+��Cl��
A. �٢� B. �٢� C. �ڢ� D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҩҩ����˪����Ҫ�ɷ�ΪAs2O3������ˮ�������������Ƽ���Ѫ������ҵ���ú����飨As2S3)�ķ���������˪�Ĺ���������ͼ��ʾ��
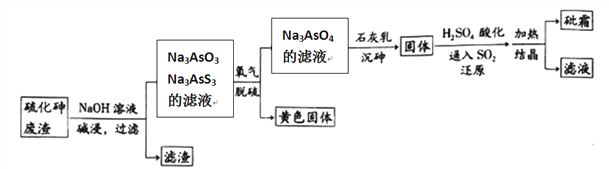
��1����������Ԫ�ػ��ϼ�Ϊ__________����������ˮ�����������������Ԫ�ؼ�̬���䣬��������Ҫ��Ӧ�����ӷ���ʽΪ________________________��
��2��������������б�������Ԫ����____________��
��3����ԭ������H3AsO4ת��ΪH3AsO3����Ӧ�Ļ�ѧ����ʽ��____________________��
��4��������������һ���¶��½���Ԫ��ת��ΪCa5(AsO4)3OH�����Ĺ��̣���Ҫ��Ӧ�У�
a.Ca(OH)2(S)![]() Ca2+(aq) +2OH-(aq) Ksp=10-7
Ca2+(aq) +2OH-(aq) Ksp=10-7
b.Ca5(AsO4)3OH (S)![]() 5Ca2+(aq)+OH-(aq)+3AsO43-(aq) Ksp=10-40
5Ca2+(aq)+OH-(aq)+3AsO43-(aq) Ksp=10-40
����ʯ�������Һ��c(OH-) =0.01mol L-1����ʱ��Һ��c(AsO43-) =________________��(��֪�� ![]() =2. 15)
=2. 15)
��5����ԭ�������Һ��H3AsO3�ֽ�ΪAs2O3���ᾧ�õ���As2O3��As2O3�ڲ�ͬ�¶ȺͲ�ͬŨ�������е��ܽ�ȶ�(S)��������ͼ��ʾ��
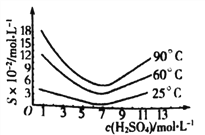
Ϊ����ߴ�As2O3�ij����ʣ����ᾧ�����̽��еIJ���������Ũ������ȴ�ᾧ�����ˣ�ϴ�ӣ��ڴ˹�����Ӧ���Ƶ�����Ϊ_________________��
��6���ڹ�ҵ�����У����һ��������Һ��ѭ��ʹ�ã���Ŀ����____________________��
��7����Ԫ�ع㷺��������Ȼ�磬�����仯���ﱻ������ũҩ�����ݼ���ɱ����ȡ�
����ij�����������As2O3��As2O5������As2O5���ȶ��Բ����ͼ1д��As2O5�ֽ�ΪAs2O3���Ȼ�ѧ����ʽ___________________________________________��
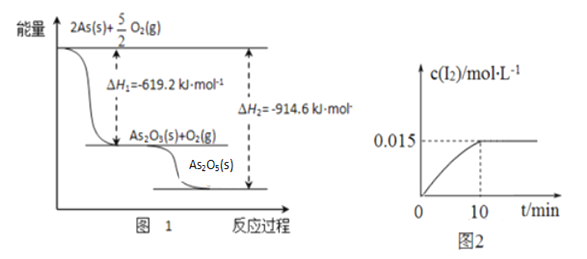
�������ƾ��������ԣ�298 Kʱ����100 mL�ձ��м���10 mL 0.1 mol/L Na3AsO4��Һ��20 mL 0.1 mol/L KI��Һ��20 mL 0.05 mol/L������Һ���������з�Ӧ��AsO43-(��ɫ)+2I-+2H+![]() AsO33-(��ɫ)+I2(dz��ɫ)+H2O �������Һ��c(I2)��ʱ��(t)�Ĺ�ϵ��ͼ2��ʾ����Һ����仯���Բ��ƣ���������������������淴Ӧ�ﵽƽ��״̬����_______������ĸ���ţ���
AsO33-(��ɫ)+I2(dz��ɫ)+H2O �������Һ��c(I2)��ʱ��(t)�Ĺ�ϵ��ͼ2��ʾ����Һ����仯���Բ��ƣ���������������������淴Ӧ�ﵽƽ��״̬����_______������ĸ���ţ���
a����Һ��ɫ���ֲ��ٱ仯 b��c(AsO33-)+c(AsO43-)���ٱ仯
c��AsO43-���������ʵ���I2���������� d�� ![]() ���ֲ��ٱ仯
���ֲ��ٱ仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2022�걱�����»��ٻ��������ڹ����ٻ��ݾ��С��˶�Ա�������ٻ������ɲ�����Ƴɣ�����ֺ��е�����ҪԪ���ǣ� ��
A.��B.̼C.��D.��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A. �ñ��Ӷ���ʢ��������ƿ�ڣ��Ϳ����ᵽ��������ζ
B. �������ſ����������ռ�������������
C. ���ȹ�����й©��Ӧ����緽����ɢȺ��
D. ��������Һ��й©ʱ��Ӧ������������й©����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com