
| A. | 平衡体系中C的体积分数为$\frac{1}{9}$ | B. | 平衡时A的浓度为2.4mol/L | ||
| C. | D的平均速率为0.32mol/L•min | D. | B的转化率为20% |
分析 设转化的A为xmol,则
2A(g)+2B(g)?C(g)+2D(g)
开始 4 4 0 0
转化 x x 0.5x x
平衡 4-x 4-x 0.5x x
经5min达到平衡,测得压强减小了10%,可知$\frac{4+4}{4-x+4-x+0.5x+x}$=$\frac{P}{P×(1-10%)}$,解得x=1.6mol,以此来解答.
解答 解:设转化的A为xmol,则
2A(g)+2B(g)?C(g)+2D(g)
开始 4 4 0 0
转化 x x 0.5x x
平衡 4-x 4-x 0.5x x
经5min达到平衡,测得压强减小了10%,可知$\frac{4+4}{4-x+4-x+0.5x+x}$=$\frac{P}{P×(1-10%)}$,解得x=1.6mol,
A.平衡体系中C的体积分数为$\frac{0.5×1.6}{8-0.5×1.6}$=$\frac{1}{9}$,故A正确;
B.平衡时A的浓度为$\frac{(4-1.6)mol}{2L}$=1.2mol/L,故B错误;
C.D的平均速率为$\frac{\frac{1.6mol}{2L}}{5min}$=0.16mol/(L•min),故C错误;
D.B的转化率为$\frac{1.6}{4}$×100%=40%,故D错误;
故选A.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、速率及转化率的计算为解答的关键,侧重分析与计算能力的考查,注意物质的量比等于压强比的应用,题目难度不大.


科目:高中化学 来源:2016-2017学年河南省新乡市高二上第一次月考化学卷(解析版) 题型:选择题
已知H2(g)、C2H4(g)和C2H5OH(l)的燃烧热分别是285.8 kJ·mol-1、1 411.0 kJ·mol-1和1 366.8 kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的ΔH为( )
A.-44.2 kJ·mol-1 B.+44.2 kJ·mol-1 C.-330 kJ·mol-1 D.+330 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高二上第一次月考化学卷(解析版) 题型:选择题
下列有关溶液中微粒的物质的量浓度关系正确的是
A.某弱酸的酸式盐NaHA溶液中一定有:c(OH-)+2c(A2-)=c(H+)+c(H2A)
B.0.2 mol·L-1 CH3COONa溶液与0.1 mol·L-1盐酸等体积混合后的酸性溶液中:c(Na+)>c(CH3COO-)>c(CH3COOH)>c(Cl-)>c(H+)
C.室温下,向100mL 0.5mol/L的Na2CO3溶液中加入0.05molCaO,溶液中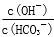 增大
增大
D.0.1 mol·L-1(NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3·H2O)+c(Fe2+)=0.3 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14g氮气含有的原子数为0.5NA | |
| B. | 4 g金属钙变成钙离子时失去的电子数为0.1NA | |
| C. | 1 mol O2分子的质量等于1 mol氧原子的质量 | |
| D. | 16 g O2分子和16g O3分子所含的氧原子数目相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
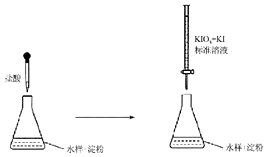 含硫化合物在生产生活中应用广泛,科学使用对人体健康及环境保持意义重大.
含硫化合物在生产生活中应用广泛,科学使用对人体健康及环境保持意义重大.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、Cl-、NO3- | B. | Cu2+、K+、SO42-、NO3- | ||
| C. | Na+、Ag+、NO3-、HCO3- | D. | Na+、NH4+、CO32-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若HnXOm为强酸,则X的氢化物溶于水一定显酸性 | |
| B. | 若X(OH)n为强碱,则Y(OH)n也一定为强碱 | |
| C. | 若X元素形成的单质是X2,则Y元素形成的单质一定是Y2 | |
| D. | 若Y的最高正价为m,则X的最高正价一定为m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com