
����Ŀ��ij��ѧС���������������������װ��(��ͼ)���Ի������Ʊ�����ϩ��
��֪��
�ܶ�/g��cm��3 | �۵�/�� | �е�/�� | �ܽ��� | |
������ | 0.96 | 25 | 161 | ������ˮ |
����ϩ | 0.81 | ��103 | 83 | ������ˮ |
��12.5 mL�����������Թ�A�У��ټ���1 mLŨ���ᣬҡ�Ⱥ�������Ƭ��������������Ӧ��ȫ�����Թ�C�ڵõ�����ϩ��Ʒ��
��1��A�����Ƭ�������� �� ����B���˵�������е���������
��2���Թ�C���ڱ�ˮԡ�е�Ŀ������
��3������ϩ��Ʒ�к��л������������������ʵȡ����뱥��ʳ��ˮ�������á��ֲ㣬����ϩ����(��ϡ����¡�)����Һ����(������)ϴ�ӡ�
a��KMnO4��Һ��b��ϡ���ᡡc��Na2CO3��Һ
��4���ٽ�����ϩ�������ɵû���ϩ��Ʒ������ʱҪ������ʯ�ң�Ŀ������
���𰸡�
��1������������
��2����ֹ����ϩ�ӷ�
��3���ϣ�c
��4����ˮ��Ӧ�����ڻ���ϩ������
��������(1)�ڻ�ѧʵ���У��������Ƭ�������Ƿ�ֹ��Һ���У�����B�Ƚϳ���������������ĽӴ�������������ǵ����ͽ����ɵ�������������������(2)��Ϊ���ﻷ��ϩ�ķе�ֻ��83 �棬�ӷ����������ڱ�ˮԡ�е�Ŀ���Ƿ�ֹ����ϩ�Ļӷ�����������ʧ��(3)����ϩ������ˮ�����ܶȱ�ˮС�����뱥��ʳ��ˮ����Һ�ֲ㣬����ϩ���ϲ㣻����ϩ�к���̼̼˫�������Ա�KMnO4��Һ������ϡH2SO4���ܳ�ȥ�����������µ��������ʣ�ֻ��Na2CO3��Һ�������뻷��ϩ��Ӧ���������������ʷ�Ӧ����ѡ��(4)������ʯ�Һ�����ˮ��Ӧ���������ټ���ʱ�Ͳ�������ˮ�ӷ�������ɲ�Ʒ�����ˡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ֵ��������ʾ���͵�������������������ı���̶���С����������ֵ�궨Ϊ100����ͼ������������ģ�ͣ����������ϵͳ����Ϊ�� �� 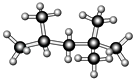
A.1��1��3��3���ļ�����
B.2��2��4����������
C.2��4��4����������
D.2��2��4����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪʵ������ȡ��������������װ��ͼ�����й��ڸ�ʵ��������в���ȷ����(����)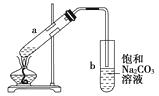
A.��a�Թ����ȼ���Ũ���ᣬȻ���ҡ���Թܱ����������Ҵ����ټӱ�����
B.�Թ�b�е������¶˹ܿڲ��ܽ���Һ���ԭ���Ƿ�ֹʵ������з�����������
C.ʵ��ʱ�����Թ�a��Ŀ���Ǽ�ʱ�����������������ӿ췴Ӧ����
D.�Թ�b�б���Na2CO3��Һ��������������������������������������Ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й�������ԭ��Ӧ��������ȷ���ǣ� ��
A.������ԭ��Ӧ��ʵ���ǵ��ӵ�ת�ƣ���ʧ��ƫ�ƣ�
B.������ԭ��Ӧ��ʵ����Ԫ�ػ��ϼ۵�����
C.������ԭ��Ӧ��ʵ��������Ԫ�صĵ�ʧ
D.��������Ԫ�ػ��ϼ����ߵķ�Ӧ�ǻ�ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���ڱ�״���£�������NO2���Թܵ��۵�ʢˮ��ˮ���У�һ��ʱ����Թ��������������Թ������________________�������Թ������ʲ���ɢ�����Թ�����Һ�����ʵ����ʵ���Ũ��Ϊ___________________��
��2��ij����������������Ʒ����5mol/L������100mLǡ����ȫ�ܽ⣬������Һ�������ձ�״����1.12L������ʹ����Fe2+ǡ��ȫ��ת��ΪFe3+��������Ӧ�����ӷ���ʽΪ_________������Ʒ��Fe��O�ĸ�����Ϊ_______________��
��3����ʢ��10mL1mol/LNH4Al(SO4)2��Һ���ձ��еμ�1mol/LNaOH��Һ���������ʵ�����NaOH��Һ����仯ʾ��ͼ������(��֪NH4++OH-=NH3��H2O)
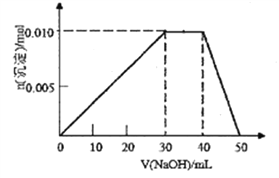
��д���μ�NaOH��Һ40��50mLʱ��Ӧ�����ӷ���ʽ��__________________��
����10mL1mol/LNH4Al(SO4)2��Һ�иļ�20mL1.15mol/LBa(OH)2��Һ����ַ�Ӧ����Һ�в������������ʵ���Ϊ_________________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ,����˵����ȷ����
A. ��״����22.4L��������ˮ�γɱ�����Һ,������Ӧ����ת�Ƶ�����ĿΪNA
B. ��״����,22.4LNO��11.2LO2��Ϻ������з�����������NA
C. ��1L0.1mol/LFeCl3��Һ�����ˮ��,�Ƶõ�Fe(OH)3������ĿΪ0.1NA
D. ������0.1 molOH����NA������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У���Ϊ�������һ���ǣ� ��
A.��� �ɱ�B.ʯ�� Һ��
C.Na2CO3��10H2O Na2CO3D.ʯ��ʯ ��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ��Ϊ��̽������CO2�ķ�Ӧ,������ͼװ�ý���ʵ�顣(��֪PdCl2�ܱ�CO��ԭ�õ���ɫ��Pd)
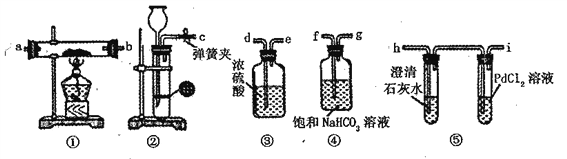
��1���뽫��ͼ��װ����������(��дװ������ĸ):c�� f�� g��_____ ��______��a ��b ��h��
��2������ϡ������CaCO3��Ӧ�Ʊ�CO2�ڼ�ϡ����ʱ,����CaCO3��ϡ����ܽӴ�,��ϡ�����ֲ�����,Ϊʹ��Ӧ��˳������,����©���м�����Լ���_________��
A.H2SO4��Һ B.CCl4 C.�� D.ϡ����
��3�����װ�������Բ�װ��ҩƷ��,��ȼ�ƾ���֮ǰӦ���еIJ����Ǵ��ɼ�,��CO2��������װ��,���۲쵽__________________ʱ�ٵ�ȼ�ƾ��ơ�
��4������Ӧ������CO2����,̽������CO2��ַ�Ӧ����������ܵ����,ijͬѧ��Ϊ���ɵ����ʽ�ΪNa2CO3����,��ʦ��Ϊ������Na2CO3�Dz����ܵ�,����˵�������ܵ�����_______��
��5�����練Ӧ�������������������,�ֱ�д���������������CO2��Ӧ�Ļ�ѧ����ʽ��
I.װ�â�PdCl2��Һ�й۵��к�ɫ����װ�â��й���ɷ�ֻ��һ��,��������м���ϡ���������ʹ����ʯ��ˮ����ǵ����壺_________________________________��
��װ�â����Ƶ�����Ϊ0.46g,��ַ�Ӧ��,��װ�â��еĹ�����뵽���������в���224mL��״��)CO2����,����Һ�л��й������_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������ع���ʱ��ӦΪ��4VB2+11O2=4B2O3+2V2O5 �� �������øõ��Ϊ��Դ���ö��Ե缫��ⱥ�ͷջ�����Һ��װ����ͼ�������·��ͨ��0.04mol����ʱ����װ������Һ�����Ϊ400mL��������˵����ȷ���ǣ� �� 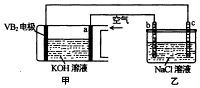
A.���·�е�����a�缫����b�缫
B.�缫��������������Ϊ4.48L
C.��װ������Һ��pHΪ13
D.VB2�缫�����ĵ缫��ӦΪ��VB2+11H2O��22e��=VB2+2B2O3+22H+
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com