
���� ��CO2��H2�ķ�ӦΪ���淴Ӧ����Ӧ�ﵽƽ��ʱ������CH3OH�����ʵ���С��1mol���ų�������������CH3OH�����ʵ��������ȣ�
�ڻ�ѧ��Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�ɴ�������һЩ������Ҳ���䣬�Դ˽��
�۸÷�Ӧ����ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ���
��� �⣺�ٿ��淴Ӧ����Ӧ���ܽ��е��ף�CO2��H2�ķ�ӦΪ���淴Ӧ����Ӧ�ﵽƽ��ʱ������CH3OH�����ʵ���С��1mol����ƽ��ʱ�ų�������С��49.0kJ��
�ʴ�Ϊ��C��
��A����ѧ��ӦΪ��̬ƽ�⣬�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�����Ӧû��ֹͣ����A����
B���ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�H2��ת���ʴﵽ���B��ȷ��
C���ﵽƽ��״̬ʱ����Ӧ����v����CO2��=3v����H2������Ӧ����v����CO2��=v����H2������Ӧ������У���C����
�ʴ�Ϊ��B��
�ۻ�ѧƽ�ⳣ��Ϊ������Ũ��ϵ�����ݵij˻��뷴Ӧ��Ũ��ϵ�����ݳ˻��ı�ֵ���÷�Ӧ����ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ���ƽ�ⳣ��K����С��
�ʴ�Ϊ����С��
���� ���⿼����淴Ӧ���漰��Ӧ�ȵļ��㡢��ѧƽ��״̬���жϡ�ƽ�ⳣ����Ӱ�����صȣ���Ŀ�ѶȲ���ע�⻯ѧƽ��״̬���������ﵽƽ��״̬ʱ���淴Ӧ������ȣ�����Ӧû��ֹͣ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ����װ������KClO3��ȡO2��װ����ͬ | |
| B�� | ������ˮ���ռ����� | |
| C�� | ����������������պ��Ũ����IJ����������Թܿڸ��� | |
| D�� | �����ü�ʯ�Ҹ��ﰱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� ���� | ��A | 0 | ||||||
| 1 | �� | ��A | ��A | ��A | ��A | ��A | ��A | |
| 2 | �� | �� | �� | �� | ||||
| 3 | �� | �� | �� | �� |
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʵ���������������۷ֱ���ȫȼ�գ����߷ų������� | |
| B�� | ��C��ʯī��?C�����ʯ����H=+1.9kJ/mol��֪�����ʯ��ʯī�ȶ� | |
| C�� | �����Ȼ�ѧ����ʽ��S��s��+O2��g��?SO2��g����H=-297.23kJ/mol������֪1 mol SO2 ��g���������ܺʹ���1 mo S��s����1 mol O2��g���������ܺ� | |
| D�� | ����ϡ��Һ�з�Ӧ��H+��aq��+OH-��aq��?H2O��l����H=-57.3kJ/mol��������0.5 mol H2SO4��Ũ�����뺬l mol NaOH��ϡ��Һ���ʱ���ų�����������57.3 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
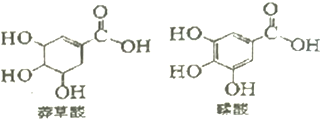
| A�� | ����ķ���ʽΪC7H8O5 | |
| B�� | �����ᶼ������ˮ��Ӧ | |
| C�� | ç������Ӻ����������������������ͬ | |
| D�� | �����ʵ�������������NaOH��Ӧ������NaOH������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.2 mol | B�� | 0.1 mol | C�� | 0.2 mol/L | D�� | 0.1 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ��� | 1 | 2 | 3 | 4 | 5 | 6 |
| ���ܼ����� |  |  |  |  |  |  |
| ÿ����Ƥ���϶����������� | ||||||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
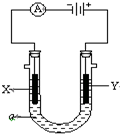 ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã�
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com