
【题目】环己酮(如图1)是一种重要的化工原料,实验室常用下列原理和装置制备(部分夹持仪器未画出)(如图2):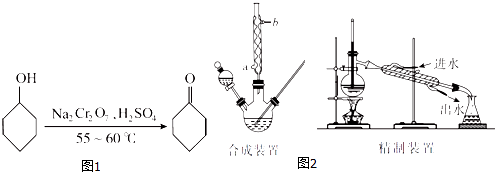
环己醇、环己酮和水的部分物理性质见下表(*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点):
物质 | 相对分子质量 | 沸点(℃) | 密度(gcm﹣3 , 20℃) | 溶解性 |
环己醇 | 100 | 161.1(97.8) | 0.9624 | 能溶于水 |
环己酮 | 98 | 155.6(95) | 0.9478 | 微溶于水 |
水 | 18 | 100.0 | 0.9982 |
(1)已知合成环己酮的反应是放热反应,反应剧烈将导致体系温度迅速上升,副反应增多.实验时,先在合成装置中加入5.2 mL(5 g)环己醇和几粒沸石,再加入酸性Na2Cr2O7溶液.酸性Na2Cr2O7溶液的加料方式为(填代号).
A.一次性加入
B.缓慢加入
C.无所谓,怎样加入都可以
(2)若酸性Na2Cr2O7溶液的体积为35 mL,则应选取(填“100 mL”或“250mL”)的三颈瓶.
(3)反应完成后,加入适量水,蒸馏,收集95~100℃的馏分(设为A),其主要成分是的混合物.
(4)合成装置中冷凝管的作用是 , 冷凝水从冷凝管的(填“a”或“b”)口进入.
(5)在馏分A中加入氯化钠固体至饱和,振荡、静置、分液,得有机层(设为B).加入氯化钠固体的作用是 .
(6)在有机层B中加入无水硫酸镁固体,除去其中的少量水分.过滤,将滤液置于精制装置中蒸馏,收集(填代号)的馏分,得到纯净的环己酮.
A.100.0~102.0℃
B.154.0~156.0℃
C.160.0~162.0℃
(7)精制装置中的错误是 . (任写一点)
(8)若最终得到环己酮的质量为3.43 g,则环己酮的产率是 .
【答案】
(1)B
(2)100mL
(3)环己酮和水
(4)冷凝回流;a
(5)降低有机物在水层得溶解度,有利于液体分层
(6)B
(7)温度计的水银球未与蒸馏烧瓶支管口平齐(或冷凝水进、出口方向颠倒)
(8)70%
【解析】解:(1)合成环己酮的反应是放热反应,酸性Na2Cr2O7溶液应缓慢加入,防止剧烈反应导致温度过高,减少副反应发生,故选:B;(2)反应液的总体积是40.2mL,液体体积一般不能超过容器容积的 ![]() 即可,所以应选择100mL三颈瓶,
即可,所以应选择100mL三颈瓶,
所以答案是:100mL;(3)95℃时得到环己酮和水的恒沸溶液,100℃的馏分是水,所以95~100℃的馏分是环己酮和水的混合物,
所以答案是:环己酮和水;(4)合成装置中的冷凝管是直立的,未收集生成物,所以其作用是冷凝回流,提高原料的利用率,采取逆流原理通入冷凝水,充分冷却,即冷凝水从冷凝管的a口进入,
所以答案是:冷凝回流;a;(5)环己酮的密度与水接近,不容易分层,用饱和食盐水可降低有机物在水层得溶解度,有利于分层,
所以答案是:降低有机物在水层得溶解度,有利于液体分层;(6)环己酮的沸点是155.6℃,所以宜收集154.0~156.0℃的馏分,
所以答案是:B;(7)装置中,温度计的水银球未与蒸馏烧瓶支管口平齐,冷凝水进、出口方向颠倒,
所以答案是:温度计的水银球未与蒸馏烧瓶支管口平齐(或冷凝水进、出口方向颠倒);(8)5g环己醇理论上得到环己酮为5g× ![]() =4.9g,所以产率是
=4.9g,所以产率是 ![]() ×100%=70%,
×100%=70%,
所以答案是:70%.


科目:高中化学 来源: 题型:
【题目】下列数据中合理的是
A.用10 mL量筒量取7.13 mL稀盐酸
B.用托盘天平称量25.20 g NaCl
C.用广范pH试纸测得某溶液的pH为2.3
D.用25 mL滴定管做中和滴定实验时,用去某浓度的碱溶液21.70 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照一定标准,根据物质与水反应的不同情况,对下列物质进行分类,如图所示,请填空:
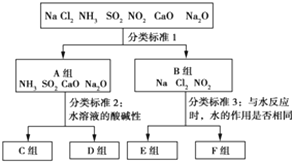
(1)上图中分类标准1(分成A、B组的依据)为_________________________________。
(2)工业上常用D组中________________(填化学式),来消除C组中物质对大气的污染,该反应的化学方程式为_____________________________________________。
(3)实验室由Al3+制备Al(OH)3时,应选择D组中________(填化学式)的水溶液,离子方程式为__________________________。
(4)F组中有两种物质,在工业上均有重要的用途,请各写出一个化学方程式表示其用途: ________________________________;________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列实验方法合理的是________。
A.用加热法除去碳酸钠固体中的碳酸氢钠
B.将碘的饱和水溶液中的碘提取出来,可用酒精进行萃取
C.实验室制取Al(OH)3:向AlCl3溶液中加入NaOH溶液至过量
D.向FeCl2溶液中滴入KSCN溶液,检验FeCl2是否已氧化变质
(2)某研究性学习小组为研究氯气是否具有漂白性,设计如图所示实验装置。试根据实验装置回答下列问题:

A、C中为干燥的有色布条,B为无色液体,D中为NaOH溶液。
① 在常温下,KMnO4固体可以与浓盐酸反应生成氯气,其反应方程式为2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,则其反应装置应选用甲、乙、丙中的________。
② B中的液体为____________,其作用为_________________________________。
③ A、C中有色布条的颜色变化分别为__________________________________,A、C的实验现象说明氯气是否具有漂白性?________(填“是”或“否”)。
④ D中NaOH溶液的作用是_______________________(用离子方程式说明)。
⑤ 将产生的氯气通入滴有酚酞的NaOH溶液中,溶液红色褪去。小组内有甲、乙两种意见:
甲:氯气溶于水后溶液显酸性,中和了NaOH,使溶液褪为无色;
乙:氯气溶于水生成漂白性物质,使溶液褪为无色。
丙同学在褪色后的溶液中逐渐加入足量的NaOH溶液,溶液一直未见红色,则 ________(填“甲”或“乙”)的意见正确。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中的一些问题常涉及到化学知识,下列叙述不正确的是()。
A.糯米中的淀粉一经发生水解反应,就酿造成酒
B.福尔马林是一种良好的杀菌剂,但不可用来消毒饮用水
C.棉花和人造丝的主要成分都是纤维素
D.室内装饰材料中缓慢释放出的甲醛、甲苯等有机物会污染空气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO与Cl2在常温常压下合成。已知NOCl是一种红褐色液体或黄色气体,其熔点64.5℃,沸点5.5℃,遇水易水解。
(1)实验室制备原料气NO和Cl2的装置如下图所示: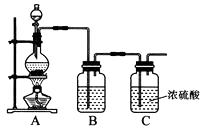
①实验室制NO时,装置A中烧瓶内发生反应的化学方程式为。
②实验室制Cl2时,装置B中盛放的试剂为 , 其作用是。
(2)将上述收集到的Cl2充入集气瓶中,按图示装置制备亚硝酰氯。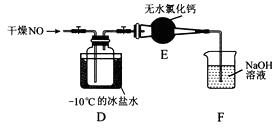
①NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为。
②装置D中的现象为。
③装置E中无水氯化钙的作用为。
④某同学认为装置F不能吸收NO,为解决这一问题,可将尾气与某种气体同时通入氢氧化钠溶液中,这种气体的化学式是。
(3)NO可用间接电化学法除去,其原理如下图所示:
①阴极的电极反应式为。
②吸收塔内发生反应的离子方程式为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列有关物质用途的叙述不正确的是()
A.明矾可用作净水剂B.NH4HCO3可用作氮肥
C.FeCl3溶液可用于腐蚀印刷电路板D.NaOH可用于治疗胃酸过多的疾病
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2和N2O4可以相互转化:2NO2(g)N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法不正确的是( ) 
A.图中的两条曲线,X表示NO2浓度随时间的变化曲线
B.前10 min内用v(N2O4)=0.02 mol/(Lmin)
C.25 min时,NO2转变为N2O4的反应速率增大,其原 因是将密闭容器的体积缩小为1L
D.该温度下反应的平衡常数 K=1.11 L/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com