
【题目】某温度下,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表,下列说法错误的是
物质 | X Y Z |
初始浓度/mol·L-1 | 0.1 0.2 0 |
平衡浓度/mol·L-1 | 0.05 0.05 0.1 |
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y![]() 2Z
2Z
C.平衡常数 K = 1600 mol-2·L2
D.增大压强和升高温度,平衡正方向移动
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.将海水中钢闸门连接电源正极可防止其被腐蚀
B.常温下,向![]() 溶液中加入少量
溶液中加入少量![]() 固体,溶液中
固体,溶液中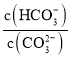 值减小
值减小
C.反应![]() 浓
浓![]() 的
的![]() ,
,![]()
D.对硫酸工业中的反应:![]() ,采用
,采用![]() 左右的高温主要是为了加快反应速率
左右的高温主要是为了加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、铁元素在细菌的作用下可发生如图所示的转化。下列说法正确的是
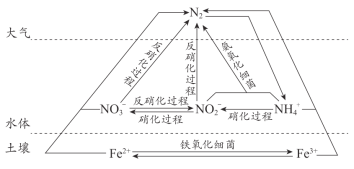
A.反硝化过程均属于氮的固定
B.硝化过程中,含氮物质均发生还原反应
C.在氨氧化细菌作用下,水体中的氮元素可转移至大气中
D.Fe3+将![]() 转化为N2的离子方程式为Fe3++2
转化为N2的离子方程式为Fe3++2![]() =Fe2++N2↑+8H+
=Fe2++N2↑+8H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成 P4O6,空气充足时生成 P4O10。
(1)已知 298K 时白磷、红磷完全燃烧的热化学方程式分别为
![]() △H1 =—2983.2kJ/mol
△H1 =—2983.2kJ/mol
![]() △H2 =—738.5kJ/mol
△H2 =—738.5kJ/mol
则该温度下白磷转化为红磷的热化学方程式为________________________.
(2)已知 298K 时白磷不完全燃烧的热化学方程式为 ![]() △H =—1638kJ/mol。在某密闭容器中加入 62g 白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O6 与P4O10 的物质的量之比为________________,反应过程中放出的热为_________________
△H =—1638kJ/mol。在某密闭容器中加入 62g 白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O6 与P4O10 的物质的量之比为________________,反应过程中放出的热为_________________
(3)已知白磷和 PCl3 的分子结构如图所示,现提供以下化学键的键能(KJ/mol):P-P:198, Cl-Cl:243, P-Cl :331 .
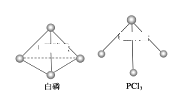
则反应 ![]() 的反应热 △H2 =__________.
的反应热 △H2 =__________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t ℃时AgCl的Ksp=4×10-10 mol2·L-2,下列说法不正确的是
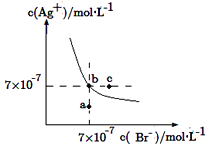
A.在t ℃时,AgBr的Ksp为4.9×10-13 mol2·L-2
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由b点到c点
C.图中a点对应的是AgBr的不饱和溶液
D.在t ℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)的平衡常数K≈816
AgBr(s)+Cl-(aq)的平衡常数K≈816
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。已知:p(Ba2+)=-lgc(Ba2+),p(SO42-)=-lg c(SO42-)。下列说法正确的是( )

A.加入BaCl2可以使溶液由c点变到a点
B.a点的Ksp(BaSO4)小于b点的Ksp(BaSO4)
C.d点表示的是该温度下BaSO4的不饱和溶液
D.该温度下,Ksp(BaSO4)=1.0×10-24
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,金属离子(Mn+)浓度的负对数值随溶液pH变化关系如图所示[已知:pM=-lgc(Mn+),且假设c(Mn+)≤10-6mol/L认为该金属离子已沉淀完全]。根据判断下列说法正确的是( )
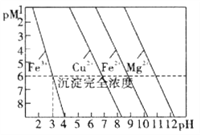
A. 常温下,Ksp[Mg(OH)2]<Ksp[Fe(OH)2]
B. 可以通过调节溶液pH的方法分步沉淀Cu2+和Fe2+
C. 除去Cu2+中少量Fe3+,可控制溶液3≤pH<4
D. pM与Ksp之间的关系式为:pM=lgKsp- nlgc(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是
A. 0.1mo1·L-1NH4HS溶液中有:c(NH4+)<c(HS-)+c(S2-)+c(H2S)
B. 25℃时,将a mo1·L-1的氨水与0.01 mo1·L-1的盐酸等体积混合后,c(NH4+)=c(Cl-),则NH3·H2O的电离常数为![]()
C. 等浓度的HCN和NaCN混合溶液中有:2c(Na+)=c(CN-)+c(HCN)
D. 等pH的HA和HB溶液,分别与一定浓度的氢氧化钠溶液完全中和,HA消耗的氢氧化钠溶液体积多,则可证明酸性HA<HB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已如:FeCl3固体遇到水蒸气容易发生潮解变质,使用下图装置并按a、e、d、b、c的顺序连接装置,利用浓盐酸制取氯气并制备一定量的FeCl3,下列说法错误的是

A. 装置a烧瓶内加入的固体可以是MnO2
B. b、c之间最好再连接一个盛有浓硫酸的洗气装置d
C. e中的溶液可以是饱和食盐水,也可以是饱和碳酸氢钠溶液
D. 反应结束后,c中的溶液能够使KI-淀粉试纸变蓝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com