

| A. | 该化合物可以发生水解反应 | B. | 该化合物能发生银镜反应 | ||
| C. | 该化合物能使酸性KMnO4溶液褪色 | D. | 该化合物共含有四种官能团 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
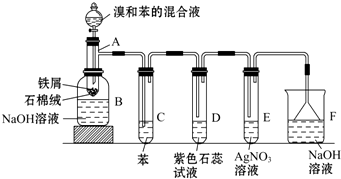
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸乙酯(乙酸):加饱和Na2CO3溶液,充分振荡静置后,分液,弃水层 | |
| B. | 苯(苯酚):加溴水,振荡,过滤除去沉淀 | |
| C. | 溴乙烷(乙醇):多次加水振荡,分液,弃水层 | |
| D. | 乙醇(水):加入新制生石灰,蒸馏,收集馏出物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3mol/L | B. | 2mol/L | C. | 4mol/L | D. | 5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
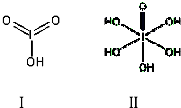
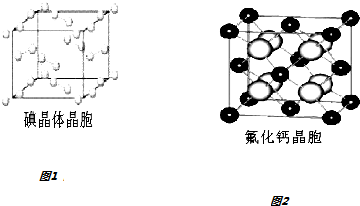
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铁及其化合物有重要用途,如聚合硫酸铁[Fe2(OH)n(SO4)3-n/2]m是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品:
铁及其化合物有重要用途,如聚合硫酸铁[Fe2(OH)n(SO4)3-n/2]m是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑦⑧ | B. | ②③⑤⑦ | C. | ①②⑦⑧ | D. | ①④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
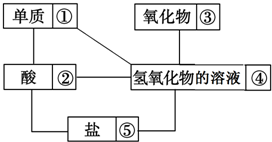
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com