
 ,G
,G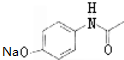 .
. .
. .
. 的合理线路(其他试剂任选,用流程图表示:写出反应物、产物及主要反应条件)
的合理线路(其他试剂任选,用流程图表示:写出反应物、产物及主要反应条件)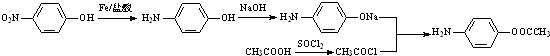 .
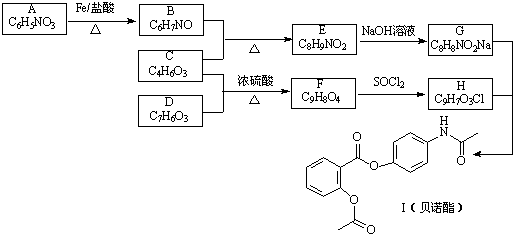
. 分析 根据贝诺酯的结构简式和G、H的分子式可知,G为 ,H为
,H为 ,再根据题各步转化的条件及有关物质的分子式可推知,E为
,再根据题各步转化的条件及有关物质的分子式可推知,E为 ,B为
,B为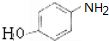 ,C为CH3COOCOCH3,A为
,C为CH3COOCOCH3,A为 ,F为
,F为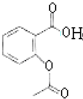 ,D为
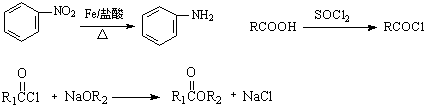
,D为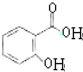 ,A发生还原反应得B,B与C发生取代反应生成E,E与氢氧化钠反应生成G,C与D发生取代反应生成F,F发生信息中的取代反应生成H,G和H发生信息中的取代反应生成I,从A和乙酸出发合成
,A发生还原反应得B,B与C发生取代反应生成E,E与氢氧化钠反应生成G,C与D发生取代反应生成F,F发生信息中的取代反应生成H,G和H发生信息中的取代反应生成I,从A和乙酸出发合成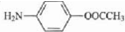 ,可以先将对硝基苯酚还原成对氨基苯酚,在碱性条件下变成对氨基苯酚钠,将醋酸与SOCl2反应生成ClCH2COOH,ClCH2COOH与对氨基苯酚钠发生信息中的反应即可得产品,据此答题.
,可以先将对硝基苯酚还原成对氨基苯酚,在碱性条件下变成对氨基苯酚钠,将醋酸与SOCl2反应生成ClCH2COOH,ClCH2COOH与对氨基苯酚钠发生信息中的反应即可得产品,据此答题.
解答 解:根据贝诺酯的结构简式和G、H的分子式可知,G为 ,H为
,H为 ,再根据题各步转化的条件及有关物质的分子式可推知,E为
,再根据题各步转化的条件及有关物质的分子式可推知,E为 ,B为
,B为 ,C为CH3COOCOCH3,A为
,C为CH3COOCOCH3,A为 ,F为
,F为 ,D为
,D为 ,A发生还原反应得B,B与C发生取代反应生成E,E与氢氧化钠反应生成G,C与D发生取代反应生成F,F发生信息中的取代反应生成H,G和H发生信息中的取代反应生成I,
,A发生还原反应得B,B与C发生取代反应生成E,E与氢氧化钠反应生成G,C与D发生取代反应生成F,F发生信息中的取代反应生成H,G和H发生信息中的取代反应生成I,
(1)根据Ⅰ(贝诺酯)的结构简式可知,I的分子式为C17H15NO5,
故答案为:C17H15NO5;
(2)A→B的反应类型是还原反应,G+H→Ⅰ的反应类型是取代反应,
故答案为:还原反应;取代反应;
(3)根据上面的分析可知,A为 ,G为
,G为 ,
,
故答案为: ;
; ;
;
(4)Ⅰ(贝诺酯)在氢氧化钠热溶液中完全水解的化学反应方程式为 ,
,
故答案为: ;
;
(5)F为 ,根据下列条件a.和F具有相同官能团,即有酯基和羧基;b.苯环上的一氯取代产物只有两种结构,说明苯环上有两个处于对位的不同基团;c.能发生银镜反应,说明有醛基,则满足条件的F的同分异构体的结构简式为
,根据下列条件a.和F具有相同官能团,即有酯基和羧基;b.苯环上的一氯取代产物只有两种结构,说明苯环上有两个处于对位的不同基团;c.能发生银镜反应,说明有醛基,则满足条件的F的同分异构体的结构简式为 ,
,
故答案为: ;
;
(6)A为 ,从A和乙酸出发合成
,从A和乙酸出发合成 ,可以先将对硝基苯酚还原成对氨基苯酚,在碱性条件下变成对氨基苯酚钠,将醋酸与SOCl2反应生成ClCH2COOH,ClCH2COOH与对氨基苯酚钠发生信息中的反应即可得产品,合成线路为
,可以先将对硝基苯酚还原成对氨基苯酚,在碱性条件下变成对氨基苯酚钠,将醋酸与SOCl2反应生成ClCH2COOH,ClCH2COOH与对氨基苯酚钠发生信息中的反应即可得产品,合成线路为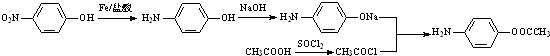 ,
,
故答案为: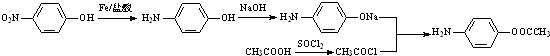 .
.
点评 本题考查有机物的推断与合成,充分根据有机物的结构进行分析解答,侧重考查学生分析推理与知识迁移应用,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
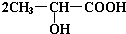 +Na2CO3→
+Na2CO3→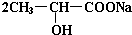 +H2O+CO2↑.
+H2O+CO2↑. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2、HClO、HCl、H2O | |
| B. | Cl、Cl-、Cl2、H2O | |
| C. | Cl2、HCl、H2O、Cl-、H+、ClO-和极少量OH- | |
| D. | Cl2、HClO、H2O、Cl-、H+、ClO-和极少量OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
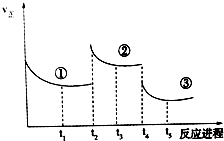 已知:2SO2(g)+O2(g)═2SO3(g)△H=-196.6kJ•mol-1,向密闭容器中加入2mol SO2和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如图所示,下列说法正确的是 ( )
已知:2SO2(g)+O2(g)═2SO3(g)△H=-196.6kJ•mol-1,向密闭容器中加入2mol SO2和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如图所示,下列说法正确的是 ( )| A. | t2~t3时间段,平衡向逆反应方向移动 | |
| B. | t4时刻改变的条件是减小压强 | |
| C. | 平衡状态①和②,SO2转化率相同 | |
| D. | 平衡状态①和②,平衡常数K值相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
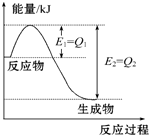 如图是一定的温度和压强下N2和H2反应生成1mol NH3过程中能量变化示意图,请写出工业合成氨的热化学方程式(△H的数值用含字母Q1、Q2的代数式表示):N2(g)+3H2(g)═2NH3(g)△H=2(Q1-Q2)kJ•mol-1.
如图是一定的温度和压强下N2和H2反应生成1mol NH3过程中能量变化示意图,请写出工业合成氨的热化学方程式(△H的数值用含字母Q1、Q2的代数式表示):N2(g)+3H2(g)═2NH3(g)△H=2(Q1-Q2)kJ•mol-1.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH、CuSO4、HCl、KNO3 | B. | HCl、KOH、NaCl、Na2SO4 | ||
| C. | Ca(OH)2、Na2CO3、NaCl、HCl | D. | NaNO3、MgCl2、KCl、Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol Na2O2与水反应转移电子数目为0.1NA | |
| B. | 标况下,2.24L Cl2含孤电子对的数目为0.2NA | |
| C. | pH=2的H2SO4溶液中含H+的数目为0.1NA | |
| D. | 在10g质量分数为17%的氨水中,含有H的数目为0.3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com