
 ),同时利用此装置的电能在铁上,下列说法正确的是( )
),同时利用此装置的电能在铁上,下列说法正确的是( )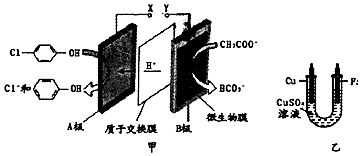
| A. | 当外电路中有0.2mol e-转移时,A极区增加的H+的个数为0.2 NA | |
| B. | A极的电极反应式为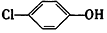 +2e-+H+=Cl-+ +2e-+H+=Cl-+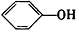 | |
| C. | 乙装置中铁电极应与甲装置中X相连接 | |
| D. | 电镀过程中乙装置中CuSO4溶液浓度逐渐减小 |
分析 原电池中阳离子移向正极,根据原电池中氢离子的移动方向可知A为正极,正极有氢离子参与反应,电极反应式为H++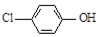 +2e-=Cl-+
+2e-=Cl-+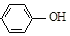 ,电流从正极经导线流向负极,据此分析.
,电流从正极经导线流向负极,据此分析.
解答 解:A、据正极有氢离子参与反应,电极反应式为H++ +2e-=Cl-+
+2e-=Cl-+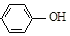 ,则当外电路中有0.2mole-转移时,通过质子交换膜的H+的个数为0.1NA,故A错误;
,则当外电路中有0.2mole-转移时,通过质子交换膜的H+的个数为0.1NA,故A错误;
B、A为正极,正极有氢离子参与反应,电极反应式为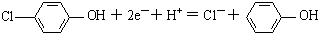 ,故B正确;
,故B正确;
C、镀件铁是阴极,与电源的负极相连,即与Y相连接,故C错误;
D、电镀过程中阳极铜失电子,阴铜离子得电子,则乙装置中CuSO4溶液浓度不变,故D错误;
故选B.
点评 本题考查了原电池原理以及电镀原理,为高频考点,侧重于学生的分析、计算能力的考查,明确原电池正负极上得失电子、电解质溶液中阴阳离子移动方向即可解答,难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 寺院内铜佛像用导线与直流电源的正极连接可以防锈 | |
| B. | 家厨内铁锅洗净后未擦干易生锈主要是发生了化学腐蚀 | |
| C. | 红葡萄酒密封贮存越久越香可能是因为缓慢生成了酯类物质 | |
| D. | 液氯泄漏时,可用肥皂水浸湿的毛巾捂鼻俯卧于低处等待救援 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
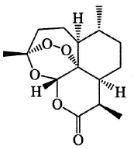 中国药学家屠呦呦因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖.青蒿素结构式如图所示,下列有关青蒿素研究的说法不正确的是( )
中国药学家屠呦呦因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖.青蒿素结构式如图所示,下列有关青蒿素研究的说法不正确的是( )| A. | 提取过程中为防止破坏青蒿素结构,应避免高温,故采用低沸点溶剂乙醚进行萃取 | |
| B. | 可使用质谱仪测出这个分子的相对分子质量,也可用紫外光谱确定这个分子的环状结构 | |
| C. | 青蒿素是脂溶性的,既可看作是醚类也可看作是酯类,既有氧化性又有还原性 | |
| D. | 元素分析仪可以确定青蒿素中是否含有C、H、O等元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 漂白粉在空气中久置 | 漂白粉变为块状 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| B | 用坩埚钳夹住点燃的镁条伸入二氧化碳气体中 | 镁条剧烈燃烧 | 二氧化碳作还原剂 |
| C | 向1.0mol•L-1的NaHCO3溶液中滴加2滴甲基橙 | 溶液呈黄色 | NaHCO3溶液呈碱性 |
| D | 向浓度均为0.1mol•L-1的Al2(SO4)3、Fe2(SO4)3的溶液中逐滴加入氨水 | 先有红褐色沉淀生成,后有白色色沉淀生成 | Al(OH)3的溶度积比Fe(OH)3的大 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
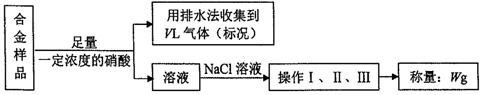
| A. | 铜、银都能与硝酸反应,收集到的VL气体全为NO | |
| B. | 操作I、II、III分别为过滤、洗涤、干燥 | |
| C. | 利用气体体积VL及样品质量mg可计算铜的质量分数 | |
| D. | 久置的银器变黑、铜绿的形成都发生了氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验步骤 | 现象 | 结论 |
| A | 向KI溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 碘易溶于CCl4,难溶于水 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 产生白色沉淀,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | FeCl3和BaCl2混合溶液中通入足量SO2 | 溶液变为浅绿色且有白色沉淀生成 | 沉淀为BaSO3 |
| D | 向AgCl悬浊液中加入NaI溶液 | 出现黄色沉淀 | Ksp (AgCl)<Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
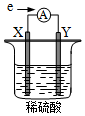 在盛有稀 H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.关于该装置,下列说法正确的是( )
在盛有稀 H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.关于该装置,下列说法正确的是( )| A. | 外电路中电流方向为:X→ →Y →Y | |
| B. | 若两电极分别为铁棒和碳棒,则 X 为碳棒,Y 为铁棒 | |
| C. | X 极上发生的是还原反应,Y 极上发生的是氧化反应 | |
| D. | 若两电极都是金属单质,则它们的活动性顺序为 X>Y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com