
��9�֣�1 Lij�����Һ�����ܺ��е��������±���
|
���ܴ������е������� |
H+ NH4+ Al3+ K+ |
|
���ܴ������е������� |
Cl- Br- I‑ ClO‑ AlO2- |
(1)������Һ����μ���NaOH��Һ���ʵ����ȣ�������������������ʵ����� �����NaOH��Һ�������
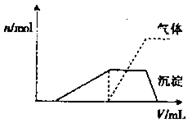
�����NaOH��Һ�������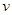 ���Ĺ�ϵ����ͼ��ʾ�������Һ��ȷ�����е�������_______________��
���Ĺ�ϵ����ͼ��ʾ�������Һ��ȷ�����е�������_______________��
����ȷ���Ƿ��е���������__________��Ҫȷ������ڿɲ�������ʵ����________��
��2������⣬����Һ�к��д�����Cl�� ��Br����I��������1 L�û����Һ��ͨ�롪������Cl2����Һ��Cl����Br����I�������ʵ�����ͨ��Cl2�������״�����Ĺ�ϵ���±���ʾ��������ش��������⣺
|
Cl2���������״���� |
2.8L |
5.6 L |
11.2 L |
|
|
1.25mol |
1.5 mol |
2 mol |
|
|
1.5 mol |
1.4 mol |
0.9 mol |
|
|
|
0 |
0 |
�ٵ�ͨ��Cl2�����Ϊ2.8 Lʱ����Һ�з�����Ӧ�����ӷ���ʽΪ___ ��
��ԭ��Һ��Cl����Br����I�������ʵ���Ũ��֮��Ϊ_____________��
 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��9�֣�1 Lij�����Һ�����ܺ��е��������±���
| ���ܴ������е������� | H+ NH4+ Al3+ K+ |
| ���ܴ������е������� | Cl- Br- I‑ ClO‑ AlO2- |
(1)������Һ����μ���NaOH��Һ���ʵ����ȣ�������������������ʵ����������NaOH��Һ�������
���Ĺ�ϵ����ͼ��ʾ�������Һ��ȷ�����е�������_______________��
����ȷ���Ƿ��е���������__________��Ҫȷ������ڿɲ�������ʵ����________��
��2������⣬����Һ�к��д�����Cl�� ��Br����I��������1 L�û����Һ��ͨ�롪������Cl2����Һ��Cl����Br����I�������ʵ�����ͨ��Cl2�������״�����Ĺ�ϵ���±���ʾ��������ش��������⣺
| Cl2���������״���� | 2.8L | 5.6 L | 11.2 L |
|
| 1.25mol | 1.5 mol | 2 mol |
|
| 1.5 mol | 1.4 mol | 0.9 mol |
|
|
| 0 | 0 |
�ٵ�ͨ��Cl2�����Ϊ2.8 Lʱ����Һ�з�����Ӧ�����ӷ���ʽΪ___ ��
��ԭ��Һ��Cl����Br����I�������ʵ���Ũ��֮��Ϊ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
1 Lij�����Һ�����ܺ��е��������±���
| ���ܴ������е������� | H+ NH4+ Al3+ K+ |
| ���ܴ������е������� | Cl- Br- I‑ ClO‑ AlO2- |
��1��������Һ����μ���NaOH��Һ���ʵ����ȣ�������������������ʵ������������NaOH��Һ�������
���Ĺ�ϵ����ͼ��ʾ��
�����Һ��ȷ�����е�������____________________��
����ȷ���Ƿ��е���������____________________��
Ҫȷ������ڿɲ�������ʵ����____________________��
�϶������ڵ���������____________________��
��2������⣬����Һ�к��д�����Cl�� ��Br����I��������1 L�û����Һ��ͨ��һ������Cl2����Һ��Cl����Br����I�������ʵ�����ͨ��Cl2�������״�����Ĺ�ϵ���±���ʾ��������ش��������⣺
| Cl2���������״���� | 2��8L | 5��6 L | 11��2 L |
|
| 1��25mol | 1��5 mol | 2 mol |
|
| 1��5 mol | 1��4 mol | 0��9 mol |
|
|
| 0 | 0 |
�ٵ�ͨ��Cl2�����Ϊ2��8Lʱ����Һ�з�����Ӧ�����ӷ���ʽΪ____________________��
��ԭ��Һ��Cl����Br����I�������ʵ���Ũ��֮��Ϊ______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�츣��ʡ�ϰ�һ�и�����ѧ�����п��Ի�ѧ�Ծ� ���ͣ������
��9�֣�1 Lij�����Һ�����ܺ��е� �������±���
�������±���
| ���ܴ������е������� | H+ NH4+ Al3+ K+ |
| ���ܴ������е������� | Cl- Br- I? ClO? AlO2- |
 �����NaOH��Һ�������
�����NaOH��Һ������� ���Ĺ�ϵ����ͼ��ʾ�������Һ��ȷ�����е�������_______________��
���Ĺ�ϵ����ͼ��ʾ�������Һ��ȷ�����е�������_______________��
 ��ϵ���±���ʾ��������ش��������⣺
��ϵ���±���ʾ��������ش��������⣺| Cl2���������״���� | 2.8L | 5.6 L | 11.2 L |
 ��Cl���� ��Cl���� | 1.25mol | 1.5 mol | 2 mol |
 ��Br���� ��Br���� | 1.5 mol | 1.4 mol | 0.9 mol |
 ��I���� ��I���� |  mol mol | 0 | 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ���㽭ʡ����Ϫ���и�����ѧ������������ѧ�Ծ� ���ͣ������
��12�֣�1 Lij�����Һ�����ܺ��е��������±���
|
���ܴ������е������� |
H+ NH4+ Al3+ K+ |
|
���ܴ������е������� |
Cl- Br- I‑ ClO‑ AlO2- |
(1)������Һ����μ���NaOH��Һ���ʵ����ȣ�������������������ʵ������������NaOH��Һ����������Ĺ�ϵ����ͼ��ʾ��

�����Һ��ȷ�����е������� ��
����ȷ���Ƿ��е��������� ��
Ҫȷ������ڿɲ�������ʵ���� ��
�϶������ڵ��������� ��
��2������⣬����Һ�к��д�����Cl�� ��Br����I��������1 L�û����Һ��ͨ��һ������Cl2����Һ��Cl����Br����I�������ʵ�����ͨ��Cl2�������״�����Ĺ�ϵ���±���ʾ��������ش��������⣺
|
Cl2���������״���� |
2��8L |
5��6 L |
11��2 L |
|
��Cl���� |
1��25mol |
1��5 mol |
2 mol |
|
��Br���� |
1��5 mol |
1��4 mol |
0��9 mol |
|
��I���� |
mol |
0 |
0 |
�ٵ�ͨ��Cl2�����Ϊ2��8 Lʱ����Һ�з�����Ӧ�����ӷ���ʽΪ ��
��ԭ��Һ��Cl����Br����I�������ʵ���Ũ��֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ���㽭ʡ�����и�����ѧ��������У������ѧ�Ծ� ���ͣ������
��12�֣�1 Lij�����Һ�����ܺ��е��������±���
|
���ܴ������е������� |
H+ NH4+ Al3+ K+ |
|
���ܴ������е������� |
Cl- Br- I‑ ClO‑ AlO2- |
(1)������Һ����μ���NaOH��Һ���ʵ����ȣ����� ��������������ʵ����� �������NaOH��Һ�������
�������NaOH��Һ������� ���Ĺ�ϵ����ͼ��ʾ��
���Ĺ�ϵ����ͼ��ʾ��

�����Һ��ȷ�����е�������____ ___ __��
����ȷ���Ƿ��е���������_______ ___��
Ҫȷ������ڿɲ�������ʵ����______ _��
�϶������ڵ���������________ ___��
��2������⣬����Һ�к��д�����Cl�� ��Br����I��������1 L�û����Һ��ͨ��һ������Cl2����Һ��Cl����Br����I�������ʵ�����ͨ��Cl2�������״�����Ĺ�ϵ���±���ʾ��������ش��������⣺
|
Cl2���������״���� |
2��8L |
5��6 L |
11��2 L |
|
|
1��25mol |
1��5 mol |
2 mol |
|
|
1��5 mol |
1��4 mol |
0��9 mol |
|
|
|
0 |
0 |
�ٵ�ͨ��Cl2�����Ϊ2��8 Lʱ����Һ�з�����Ӧ�����ӷ���ʽΪ__ _��
��ԭ��Һ��Cl����Br����I�������ʵ���Ũ��֮��Ϊ_____ ________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com