
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
| A. | Na2SO3溶液中c(H+)<c (OH-) | |
| B. | Na2SO3溶液中c(Na+))>c (SO32-)>c (HSO3-)>c (OH-)>c(H+) | |
| C. | 当吸收液呈中性时,c(Na+))>c (SO32-)>c (HSO3-)>c (OH-)=c(H+) | |
| D. | 当吸收液呈中性时,c(Na+)>c (HSO3-)+c (SO32-) |
分析 A.表格数据知,亚硫酸钠溶液呈碱性;
B.亚硫酸钠溶液呈碱性,且盐类水解是微弱的,根据电荷守恒判断离子浓度大小;
C.当吸收液呈中性时,溶液中的溶质是亚硫酸钠和硫酸钠,但亚硫酸氢钠的浓度大于亚硫酸钠;
D.溶液中存在电荷守恒.
解答 解:用Na2SO3溶液吸收SO2时,随着吸收的增多,溶液由碱性逐渐变为酸性,
A.由表中信息可知Na2SO3溶液为碱性溶液,c(H+)<c (OH-),故A正确;
B.Na2SO3溶液中SO32-的水解存在二级水解,亚硫酸氢根离子水解程度较小,且水电离也产生氢氧根离子,所以c(HSO3-)应小于c (OH-),故B错误;
C.由表中数据,当c (SO32-)=c (HSO3-)时,pH=7.2,故当吸收液呈中性时,可推出c (SO32-)<c (HSO3-),故C错误;
D.因c(H+)=c (OH-),根据电荷守恒,c(Na+)=c (HSO3-)+2c (SO32-)成立,c(Na+)>c (HSO3-)+c (SO32-),故D正确;
故选AD.
点评 本题考查离子浓度大小的比较,根据物料守恒及电荷守恒来分析解答,题目难度中等.


科目:高中化学 来源: 题型:推断题
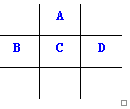 有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1mol E单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1mol E单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题: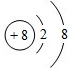 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
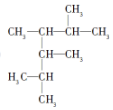 2,3,4,5-四甲基己烷
2,3,4,5-四甲基己烷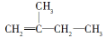 2-甲基-1-丁烯
2-甲基-1-丁烯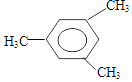 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
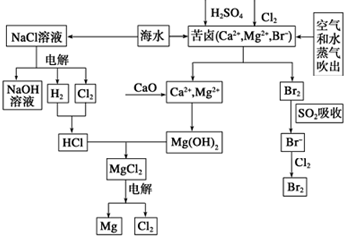 海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原料.下图是海水综合利用的部分流程图,据图回答问题:
海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原料.下图是海水综合利用的部分流程图,据图回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合物电离时,生成的阳离子有氢离子的是酸 | |
| B. | 化合物电离时,生成的阴离子有氢氧根离子的是碱 | |
| C. | 化合物电离时,生成金属阳离子和酸根离子的是盐 | |
| D. | NH4Cl通电时能电离出NH4+和Cl-,所以NH4Cl是盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | H2CO3 | H2SO3 |
| 电离平衡常数K | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应KClO3+6HCl═3C12↑+KCl+3H2O,每生成1.5molC12转移电子数为2.5NA | |
| B. | 标准状况下,11.2LNO与11.2LO2混合后所含分子数为0.75NA | |
| C. | 1L0.1mol/LNH4Cl溶液中NH4+的数目为0.1NA | |
| D. | 40gSiC中含有Si-C键的数目为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com