
现有室温下浓度均为1×10-3mol/L的几种溶液:
①盐酸、②硫酸、③醋酸、④氯化铵、⑤氨水、⑥NaOH,回答下列问题:
(1)将③、⑥混合后,若溶液呈中性,则消耗两溶液的体积为③ ________ ⑥(填“>”、“<”或“=”)溶液中的离子浓度由大到小的顺序为
(2)将等体积的①、⑤混合,则溶液的pH ________ 7(填“>”、“<”或“=”)
用离子方程式说明其原因 _______________________
(3)向相同体积的①、②、③溶液中分别加入相同的且足量的锌粒,反应的初始速率由快到慢的为________ (填写序号)
最终产生H2总量的关系为___________(填写序号)
(4)向相同体积的①、③溶液中分别加入相同浓度、相同体积的CH3COONa溶液,充分混合后,混合液的pH 大小关系为① _________ ③(填“>”、“<”或“=”)
(5)将等体积的⑤、⑥溶液加热至同温度后,溶液的pH ⑤ _____ ⑥(填“>”、“<”或“=”)
(1)> ;c(Na+)=c (CH3COO-)> c(H+)=c c(OH-).
(2)< NH4++H2O NH3·H2O+H+ (3)②>①>③; ②>①=③ ;(4)< (5)<
NH3·H2O+H+ (3)②>①>③; ②>①=③ ;(4)< (5)<
【解析】
试题分析:(1)由于醋酸是弱酸,NaOH是强碱,所以将③、⑥混合后,若溶液呈中性,则消耗两溶液的体积为③>⑥; 根据电荷守恒可得:c(Na+)+c(H+)=c (CH3COO-)+c(OH-),由于溶液呈中性, c(H+)=c c(OH-),所以c(Na+)=c (CH3COO-),在盐溶液中盐电离远大于弱电解质水的电离作用,所以c(Na+)=c (CH3COO-)> c(H+)=c c(OH-);(2)由于HCl是强酸,NH3·H2O是弱碱,所以将等体积的①、⑤混合,则恰好完全发生产生盐NH4Cl,该盐是强酸弱碱盐,NH4+水解消耗水电离产生的OH-,最终使溶液中的H+的浓度大于OH-,所以溶液显酸性,pH<7,水解的离子方程式是NH4++H2O NH3·H2O+H+;(3)向相同体积的①、②、③溶液中分别加入相同的且足量的锌粒,由于溶液中c(H+)关系是:②>①>③,所以反应的初始速率由快到慢的为②>①>③,因为硫酸是二元酸,而盐酸和醋酸是一元酸,所以最终产生H2总量的关系为②>①=③ ;(4)盐酸是强酸,完全电离,而醋酸是弱酸,部分电离,在溶液中存在电离平衡,当向相同体积的①、③溶液中分别加入相同浓度、相同体积的CH3COONa溶液,充分混合后,由于会对醋酸的电离平衡起抑制作用,所以醋酸的酸性比原来还小,混合液的pH 大小关系为①<③; (5)NH3·H2O是弱碱,部分电离,而NaOH是强碱,完全电离,所以溶液中离子的浓度NaOH>NH3·H2O故溶液的pH ⑤ <⑥。
NH3·H2O+H+;(3)向相同体积的①、②、③溶液中分别加入相同的且足量的锌粒,由于溶液中c(H+)关系是:②>①>③,所以反应的初始速率由快到慢的为②>①>③,因为硫酸是二元酸,而盐酸和醋酸是一元酸,所以最终产生H2总量的关系为②>①=③ ;(4)盐酸是强酸,完全电离,而醋酸是弱酸,部分电离,在溶液中存在电离平衡,当向相同体积的①、③溶液中分别加入相同浓度、相同体积的CH3COONa溶液,充分混合后,由于会对醋酸的电离平衡起抑制作用,所以醋酸的酸性比原来还小,混合液的pH 大小关系为①<③; (5)NH3·H2O是弱碱,部分电离,而NaOH是强碱,完全电离,所以溶液中离子的浓度NaOH>NH3·H2O故溶液的pH ⑤ <⑥。
考点:考查溶液中两种浓度的大小比较、还小反应速率的计算、溶液的酸碱性的知识。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2013-2014四川省宜昌市春季期中考试高二化学试卷(解析版) 题型:选择题
如图为某化学反应的速率与时间的关系示意图。在t1时刻升高温度或增大压强,速率的变化都符合示意图的反应是
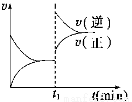
A.2SO2(g)+O2(g) 2SO3(g) ΔH<0
2SO3(g) ΔH<0
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH<0
4NO(g)+6H2O(g) ΔH<0
C.H2(g)+I2(g) 2HI(g) ΔH>0
2HI(g) ΔH>0
D.2A(g)+B(s) 2C(g) ΔH>0
2C(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:选择题
原计划实现全球卫星通讯需发射77颗卫星,这一数字与铱(Ir)元素的原子核外电子数恰好相等,因此称为“铱星计划”.已知铱的一种同位素的质量数为191,则其核内的中子数与质子数之差是
A.77 B.114 C.37 D.268
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省长春市高一下学期期末考试化学试卷(解析版) 题型:选择题
关于下图所示装置(盐桥含KCl)的叙述,正确的是
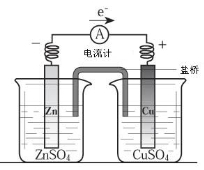
A.铜离子在铜片表面被氧化
B.铜作阳极,铜片上有气泡产生
C.电流从锌片经导线流向铜片
D.右侧烧杯中,SO42-的物质的量几乎不变,K+的数目增多
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省长春市高一下学期期末考试化学试卷(解析版) 题型:选择题
已知在一定条件下, 2SO2+O2 2SO3 反应达平衡后SO2的转化率为45.3%,加入V2O5(催化剂)后,SO2的转化率为
2SO3 反应达平衡后SO2的转化率为45.3%,加入V2O5(催化剂)后,SO2的转化率为
A. 大于45.3% B. 小于45.3% C. 等于45.3% D. 无法确定
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省白城市高二上学期期末考试化学(B卷)试卷(解析版) 题型:选择题
体积相同的甲、乙两个容器中,分别充入等物质的量的SO2和O2,在相同温度下发生反应:2SO2(g)+O2(g) 2SO3(g),并达到平衡,在此过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为
2SO3(g),并达到平衡,在此过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为
A.等于p% B.大于p% C.小于p% D.无法比较
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省白城市高二上学期期末考试化学(B卷)试卷(解析版) 题型:选择题
为探究钢铁的吸氧腐蚀原理设计了如图所示装置,下列有关说法中错误的是
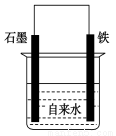 A.正极的电极方程式为:O2+2H2O+4e-===4OH-
A.正极的电极方程式为:O2+2H2O+4e-===4OH-
B.将石墨电极改成Mg电极,难以观察到铁锈生成
C.若向自来水中加入少量NaCl(s),可较快地看到铁锈
D.向铁电极附近吹入O2比向石墨电极附近吹入O2,铁锈出现得快
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省白城市高二上学期期末考试化学试卷(A卷)(解析版) 题型:选择题
在溶液中,CaCl2+CO2+H2O=CaCO3↓+2HCl在任何条件下都不能发生,原因是该反应的( )
A. △H >0 ΔS>0 B.△H<0 ΔS<0 C.△H<0 ΔS>0 D.△H >0 ΔS<0
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省白城市高一上学期期末考试化学(B卷)试卷(解析版) 题型:选择题
现有三组溶液:①汽油和氯化钠溶液;②39%的乙醇溶液;③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是 ( )
A.分液、萃取、蒸馏 B.分液、蒸馏、萃取
C.萃取、蒸馏、分液 D.蒸馏、萃取、分液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com