
【题目】氧化铁是一种重要的无机材料,化学性质稳定,催化活性高,具有良好的耐光性、耐热性和对紫外线的屏蔽性,从某种工业酸性废液(主要含Na+、Fe2+、Fe3+、Mg2+、Al3+、Cl﹣、SO42﹣)中回收氧化铁流程如图:

已知:常温下Ksp[Mg(OH)2]=1.2×10﹣11; Ksp[Fe(OH)2]=2.2×10﹣16;Ksp[Fe(OH)3]=3.5×10﹣38;Ksp[Al(OH)3]=1.0×10﹣33。
(1)写出在该酸性废液中通入空气时发生的离子反应方程式_____。
(2)常温下,根据已知条件在pH=5的溶液中,理论上下列微粒在该溶液中可存在的最大浓度c(Fe3+)=_____。
(3)有人用氨水调节溶液pH,在pH=5时将Fe(OH)3沉淀出来,此时可能混有的杂质是_____(填化学式,下同),用_____试剂可将其除去。
【答案】4Fe2++O2+4H+=4Fe3++2H2O; 3.5×10-11mol·L-1 Al(OH)3 NaOH
【解析】
(1)酸性废液中含有Fe2+,Fe2+能被氧气氧化进行分析;
(2)根据溶度积进行计算;
(3)根据溶度积进行分析和计算。
(1)酸性废液中含有Fe2+,Fe2+能被O2氧化,因此离子方程式为4Fe2++O2+4H+=4Fe3++2H2O;
答案:4Fe2++O2+4H+=4Fe3++2H2O;
(2)溶液的pH=5,则溶液c(OH-)=![]() mol·L-1=10-9mol·L-1,根据Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-),代入数值,得到c(Fe3+)=
mol·L-1=10-9mol·L-1,根据Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-),代入数值,得到c(Fe3+)=![]() mol·L-1=3.5×10-11mol·L-1;
mol·L-1=3.5×10-11mol·L-1;
答案:3.5×10-11mol·L-1;
(3) 溶液的pH=5,则溶液c(OH-)=![]() mol·L-1=10-9mol·L-1,Ksp[Mg(OH)2]=c(Mg2+)×c2(OH-)代入数值,c(Mg2+)=1.2×107mol·L-1,说明Mg2+没有出现沉淀,Ksp[Al(OH)3]=c(Al3+)×c3(OH-),代入数值,得出c(Al3+)=10-6mol·L-1<1×10-5mol·L-1,说明Al3+几乎完全沉淀,混有的杂质为Al(OH)3,Al(OH)3属于两性氢氧化物,Fe(OH)3为碱性氢氧化物,因此需要加入NaOH溶液溶解Al(OH)3;
mol·L-1=10-9mol·L-1,Ksp[Mg(OH)2]=c(Mg2+)×c2(OH-)代入数值,c(Mg2+)=1.2×107mol·L-1,说明Mg2+没有出现沉淀,Ksp[Al(OH)3]=c(Al3+)×c3(OH-),代入数值,得出c(Al3+)=10-6mol·L-1<1×10-5mol·L-1,说明Al3+几乎完全沉淀,混有的杂质为Al(OH)3,Al(OH)3属于两性氢氧化物,Fe(OH)3为碱性氢氧化物,因此需要加入NaOH溶液溶解Al(OH)3;
答案:Al(OH)3;NaOH。


科目:高中化学 来源: 题型:
【题目】常温下,FeS的Ksp=6.25×10-18(设饱和溶液的密度为1g/mL)。若已知H2S饱和溶液在常温下,c(H+)与c(S2-)之间存在以下关系:c2(H+)·c(S2-)=1.0×10-22,在该温度下,将适量FeS投入H2S饱和溶液中,欲使溶液中c(Fe 2+)达到1mol/L,应调节溶液的pH为___________
(已知:lg2 = 0.3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知每个手性碳原子具有一对旋光异构体,也称对映异构体。据此化合物![]() 分子中有a种化学环境不同的氢原子,如果用氯取代分子中的氢原子,生成的一氯代物可能有b种,则a、b分别是
分子中有a种化学环境不同的氢原子,如果用氯取代分子中的氢原子,生成的一氯代物可能有b种,则a、b分别是
A.3、6B.4、8C.4、6D.4、12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾(K2Cr2O7).工艺流程如图1及相关物质溶解度曲线如图2:
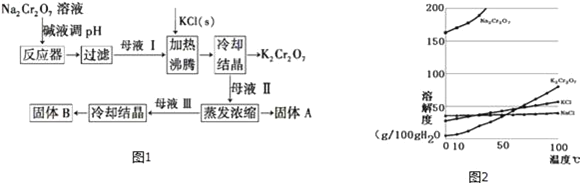
(1)由Na2Cr2O7生产K2Cr2O7的化学方程式为:____________.通过冷却结晶析出大量K2Cr2O7的原因是____________.
(2)向Na2Cr2O7母液中加碱液调pH的目的是____________.
(3)固体A主要为____________(填化学式),固体B主要为____________(填化学式).
(4)为检验得到的重铬酸钾晶体中含有少量的氯化钠杂质,实验方法是:____________;进一步提纯产品的方法是____________
(5)将SO2通入用硫酸酸化的重铬酸钾溶液中,可制得硫酸铬钾KCr(SO4)2,反应的化学方程式为____________;如果溶液的酸碱性控制不当,可能会有Cr(OH)SO4杂质生成.现从得到的硫酸铬钾产品中取出3.160g样品加入足量盐酸和BaCl2溶液后,得到白色沉淀5.126g.若产品中杂质只有Cr(OH)SO4,则该产品中KCr(SO4)2的质量分数为____________(用百分数表示,保留1位小数).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
温度/℃ | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
pH | 8.3 | 8.4 | 8.5 | 8.8 |
(1)甲同学认为,该溶液的pH升高的原因是HCO3-水解程度增大,故碱性增强,该反应的离子方程式为______________________。乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度________NaHCO3(填“大于”或“小于”)。丙同学认为甲、乙的判断都不充分,丙认为:
(2)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则________(填“甲”或“乙”)判断正确。试剂X是________(填选项)。
A.Ba(OH)2溶液 | B.BaCl2溶液 |
C.NaOH溶液 | D.澄清的石灰水 |
(3)查阅资料发现NaHCO3的分解温度为150℃,丙断言________(填“甲”或“乙”)判断是错误的,理由是________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.1 mol过氧化钠中阴离子所带的负电荷数为NA
B.14 g乙烯和丙烯的混合物中含有的碳原子的数目为NA
C.28 g C16O与28 g C18O中含有的质子数均为14 NA
D.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属腐蚀与防护的说法正确的是( )

A. 图1中,插入海水中的铁棒,越靠近底端,腐蚀越严重
B. 镀层破损后,镀锌铁比镀锡铁更耐用
C. 纯银器表面在空气中因电化学腐蚀渐渐变暗
D. 图2中,金属棒X若为Cu,可使埋在地下的钢管免受腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有着广泛用途。一种合成阿魏酸的反应可表示为
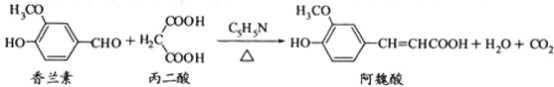
下列说法正确的是
A.可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成
B.香兰素、阿魏酸均可与Na2CO3、NaOH溶液反应
C.通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应
D.1mol香兰素最多可以与4molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 mol H—H键的键能是436kJ,1 mol I—I键的键能是151kJ,1 mol H—I键的键能是299kJ,则对反应H2(g)+I2(g)![]() 2HI(g)的说法,不正确的是 ( )
2HI(g)的说法,不正确的是 ( )
A.放热反应B.吸热反应C.化合反应D.可逆反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com