
�����DZ�ʾ��Ӧ2A��B��3C��4D�ķ�Ӧ�������ݡ����շ�Ӧ����˳������ӦΪ( )
�٦�(A)��0.5mol?L-1?S-1 �ڦ�(B)��0.3mol?L-1?S-1
�ۦ�(C)��0.8mol?L-1?S-1 �ܦ�(D)��1mol?L-1?S-1
A����>��>��>�� B����>��>�٣��� C����>��>��>�� D����>��>�٣���
 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
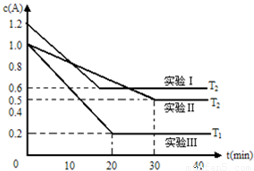
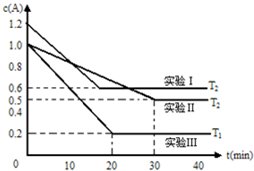 ������ϵ���������·�Ӧ2A��g��?B��g��+xC��������H����ʼʱB��C���ʵ���Ũ��Ϊ0��A�����ʵ���Ũ����ʱ��仯��ͼ��ij����С��һ����������ͼ��ʾ������ʵ�飬����T1��T2��ʾ��ͬ�ķ�Ӧ�¶ȣ���
������ϵ���������·�Ӧ2A��g��?B��g��+xC��������H����ʼʱB��C���ʵ���Ũ��Ϊ0��A�����ʵ���Ũ����ʱ��仯��ͼ��ij����С��һ����������ͼ��ʾ������ʵ�飬����T1��T2��ʾ��ͬ�ķ�Ӧ�¶ȣ���| c(B)?c(C) |
| c2(A) |
| c(B)?c(C) |
| c2(A) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ģ���� ���ͣ������
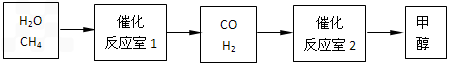
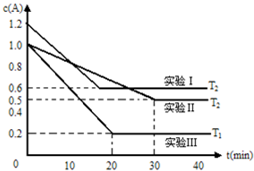
 CH3OH (g)��CO��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ����
CH3OH (g)��CO��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ���� 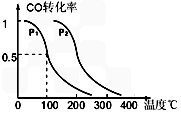
 CO(g) + 2H2(g)��Ӧ��ƽ�ⳣ��Ϊ________���ú�a��V�Ĵ���ʽ��ʾ��
CO(g) + 2H2(g)��Ӧ��ƽ�ⳣ��Ϊ________���ú�a��V�Ĵ���ʽ��ʾ��  SO3��g��+NO��g��������Ӧ������Ӧ������ʱ��仯��������ͼ��ʾ����ͼ��֪����˵����ȷ����__________������ĸ����
SO3��g��+NO��g��������Ӧ������Ӧ������ʱ��仯��������ͼ��ʾ����ͼ��֪����˵����ȷ����__________������ĸ���� 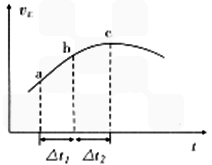
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ���Ĵ�ʡ�ɶ����и߶����ϣ���ĩ��ѧ�Ծ��������棩 ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com