
下列离子方程式正确的是( )
A.碳酸钙中加入盐酸:CO +2H+===CO2↑+H2O
+2H+===CO2↑+H2O
B.澄清石灰水与盐酸反应:Ca(OH)2+2H+===Ca2++2H2O
C.三氯化铁溶液与铁反应:2Fe3++Fe===3Fe2+
D.氯化亚铁溶液中通入少量氯气:Fe2++Cl2===Fe3++2Cl-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
A、B、C、D、E是五种短周期的主族元素,它们的原子序数依次增大,A、D都能与C按原子个数比为1:1或2:1形成化合物,A、B组成的气态化合物的水溶液呈碱性,E与C的最外层电子数相同。
(1)画出D的原子结构示意图 ,
(2)E元素在周期表中的位置是 。
(3)D与C按原子个数比为1:1的化合物的用途为 。
(4)B、C所形成氢化物的稳定性由强到弱的顺序是 (填具体的化学式)
(5)F是一种历史悠久、应用广泛的金属元素。若将F金属投入到盐酸溶液中,生成了浅绿色溶液M。写出M的酸性溶液和A与C形成的一种化合物X(化合物X中A、C原子个数比为1:1)反应的离子方程式: 。
(6)有人设想寻求合适的催化剂和电极材料,以A2、B2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极电极反应式: ;放电时溶液中的H+移向 (填“正”或“负”)极。
(7)E(s) + O2(g) == EO2(g) △H1 ; E(g) + O2(g) === EO2(g) △H2 ;则△H1 △H2(填“>”或“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.含有离子键和共价键的化合物一定是离子化合物
B.元素原子的最外层电子数等于该元素的最高正化合价
C.目前人们已发现的元素种类数目与原子种类数目相同
D.多电子原子中,在离核较近的区域内运动的电子能量较高
查看答案和解析>>
科目:高中化学 来源: 题型:
五种短周期元素的某些性质如表所示(其中Z、M、W为同周期元素)。
| 元素代号 | Y | X | W | M | Z |
| 原子半径(×10-12 m) | 64 | 73 | 78 | 96 | 113 |
| 主要化合价 | -1 | +5、-3 | +7、-1 | +4、-4 | +3 |
下列说法不正确的是( )
A.由M与W形成的化合物是含有极性键的极性分子
B. X与M之间形成的化合物,其晶体是原子晶体
C.由M元素形成的晶体,是太阳能光伏发电的主要材料,工业上制取M单质,可通过置换反应原理来生产
D.Y与Z元素形成的[ZY6]3-,离子中存在配位键,该离子构型呈正八面体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是( )
A.将一束强光通过淀粉溶液,也能产生丁达尔效应
B.在含有1 mol Fe(OH)3的胶体中,约含6.02×1023个Fe(OH)3胶粒
C.一支钢笔使用两种不同型号的蓝黑墨水,易出现堵塞
D.“雨后彩虹”、“海市蜃楼”既是一种自然现象又是光学现象,也与胶体的性质有关
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出离子反应方程式H++OH-===H2O所对应的两个不同类型化学方程式。
①________________________________________________________________________;
②________________________________________________________________________。
(2)在下列反应中:
A.2F2+2H2O===4HF+O2
B.2Na+2H2O===2NaOH+H2↑
C.CaO+H2O===Ca(OH)2
D.2H2O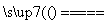 2H2↑+O2↑
2H2↑+O2↑
水只做氧化剂的是________,水只做还原剂的是________,水既做氧化剂又做还原剂的是________,水既不做氧化剂又不做还原剂的是________。请用单线桥法表示B反应的电子转移方向和数目________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于Na2CO3和NaHCO3的下列说法中正确的是( )
A.NaHCO3不如Na2CO3与盐酸反应剧烈
B.NaHCO3比Na2CO3稳定
C.石灰水能和NaHCO3反应,不与Na2CO3反应
D.等物质的量的Na2CO3和NaHCO3与足量盐酸反应,消耗HCl的物质的量之比为2∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com