
【题目】从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平.B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78.回答下列问题:
(1)A的电子式 ______________ ,A的结构简式 _______________ .
(2)与A相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式 ______________________,反应类型_______________。
(3)在碘水中加入B振荡静置后的现象_________________________
(4)B与浓H2SO4与浓HNO3在50-60℃反应的化学反应方程式 ________________________,反应类型______________________。
(5)等质量的A、B完全燃烧时消耗O2的物质的量______(填“A>B”或“A<B”或“A=B”)。
【答案】(1)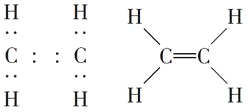
(2)CH2=CH—CH3+Br2―→CH2Br—CHBr—CH3加成反应
(3)下层无色,上层紫红色
(4)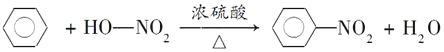 取代反应
取代反应
(5)A>B
【解析】
试题A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平,则A为CH2=CH2,B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,则原子个数之比为1:1,若符合CnH2n-6,B的相对分子质量为78,则B为12n+2n-6=78,解得n=6,所以B为苯。
(1)根据上述分析,A为乙烯,电子式为![]() ,结构简式为CH2=CH2。
,结构简式为CH2=CH2。
(2)A相邻的同系物C为CH2=CHCH3,使溴的CCl4溶液水褪色发生加成反应,该反应为CH3CH=CH2+Br2→CH2BrCHBrCH3,反应类型为加成反应。
(3)碘水中加入苯发生萃取,苯的密度比水的小,则苯在上层,观察到分层 ,下层几乎无色,上层紫红色。
(4)B与浓H2SO4与浓HNO3在50-60℃反应的化学反应方程式为C6H6+HO-NO2![]() C6H5NO2+H2O,该反应属于取代反应。
C6H5NO2+H2O,该反应属于取代反应。
(5)A为乙烯,B为苯,设A、B的质量均为m,由CxHy消耗x+y/4氧气可知,乙烯消耗氧气为m÷28×3= 3m/28,苯消耗氧气为m÷78×7.5=5m/52,则等质量的A、B完全燃烧时消耗O2的物质的量A>B。


科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述不正确的是:
A. 2.7 g 金属铝分别与足量的NaOH溶液和盐酸反应转移的电子数目均为0.3NA
B. 标准状况下,2.24 L Cl2与过量NaOH溶液反应,转移的电子总数为0.1 NA
C. 1L 1 molL-1 Na2CO3溶液中阴离子数小于NA
D. 2.3 g金属钠完全反应生成Na2O与Na2O2的混合物中阴离子数为0.05 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有①熔融的BaCl2、②H2SO4溶于水、③NH4Cl溶于水、④Na2O2溶液、⑤干冰升华、⑥溴水被CCl4萃取六种物质,按下列要求回答:
(1)化学键没有破坏的是__________,仅破坏共价键的是________,仅破坏离子键的是________,离子键和共价键都破坏的是_____________。
(2)NH4Cl的电子式是________,CO2的结构和CS2相似,请你写出CS2的电子式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。
(1)锌片上发生的电极反应:___________________;
(2)银片上发生的电极反应:____________________;
(3)总反应的离子方程式:_________________;
(4)在______片上有气泡产生,电子从______片上流向_______片上。
(5)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算产生氢气的体积(标准状况)为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. ![]() 的名称为3-甲基丁烷
的名称为3-甲基丁烷
B. CH3CH2CH2CH2CH3和 ![]() 互为同素异形体
互为同素异形体
C. CH3CH2OH和 ![]() 具有相同的官能团,互为同系物
具有相同的官能团,互为同系物
D.  和
和  为同一物质
为同一物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某容积一定的密闭容器中充入2molSO2和1molO2,一定条件下发生如下反应:2SO2+O2![]() 2SO3。下列说法不正确的是
2SO3。下列说法不正确的是
A. 升高温度或充入一定量O2均能加快化学反应速率
B. 达到平衡状态时,SO2、O2、SO3物质的量之比一定为2:1:2
C. 当SO2的生成速率与SO3的生成速率相等时,反应达到平衡状态
D. 达到平衡状态时,生成SO3的物质的量一定小于2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.电解精炼铜时,粗铜跟电源的正极相连
B.用石墨做电极电解饱和食盐水时,阴极产生黄绿色气体
C.构成原电池的正极和负极必须是两种不同金属
D.原电池是把化学能转变为电能的装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如下图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是:

A. 194 B. 391 C. 516 D. 658
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com