
 H++B(OH)4-.
H++B(OH)4-.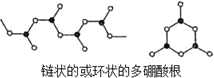 ,其组成可表示为(BO2)nn-.
,其组成可表示为(BO2)nn-.分析 (1)硼处于第二周期ⅢA族;硼与Si处于对角线位置,二者性质最相似;
(2)在硼酸[B(OH)3]分子中,B原子与3个羟基相连,则分子中B原子杂化轨道数目为3,其晶体具有与石墨相似的层状结构,其同层分子间的主要作用力是氢键;
(3)H3BO3与水分子形成配位键后电离生成B(OH)4-、H+;
(4)由均摊法,可知每个B原子独自占有2个O原子,B元素化合价为+2,O元素化合价为-2,计算化合价代数和确定离子所带电荷;
(5)六方氮化硼晶体结构与石墨晶体相似,层间相互作用为分子间作用力;
在金刚石的晶胞中含有的碳原子数为4+8×$\frac{1}{8}$+6×$\frac{1}{2}$=8,立方氮化硼与金刚石相似,所以氮化硼晶胞中硼原子和氮原子的数目各有4个,计算晶胞质量,再根据ρ=$\frac{m}{V}$计算立方氮化硼的密度.
解答 解:(1)硼处于第二周期ⅢA族,价电子排布式为2s22p1,硼与Si处于对角线位置,二者性质最相似,由此预测自然界没有游离态的硼,
故答案为:2s22p1;Si;没有;
(2)在硼酸[B(OH)3]分子中,B原子与3个羟基相连,则分子中B原子杂化轨道数目为3,分子中B原子杂化轨道的类型是,其晶体具有与石墨相似的层状结构,其同层分子间的主要作用力是氢键,
故答案为:sp2;氢键;
(3)H3BO3与水分子形成配位键后电离生成B(OH)4-、H+,即电离方程式为:H3BO3+H2O  H++B(OH)4-,
H++B(OH)4-,
故答案为:H3BO3+H2O  H++B(OH)4-;
H++B(OH)4-;
(4)由均摊法,可知每个B原子独自占有2个O原子,B元素化合价为+2,O元素化合价为-2,多硼酸根的化合价代数和为3n+2×n(-2)=-n,故多硼酸根组成可表示为:(BO2)nn-,
故答案为:(BO2)nn-;
(5)六方氮化硼晶体结构与石墨晶体相似,层间相互作用为分子间作用力;
在金刚石的晶胞中含有的碳原子数为4+8×$\frac{1}{8}$+6×$\frac{1}{2}$=8,立方氮化硼与金刚石相似,所以氮化硼晶胞中硼原子和氮原子的数目各有4个,晶胞质量为4×$\frac{25}{{N}_{A}}$g,晶胞边长为361.5pm,则氮化硼的密度为4×$\frac{25}{{N}_{A}}$g÷(361.5×10-10cm)3=$\frac{4×25}{{N}_{A}×(361.5×1{0}^{-10})^{3}}$g•cmˉ3,
故答案为:分子间作用力;$\frac{4×25}{{N}_{A}×(361.5×1{0}^{-10})^{3}}$.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、微粒结构、杂化方式、氢键、晶胞结构与计算等,(5)中密度计算为易错点,注意识记中学常见晶胞结构,难度中等.


科目:高中化学 来源: 题型:推断题
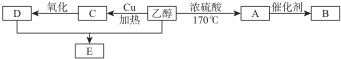
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 HClO
HClO
 Mg
Mg .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③⑤ | C. | ②④⑤ | D. | ②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用肥皂水检查煤气管道是否漏气和用浓氨水检查氯气管道是否漏气的原理相同 | |
| B. | 在轮船的吃水线下焊上锌块是利用了牺牲阳极的阴极保护法防止船体被腐蚀 | |
| C. | 天津港爆炸事故救援过程中,化学品仓库内存放有金属钠、电石、甲苯二异氰酸酯等化学危险品,消防员不应用水而应用泡沫灭火器将火扑灭 | |
| D. | 工业生产中,常将氯气通入澄清石灰水中,制取漂白粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气的首要污染物包括CO2、SO2、NO、NO2、O3等 | |
| B. | PM2.5指的是直径为2.5微米的可吸入颗粒物,因其直径小、比表面积大、活性强、易吸附有毒有害的物质,对人的健康和大气环境质量的影响较大 | |
| C. | 光化学烟雾的形成与氮氧化物有关 | |
| D. | SO2的治理技术和设备有:原煤脱硫技术、改进燃烧技术和烟气脱硫设备等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核外有38个电子,核内有95个质子 | B. | 核外有38个电子,核内有57个中子 | ||
| C. | 核外有57个电子,核内有57个质子 | D. | 核外有57个电子,核内有38个质子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com