
【题目】一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5,表示,咸水中的主要溶质为NaCl。下列有关说法正确的是

A. a为原电池的负极
B. b电极附近溶液的pH减小
C. a电极反应式为![]()
D. 中间室:Na+移向左室,Cl-移向右室
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。 据此下列说法错误的是
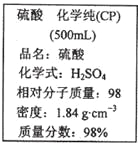
A. 该硫酸具有强烈的腐蚀性,应放于危险化学用品柜中妥善保管
B. 取10 mL该硫酸于烧杯中,再加等体积的水,可配得49%的硫酸
C. 配制200mL4.6 mol·L-1的稀硫酸需取该硫酸50 mL
D. 该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】抗丙肝新药的中间体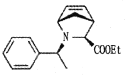 合成路线图如下:
合成路线图如下:

已知:-Et为乙基。
(1)![]() 的名称是____,
的名称是____,![]() 所含官能团的名称是____。
所含官能团的名称是____。
(2)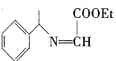 的分子式为____。
的分子式为____。
(3)反应②化学方程式为________,反应③的反应类型是____。
(4)写出与 互为同分异构体的芳香类化合物的结构简式(核磁共振氢谱为四组峰,峰面积比为1:2:2:6,且不含-NH2)____
互为同分异构体的芳香类化合物的结构简式(核磁共振氢谱为四组峰,峰面积比为1:2:2:6,且不含-NH2)____
(5)设计由乙醇、1,3-丁二烯和甲氨( CH3NH2)合成![]() 路线(其他试剂任选)。__________
路线(其他试剂任选)。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下发生反应3A(g)+2B(g) ![]() zC(g)+2D(g),在2 L 的密闭容器中把4 mol A 和 2 mol B 混合,2 min 后反应达到平衡时生成 1.6 mol C,又测得反应速率v(D)=0.2 mol·(L·min) -1 。则下列说法不正确的是
zC(g)+2D(g),在2 L 的密闭容器中把4 mol A 和 2 mol B 混合,2 min 后反应达到平衡时生成 1.6 mol C,又测得反应速率v(D)=0.2 mol·(L·min) -1 。则下列说法不正确的是
A. z=4 B. B 的转化率是40%
C. A 的平衡浓度是1.4 mol·L-1 D. 平衡时气体压强是原来压强的0.9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图装置可处理乙醛废水,乙醛在阴、阳极分别转化为乙醇和乙酸。下列说法正确的是( )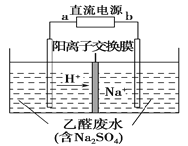
A.b电极为正极
B.电解过程中,阴极区Na2SO4的物质的量增大
C.阳极电极反应式为CH3CHO-2e-+H2O===CH3COOH+2H+
D.电解过程中,阴、阳极还分别产生少量的O2和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的

A. 用溴水能鉴别CH3CH==CHCH2OH和CH3CH2CH2CHO
B. 用如图所示方法可保护钢闸门不被腐蚀
C. 根据核磁共振氢谱不能鉴别1溴丙烷和2溴丙烷
D. 食用花生油和鸡蛋清都能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 用惰性电极电解MgCl2溶液:2Cl- + 2H2O![]() 2OH-+ H2↑+ Cl2↑
2OH-+ H2↑+ Cl2↑
B. 用银氨溶液检验乙醛中的醛基:CH3CHO+![]() +2OH-
+2OH-![]() CH3COO-+
CH3COO-+![]() +3NH3+2Ag↓+H2O
+3NH3+2Ag↓+H2O
C. 邻羟基苯甲酸中加入足量NaHCO3溶液:

D. 向含NaOH的Cu(OH)2悬浊液中加入乙醛溶液并加热: CH3CHO +2Cu(OH)2+ OH-![]() CH3COO-+ Cu2O↓+3H2O
CH3COO-+ Cu2O↓+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠广泛用于工业、建筑业及食品加工业。某课外活动小组的同学拟制备亚硝酸钠、测定其产品的纯度并验证亚硝酸钠的某些性质。
(1)甲组同学采用下图装置制取亚硝酸钠。
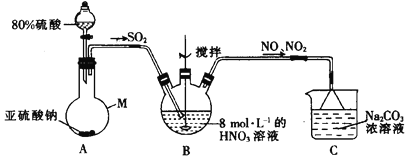
①仪器M的名称是______________。
②装置A中用较浓的硫酸而不用稀硫酸的原因是_____________________。
③若装置B中生成等物质的量的NO与NO2,则装置B中发生反应的离子方程式为______。
④已知NO与NaOH溶液不反应,而NO2可与NaOH溶液发生反应:2NO2+2NaOH ![]() NaNO3+NaNO2+H2O。若通入装置C中的NO与NO2物质的量之比为1 :1,则装置C中发生反应的化学方程式为_______。
NaNO3+NaNO2+H2O。若通入装置C中的NO与NO2物质的量之比为1 :1,则装置C中发生反应的化学方程式为_______。
(2)乙组同学拟测定甲组制得的产品中NaNO2的纯度。乙组同学采用高锰酸钾滴定法,称取m g试样于锥形瓶中,加入适量水溶解,然后用c mol·L-1的KMnO4溶液(适量稀H2SO4酸化)进行滴定,并重复上述操作2次。
①高锰酸钾溶液应盛放在___________(填“酸式”或“碱式”)滴定管中。
②滴定至终点时溶液的颜色变化是__________________。
③若滴定至终点时平均消耗VmL标准溶液,则产品的纯度为_____(用含c、m、V的代数式表示)。
(3)丙组同学拟设计实验证明:
①酸性条件下NaNO2具有氧化性。实验操作为________________________。
②HNO2的酸性比CH3COOH强。实验操作为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,容积固定的密闭容中对于可逆反应X(g)+3Y(g) ![]() 2Z(g),若X、Y、Z的起始浓度分别为 c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断不合理的是( )
2Z(g),若X、Y、Z的起始浓度分别为 c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断不合理的是( )
A. c1∶c2=1∶3
B. 平衡时,Y和Z的生成速率之比为2∶3
C. 达到平衡时,容器内的压强不再变化
D. c1的取值范围为0 mol/L<c1<0.14 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com