
| A. | Ca2+的结构示意图为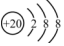 ,NH4Cl的电子式为 ,NH4Cl的电子式为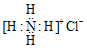 | |
| B. | 抗冰雪灾害时使用的融雪剂所含的氯化钠、氯化镁、氯化钙都属于盐 | |
| C. | 表示乙炔(CH≡CH)“燃烧热”的热化学方程式:CH≡CH(g)+$\frac{5}{2}{O_2}$(g)→2CO2(g)+H2O(g)+1256kJ | |
| D. | 质量数为16的氧原子:816O |
分析 A.NH4Cl的电子式中氯原子核外的电子没有标出;
B.氯化钠、氯化镁、氯化钙都为金属的氯化物,属于盐;
C.表示燃烧热,生成的水应为液态;
D.质量数应在左上角.
解答 解:A.NH4Cl的电子式中氯原子核外的电子没有标出,应为 ,故A错误;
,故A错误;
B.氯化钠、氯化镁、氯化钙都为金属的氯化物,可电离出金属离子和酸根离子,属于盐,故B正确;
C.表示燃烧热,应生成稳定的氧化物,生成的水应为液态,故C错误;
D.质量数应在左上角,应为168O,故D错误.
故选B
点评 本题主要是对常见化学用语的考查,为高频考点,侧重考查学生的双基知识以及化学用语的掌握,涉及核素的表示方法、质量数与质子数和中子数的关系、电子式的书写、结构简式书写等,难度不大.


科目:高中化学 来源: 题型:选择题
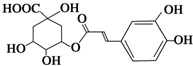 从金银花中提取的绿原酸结构简式如图所示.其有抗菌、消炎、解毒.利胆.降压和增加胃肠蠕动的作用.用于急性细菌性感染及放、化疗所致的白细胞减少症.下列说法不正确的是( )
从金银花中提取的绿原酸结构简式如图所示.其有抗菌、消炎、解毒.利胆.降压和增加胃肠蠕动的作用.用于急性细菌性感染及放、化疗所致的白细胞减少症.下列说法不正确的是( )| A. | 绿原酸的分子式为C16H18O9 | |
| B. | 绿原酸及其水解产物之一在空气中均能稳定存在,遇FeCl3溶液时显紫色 | |
| C. | 1mol绿原酸与NaOH溶液反应时,最多消4molNaOH | |
| D. | 1mol绿原酸与足量金属Na反应时能产生3molH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称取7.68g硫酸铜,加入 480mL水 | B. | 称取12.0g胆矾配成500mL溶液 | ||
| C. | 称取8.0g硫酸铜,加入500mL水 | D. | 称取12.5g胆矾配成500mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CS2是极性键构成的极性分子 | |
| B. | SO2与CO2为等电子体 | |
| C. | 金属晶体的六方最密堆积和面心立方最密堆积的方式空间利用率最高 | |
| D. | 1molNaHSO4熔融态时有3mol离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图中新月形分子和环状分子“组合”在一起,铜离子起关键作用 | |
| B. | 利用此方式可以合成新分子,同时也可能创造一种全新“机械键” | |
| C. | 在创造新分子技术中,铜离子是唯一可以借助的金属离子 | |
| D. | 此技术可以“互锁”合成 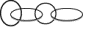 分子,甚至成更复杂的分子 分子,甚至成更复杂的分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则该溶液中一定不含K+ | |
| B. | 向无色溶液中加入盐酸酸化的BaCl2溶液有白色沉淀出现,则该溶液中一定含有SO42- | |
| C. | 向无色溶液中加入盐酸产生能使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- | |
| D. | 向某溶液中加入KSCN溶液无现象,再滴入少量H2O2,呈血红色,则该溶液中一定含有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
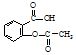 )具有解热镇痛作用(选填“解热镇痛”或“抗菌消炎”),必须密闭干燥存储以防止发生水解,在酸性条件下阿司匹林水解生成乙酸和
)具有解热镇痛作用(选填“解热镇痛”或“抗菌消炎”),必须密闭干燥存储以防止发生水解,在酸性条件下阿司匹林水解生成乙酸和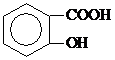 (写出结构简式).
(写出结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 Na2SO3•7H2O是食品工业中常用的漂白剂、抗氧化剂和防腐剂.该小组同学用Na2SO3与浓硫酸制备SO2,并把SO2通入NaNO3溶液中,他们为了检验产生的气体是NO还是
Na2SO3•7H2O是食品工业中常用的漂白剂、抗氧化剂和防腐剂.该小组同学用Na2SO3与浓硫酸制备SO2,并把SO2通入NaNO3溶液中,他们为了检验产生的气体是NO还是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com