

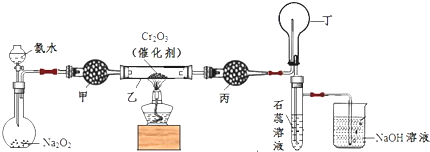
·ÖĪö ÓÉ·ÖĄėĮ÷³ĢæÉÖŖ£¬ŹŌ¼Į¢Ł½«Ć¾Ąė×Ó×Ŗ»ÆĪŖ³Įµķ£¬ĒŅ²»ŅżČėŠĀŌÓÖŹ£¬Ōņ¢ŁĪŖNaOH£¬ÓÉ×Ŗ»ÆæÉÖŖ£¬ŹŌ¼Į¢ŚĪŖŃĪĖį£¬Č»ŗóŌŚHClĘųĮ÷ÖŠÕō·¢µĆµ½ĪŽĖ®ĀČ»ÆĆ¾£¬×īŗóµē½āČŪČŚĀČ»ÆĆ¾µĆµ½Mg£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗÓÉ·ÖĄėĮ÷³ĢæÉÖŖ£¬ŹŌ¼Į¢Ł½«Ć¾Ąė×Ó×Ŗ»ÆĪŖ³Įµķ£¬ĒŅ²»ŅżČėŠĀŌÓÖŹ£¬Ōņ¢ŁĪŖNaOH£¬ÓÉ×Ŗ»ÆæÉÖŖ£¬ŹŌ¼Į¢ŚĪŖŃĪĖį£¬Č»ŗóŌŚHClĘųĮ÷ÖŠÕō·¢µĆµ½ĪŽĖ®ĀČ»ÆĆ¾£¬×īŗóµē½āČŪČŚĀČ»ÆĆ¾µĆµ½Mg£¬
£Ø1£©ŹŌ¼Į¢Ł½«Ć¾Ąė×Ó×Ŗ»ÆĪŖ³Įµķ£¬ĒŅ²»ŅżČėŠĀŌÓÖŹ£¬Ōņ¢ŁĪŖNaOH£¬MgSO4ÓėNaOH·“Ӧɜ³ÉĮĖMg£ØOH£©2£¬Ąė×Ó·½³ĢŹ½ĪŖMg2++2OH-ØTMg£ØOH£©2”ż£¬ŅŖŹ¹MgSO4ĶźČ«×Ŗ»ÆĪŖ³Įµķ£¬¼ÓČėŹŌ¼ĮµÄĮæÓ¦¹żĮ棬ŅņMg£ØOH£©2³Įµķ²»ČÜÓŚĖ®£¬æÉÓĆ¹żĀĖµÄ·½·Ø·ÖĄė£¬
¹Ź“š°øĪŖ£ŗNaOHČÜŅŗ£»¹żĮ棻¹żĀĖ£»
£Ø2£©·“Ó¦¢ŁµÄĄė×Ó·½³ĢŹ½ŹĒMg2++2OH-ØTMg£ØOH£©2”ż£¬
¹Ź“š°øĪŖ£ŗMg2++2OH-ØTMg£ØOH£©2”ż£»
£Ø3£©ĪŽĖ®MgCl2ŌŚČŪȌדĢ¬ĻĀ£¬Ķصēŗó»į²śÉśMgŗĶCl2£ŗMgCl2£ØČŪČŚ£©$\frac{\underline{\;Ķصē\;}}{\;}$Mg+Cl2”ü£¬“Ó”°Ō×Ó¾¼Ć”±µÄ½Ē¶ČĄ“æ“£¬øĆ·“Ó¦²śÉśµÄø±²śĘ·Cl2Ó¦½ųČėÉś²śŃĪĖįµÄ¹¤³§ŗĶĒāĘų·“Ӧɜ³ÉĀČ»ÆĒāÓĆĄ“ÖʱøŃĪĖį£¬
¹Ź“š°øĪŖ£ŗMgCl2£ØČŪČŚ£©$\frac{\underline{\;Ķصē\;}}{\;}$Mg+Cl2”ü£»½ųČėÉś²śŃĪĖįµÄ¹¤³§ŗĶĒāĘų·“Ӧɜ³ÉĀČ»ÆĒāÓĆĄ“ÖʱøŃĪĖį£®
µćĘĄ ±¾ĢāŅŌŗ£Ė®ĢįĆ¾æ¼²é»ģŗĻĪļ·ÖĄėĢį“棬ĪŖøßĘµæ¼µć£¬°ŃĪÕĮ÷³ĢÖŠµÄ·“Ó¦”¢»ģŗĻĪļ·ÖĄė·½·ØĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪö”¢ŹµŃéÄÜĮ¦µÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĻ©ĶØČėĖįŠŌøßĆĢĖį¼ŲČÜŅŗ£¬·¢ÉśČ”“ś·“Ó¦ | |
| B£® | ĻņŹŌ¹ÜÖŠ¼ÓČė2mL5%ĮņĖįĶČÜŅŗ£¬ŌŁµĪ¼Ó¼øµĪĻ”ĒāŃõ»ÆÄĘČÜŅŗ£¬»ģŌČ£¬Į¢¼“¼ÓČė2mL10%ĘĻĢŃĢĒČÜŅŗ£¬ŌŚ¾Ę¾«µĘÉĻ¼ÓČČÖĮ·ŠĢŚ£¬æÉ擵½ŗģÉ«³Įµķ | |
| C£® | ÓĆÕōĮó·Ø·ÖĄėŅŅĖįŅŅõ„ŗĶ±„ŗĶĢ¼ĖįÄĘČÜŅŗ | |
| D£® | ĆŗµÄøÉĮó”¢ĆŗµÄĘų»Æ”¢ŹÆÓĶĮŃ»ÆŹĒ»Æѧ±ä»Æ£¬ŹÆÓĶµÄ·ÖĮóŹĒĪļĄķ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ĒėŌŚøĆ·½³ĢŹ½ÖŠ±źĆ÷µē×Ó×ŖŅʵķ½ĻņŗĶŹżÄæ
ĒėŌŚøĆ·½³ĢŹ½ÖŠ±źĆ÷µē×Ó×ŖŅʵķ½ĻņŗĶŹżÄæ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĻ©·¢Éś¼Ó¾Ū·“Ó¦ÖĘµĆ¾ŪŅŅĻ©øß·Ö×Ó²ÄĮĻ | |
| B£® | ÓĆ¼×ĶéÓėĀČĘųÖʱøŅ»ĀČ¼×Ķé | |
| C£® | ÓƱ½ŗĶÅØĮņĖį”¢ÅØĻõĖįĪŖŌĮĻÖĘČ”Ļõ»ł±½ | |
| D£® | ÓĆŹÆ»ŅŹÆŗĶĻ”ŃĪĖį·“Ó¦ÖʵƶžŃõ»ÆĢ¼ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«°±ĘųĶØČė“×ĖįÖŠ£ŗNH3+H+ØTNH4+ | |
| B£® | ŌŚNH4ClČÜŅŗÖŠµĪČėĒāŃõ»ÆÄĘČÜŅŗ²¢¼ÓČČ£ŗNH4++OH-$\frac{\underline{\;\;”÷\;\;}}{\;}$NH3”ü+H2O | |
| C£® | ½«ÉŁĮæĶŠ¼·ÅČėĻ”ĻõĖįÖŠ£ŗCu+4H++NO3-ØTCu2++NO”ü+2H2O | |
| D£® | ½«Ļ”ĻõĖįµĪŌŚĢśĘ¬ÉĻ£ŗFe+2H+ØTFe2++H2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū | B£® | ¢Ł¢Ü¢Ž | C£® | ¢Ś¢Ū¢Ž | D£® | ¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņĖ®ÖŠĶØČė¶žŃõ»ÆĮņĘųĢå | B£® | ĻņĖ®ÖŠ¼ÓČėÉŁĮæĀČ»ÆĢś¹ĢĢå | ||
| C£® | ½«Ė®¼ÓČČÖó·Š | D£® | ĻņĖ®ÖŠ¼ÓČėĢ¼ĖįÄĘ¾§Ģå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·“Ó¦ŗóČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”¹ŲĻµĪŖ£ŗc£ØNO3-£©£¾c£ØAg+£©£¾c£ØCl-£©£¾c£ØI-£© | |
| B£® | ČÜŅŗÖŠĻČ²śÉśµÄŹĒAgI³Įµķ | |
| C£® | AgClµÄKSPµÄŹżÖµĪŖ1.69”Į10-10 | |
| D£® | ČōŌŚAgClŠü×ĒŅŗÖŠµĪ¼ÓKIČÜŅŗ£¬°×É«³Įµķ»į×Ŗ±ä³É»ĘÉ«³Įµķ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
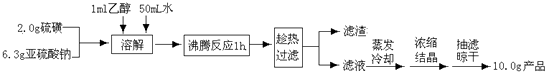
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com