
·ÖĪö £Ø1£©Ö»ŅŖÄܼõÉŁ»ÆŹÆČ¼ĮĻµČ׏Ō“µÄŌĖÓƶ¼ŹōÓŚ”°æŖŌ“½ŚĮ÷”±£»
£Ø2£©¢ŁĪļÖŹÄÜĮæŌ½øßŌ½²»ĪČ¶Ø£»ŅĄ¾ŻĶ¼ĻóÅŠ¶ĻŹÆÄ«µÄČ¼ÉÕČČ£»
¢ŚŅĄ¾Ż¼«Öµ¼ĘĖćÅŠ¶ĻÉś³ÉµÄĘųĢå×é³É£¬½įŗĻČČ»Æѧ·½³ĢŹ½¼ĘĖćµĆµ½£»
£Ø3£©¾É¼ü¶ĻĮŃĪüŹÕµÄÄÜĮæ¼õČ„ŠĀ¼üÉś³ÉŹĶ·ÅµÄÄÜĮæÖµ¼“ĪŖ»Æѧ·“Ó¦ĖłĪüŹÕµÄÄÜĮ棬½įŗĻN2”¢O2·Ö×ÓÖŠ»Æѧ¼üµÄ¼üÄÜ·Ö±šŹĒ946kJ•mol-1”¢497kJ•mol-1£¬N2£Øg£©+O2£Øg£©=2NO£Øg£©£¬”÷H=+180kJ•mol-1æÉŅŌ¼ĘĖćNO·Ö×ÓÖŠ»Æѧ¼üµÄ¼üÄÜ£»
£Ø4£©ĄūÓĆøĒĖ¹¶ØĀɽįŗĻŅŃÖŖČČ»Æѧ·½³ĢŹ½¼ĘĖć·“Ó¦ČČ£¬ŌŁŠ“³öČČ»Æѧ·½³ĢŹ½£®
½ā“š ½ā£ŗ£Ø1£©Ö»ŅŖÄܼõÉŁ»ÆŹÆČ¼ĮĻµČ׏Ō“µÄŌĖÓƶ¼ŹōÓŚ”°æŖŌ“½ŚĮ÷”±£¬a”¢c”¢dÄܼõÉŁ»ÆŹÆČ¼ĮĻµÄŌĖÓĆ£¬b£®“óĮ¦æŖ²ÉĆŗ”¢ŹÆÓĶŗĶĢģČ»Ęų£¬²»ÄܼõÉŁ»ÆŹÆČ¼ĮĻµÄŌĖÓĆ£¬¹Ź“š°øĪŖ£ŗacd£»
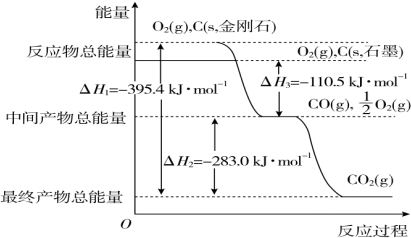
£Ø2£©¢ŁĶ¼Ļó·ÖĪö½šøÕŹÆÄÜĮæøßÓŚŹÆÄ«£¬ÄÜĮæŌ½µĶŌ½ĪČ¶Ø£¬ĖłŅŌĖµĆ÷ŹÆÄ«ĪČ¶Ø£¬Ķ¼Ļó·ÖĪö1molŹÆÄ«ĶźČ«Č¼ÉÕÉś³É1mol¶žŃõ»ÆĢ¼·Å³öµÄČČĮæĪŖ£Ø110.5+283.0£©kJ=393.5kJ£¬ŌņŹÆÄ«µÄČ¼ÉÕČČĪŖ393.5kJ?mol-1£¬
¹Ź“š°øĪŖ£ŗŹÆÄ«£»393.5kJ?mol-1£»
¢Ś12gŹÆÄ«ĪļÖŹµÄĮæĪŖ1mol£¬ŌŚŅ»¶ØĮææÕĘųÖŠČ¼ÉÕ£¬ŅĄ¾ŻŌŖĖŲŹŲŗć£¬ČōÉś³É¶žŃõ»ÆĢ¼ÖŹĮæĪŖ44g£¬ČōÉś³ÉŅ»Ńõ»ÆĢ¼ÖŹĮæĪŖ28g£¬Éś³ÉĘųĢå36g£¬28g£¼36g£¼44g£¬ÅŠ¶ĻÉś³ÉµÄĘųĢåĪŖŅ»Ńõ»ÆĢ¼ŗĶ¶žŃõ»ÆĢ¼ĘųĢ壬ÉčŅ»Ńõ»ÆĢ¼ĪļÖŹµÄĮæĪŖx£¬¶žŃõ»ÆĢ¼ĪļÖŹµÄĮæĪŖ£Ø1-x£©mol£¬28x+44£Ø1-x£©=36g£¬x=0.5mol£¬¶žŃõ»ÆĢ¼ĪļÖŹµÄĮæĪŖ0.5mol£»ŅĄ¾ŻĶ¼Ļó·ÖĪö£¬C£ØŹÆÄ«£¬s£©+O2£Øg£©ØTCO2£Øg£©”÷H=-393.5 kJ•mol-1 £»C£ØŹÆÄ«£¬s£©+$\frac{1}{2}$O2£Øg£©ØTCO£Øg£©”÷H=-110.5kJ•mol-1
Éś³É¶žŃõ»ÆĢ¼ŗĶŅ»Ńõ»ÆĢ¼»ģŗĻĘųĢå·Å³öČČĮæ=393.5kJ•mol-1 ”Į0.5mol+110.5 kJ•mol-1 ”Į0.5mol=252kJ£»12gŹÆÄ«ŌŚŅ»¶ØĮææÕĘųÖŠČ¼ÉÕ£¬Éś³ÉĘųĢå36g£¬øĆ¹ż³Ģ·Å³öµÄČČĮæĪŖ252.0kJ£¬
¹Ź“š°øĪŖ£ŗ252.0 kJ£»
£Ø3£©øł¾ŻN2”¢O2·Ö×ÓÖŠ»Æѧ¼üµÄ¼üÄÜ·Ö±šŹĒ946kJ•mol-1”¢497kJ•mol-1ŅŌ¼°·“Ó¦N2£Øg£©+O2£Øg£©=2NO£Øg£©”÷H=+180kJ•mol-1æÉÉčNO·Ö×ÓÖŠ»Æѧ¼üµÄ¼üÄÜĪŖx£¬ŌņÓŠ£ŗ946kJ•mol-1+497kJ•mol-1-2x=180kJ•mol-1 µĆ£ŗx=631.5kJ•mol-1£¬
¹Ź“š°øĪŖ£ŗ631.5£»
£Ø4£©ŅŃÖŖ¢ŁC£ØŹÆÄ«£¬s£©+O2£Øg£©ØTCO2£Øg£©”÷H=-393.5 kJ•mol-1 £¬
¢ŚC£ØŹÆÄ«£¬s£©+$\frac{1}{2}$O2£Øg£©ØTCO£Øg£©”÷H=-110.5 kJ•mol-1£¬
¢ŪN2£Øg£©+O2£Øg£©=2NO£Øg£©”÷H=+180kJ•mol-1£¬
ÓÉøĒĖ¹¶ØĀÉ£ŗ·½³ĢŹ½¢Ł”Į2-¢Ś”Į2-¢ŪµĆ 2NO£Øg£©+2CO£Øg£©ØTN2£Øg£©+2CO2£Øg£©”÷H=-746.0kJ?mol-1£¬
¹Ź“š°øĪŖ£ŗ2NO£Øg£©+2CO£Øg£©ØTN2£Øg£©+2CO2£Øg£©”÷H=-746.0kJ?mol-1£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ·“Ó¦ÓėÄÜĮ攢øĒĖ¹¶ØĀÉ”¢ĪļÖŹĪČ¶ØŠŌµÄÅŠ¶Ļ”¢¼üÄܵļĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬×¢Ņā°ŃĪÕøĒĖ¹¶ØĀɵÄŗ¬Ņå¼°ĘäÓ¦ÓĆ·½·Ø£®


 Š”ѧɜ10·ÖÖÓæŚĖć²āŹŌ100·ÖĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓæŚĖć²āŹŌ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 mol NH3µÄÖŹĮæĪŖ17 g•mol-1 | |
| B£® | H2SO4µÄĦ¶ūÖŹĮæĪŖ98g | |
| C£® | 3.01”Į1023øöO3·Ö×ÓŗĶ 3.01”Į1023øöO2·Ö×Óµē×ÓŹżÖ®±ČµČÓŚ1£ŗ1 | |
| D£® | µČĪļÖŹµÄĮæµÄCO2·Ö×ÓŗĶCO·Ö×ÓµÄÖŹĮæ±ČµČÓŚ11£ŗ7 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
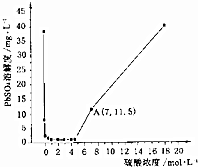 ŅŃÖŖ25”ꏱKSP£ØPbSO4£©=1.6”Į10-8”¢KSP£ØBaSO4£©=1.1”Į10-10£¬øĆĪĀ¶ČĻĀPbSO4ŌŚ²»Ķ¬ÅØ¶ČµÄĮņĖįÖŠµÄČܽā¶ČČēĶ¼ĖłŹ¾£®ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
ŅŃÖŖ25”ꏱKSP£ØPbSO4£©=1.6”Į10-8”¢KSP£ØBaSO4£©=1.1”Į10-10£¬øĆĪĀ¶ČĻĀPbSO4ŌŚ²»Ķ¬ÅØ¶ČµÄĮņĖįÖŠµÄČܽā¶ČČēĶ¼ĖłŹ¾£®ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | Ķ¼ÖŠAµćc£ØSO42-£©=7mol•L-1 | |
| B£® | ¹żĀĖµÄPbSO4³Įµķ£¬ÓĆĻ”ĮņĖįĻ“µÓ£¬æÉŅŌ¼õÉŁ³ĮµķĖšŗÄ | |
| C£® | ĮņĖįÅØ¶Č“óÓŚ5mol•L-1Ź±£¬PbSO4Čܽā¶ČŌö“óµÄŌŅņŹĒ×Ŗ»Æ³ÉPb£ØHSO4£©2 | |
| D£® | ½«Pb£ØNO3£©2”¢Ba£ØNO3£©2»ģŗĻČÜŅŗµĪČėĻ”ĮņĖįÖŠ£¬ÄÜÉś³ÉPbSO4ŗĶBaSO4Į½ÖÖ³Įµķ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ±½ŅŅĻ©£Ø
±½ŅŅĻ©£Ø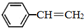 £©ŹĒÉś²śø÷ÖÖĖÜĮĻµÄÖŲŅŖµ„Ģ壬æÉĶعżŅŅ±½“ß»ÆĶŃĒāÖĘµĆ£ŗ
£©ŹĒÉś²śø÷ÖÖĖÜĮĻµÄÖŲŅŖµ„Ģ壬æÉĶعżŅŅ±½“ß»ÆĶŃĒāÖĘµĆ£ŗ CH2CH3£Øg£©$\stackrel{“߻ƼĮ}{?}$
CH2CH3£Øg£©$\stackrel{“߻ƼĮ}{?}$ =CH2£Øg£©+H2£Øg£©”÷=-Q1kJ£®mol-1
=CH2£Øg£©+H2£Øg£©”÷=-Q1kJ£®mol-1 £®
£®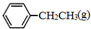 ”¢
”¢ ”¢H2£Øg£©µÄČ¼ÉÕČČ£Ø”÷H£©·Ö±šĪŖ-Q1 kJ•mol-1”¢-Q2kJ•mol-1”¢-Q3 kJ•mol-1£¬Š“³öQÓėQ1”¢Q2”¢Q3µÄ¹ŲĻµŹ½Q2+Q3-Q1£®
”¢H2£Øg£©µÄČ¼ÉÕČČ£Ø”÷H£©·Ö±šĪŖ-Q1 kJ•mol-1”¢-Q2kJ•mol-1”¢-Q3 kJ•mol-1£¬Š“³öQÓėQ1”¢Q2”¢Q3µÄ¹ŲĻµŹ½Q2+Q3-Q1£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
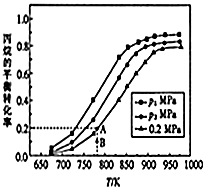 ±ūĻ©£ØC3H6£©ŹĒÖĘŌģ¾Ū±ūĻ©”¢±ūĻ©ėęµČ»Æ¹¤²śĘ·µÄŌĮĻ£®ÄæĒ°ÕżŌŚæŖ·¢±ūĶé£ØC3H8£©ĮŃ½āÖĘČ”±ūĻ©£¬ĘäŌĄķĪŖC3H8£Øg£©?C3H6£Øg£©+H2£Øg£©”÷H£®»Ų“šĻĀĮŠĪŹĢā£ŗ
±ūĻ©£ØC3H6£©ŹĒÖĘŌģ¾Ū±ūĻ©”¢±ūĻ©ėęµČ»Æ¹¤²śĘ·µÄŌĮĻ£®ÄæĒ°ÕżŌŚæŖ·¢±ūĶé£ØC3H8£©ĮŃ½āÖĘČ”±ūĻ©£¬ĘäŌĄķĪŖC3H8£Øg£©?C3H6£Øg£©+H2£Øg£©”÷H£®»Ų“šĻĀĮŠĪŹĢā£ŗ| ¹²¼Ū¼ü | C-C | C=C | C-H | H-H |
| ¼üÄÜ/KJ•mol-1 | 348 | 615 | 413 | 436 |
| n£ØCO2£©/n£ØC3H8£©ĪĀ¶Č/K | 600 | 700 | 800 | 900 | 1000 |
| 0£ŗ1 | 1.0% | 6.3% | 24.4% | 59.6% | 87.0% |
| 1£ŗ1 | 2.7% | 12.9% | 41.6% | 78.0% | 94.5% |
| 1£ŗ2 | 3.7% | 17.2% | 50.9% | 85.3% | 97.1% |
| 1£ŗ3 | 4.0% | 20.5% | 57.7% | 89.5% | 98.2% |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓŠĻąĶ¬µÄÖŠ×ÓŹżŗĶÖŹ×ÓŹż | B£® | »„ĪŖĶ¬Ī»ĖŲ | ||
| C£® | ĪļĄķŠŌÖŹĻąĶ¬ | D£® | ŗĖĶāµē×ÓŹż²»Ķ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ÓƶčŠŌµē¼«µē½ā1L1mol•L-1µÄCuSO4ČÜŅŗ£¬µ±Ņõ¼«Īö³ö3.2gĶŹ±£¬¼ÓČė0.05molCu£ØOH£©2¹ĢĢåæɽ«ČÜŅŗ»Öø“ÖĮŌÅØ¶Č | |
| B£® | Hg£Øl£©+H2SO4£Øaq£©ØTHgSO4£Øaq£©+H2£Øg£©³£ĪĀĻĀ²»ÄÜ×Ō·¢½ųŠŠ£¬ĖµĆ÷”÷H£¾0 | |
| C£® | ŅŃÖŖ25”ꏱ£¬Ksp£ØAgCl£©=1.8”Į10-10”¢Ksp£ØAg2CrO4£©=2.0”Į10-12£¬ĖłŅŌAgClµÄČܽā¶Č“óÓŚAg2CrO4µÄČܽā¶Č | |
| D£® | 25”ꏱ£¬Ļņ0.1 mol•L-1 CH3COOHČÜŅŗÖŠ¼ÓČėÉŁĮæCH3COONa¹ĢĢ壬øĆČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č½«Ōö“ó£¬ĒŅKw²»±ä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ³£ĪĀĻĀ£¬Ļņ25mL 0.1mol•L-1 MOH ČÜŅŗÖŠÖšµĪ¼ÓČė0.2mol•L-1 HAČÜŅŗ£¬ĒśĻßČēĶ¼ĖłŹ¾£ØĢå»ż±ä»ÆŗöĀŌ²»¼Ę£©£®»Ų“šĻĀĮŠĪŹĢā£ŗ
³£ĪĀĻĀ£¬Ļņ25mL 0.1mol•L-1 MOH ČÜŅŗÖŠÖšµĪ¼ÓČė0.2mol•L-1 HAČÜŅŗ£¬ĒśĻßČēĶ¼ĖłŹ¾£ØĢå»ż±ä»ÆŗöĀŌ²»¼Ę£©£®»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
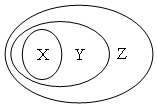 ÓĆĻĀĶ¼±ķŹ¾µÄŅ»Š©ĪļÖŹ»ņøÅÄī¼äµÄ“ÓŹō¹ŲĻµÖŠ²»ÕżČ·µÄŹĒ£Ø””””£©
ÓĆĻĀĶ¼±ķŹ¾µÄŅ»Š©ĪļÖŹ»ņøÅÄī¼äµÄ“ÓŹō¹ŲĻµÖŠ²»ÕżČ·µÄŹĒ£Ø””””£©| X | Y | Z | |
| A | Ńõ»ÆĪļ | »ÆŗĻĪļ | “æ¾»Īļ |
| B | ĀČ»ÆÄĘ | µē½āÖŹ | »ÆŗĻĪļ |
| C | ½šŹōŃõ»ÆĪļ | ¼īŠŌŃõ»ÆĪļ | Ńõ»ÆĪļ |
| D | Å£ÄĢ | ½ŗĢå | ·ÖÉ¢Ļµ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com