
下列实验式中,没有相对分子质量就可以确定分子式的是
①CH3 ②CH ③CH2 ④C2H5 ⑤CH2Cl2
A.①② B.③④⑤ C.①④⑤ D.①③④
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
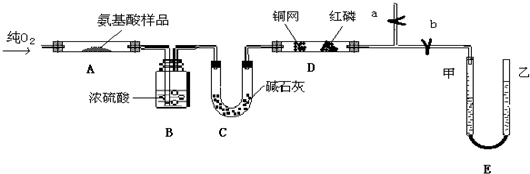
 (2010?桂林二模)某课外实验小组设计了如图所示装置进行“一器多用”的实验探究(夹持装置已略去).
(2010?桂林二模)某课外实验小组设计了如图所示装置进行“一器多用”的实验探究(夹持装置已略去).查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示:请回答下列问题:
短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示:请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
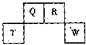 (2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
(2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江西省高三上学期第三次月考化学试卷(普) 题型:填空题
(12分)短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示:
|
|
B |
C |
D |
|
|
A |
|
E |
请回答下列问题:
⑴B、C、D元素的原子半径的大小顺序为:________>________>________(填元素符号)。
⑵E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为______________________________________________。
⑶C有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L甲气体与0.5 L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是________。
⑷在298K下,A、B的单质各1mol完全燃烧,分别放出热量a kJ和b kJ。又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来,若此置换反应生成3mol B的单质,则该反应在298K下的ΔH= (注:题中所设单质均为最稳定单质)
⑸要证明与D同主族相邻元素F的非金属性与E的非金属性的强弱,正确、合理的实验操作及现象是 。
⑹用A、B的单质作电极,C的最高价氧化物的水化物稀溶液作电解质溶液构成原电池,写出此原电池正极的电极反应式 。(假设C只被还原至+2价)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com