
| A. | H2SO4滴入NaAlO2溶液中 | B. | Ba(OH)2溶液滴入Al2(SO4)3溶液中 | ||
| C. | Al2(SO4)3溶液滴入NaOH溶液中 | D. | 氨水滴入Al2(SO4)3溶液中 |
分析 A、偏铝酸钠溶液中滴入硫酸,先生成氢氧化铝沉淀,继续滴加氢氧化铝溶解;
B、硫酸铝溶液中滴入氢氧化钡溶液过程中一定有硫酸沉淀生成;
C、氢氧化钠溶液中滴入Al2(SO4)3溶液,开始无沉淀生成,继续滴加生成沉淀;
D、Al2(SO4)3溶液中滴入氨水溶液,过程中有沉淀生成,氢氧化铝不溶于过量氨水.
解答 解:A、偏铝酸钠溶液中滴入硫酸,先生成氢氧化铝沉淀,继续滴加氢氧化铝溶解,反应的离子方程式为AlO2-+H++H2O=Al(OH)3↓;Al(OH)3+3H+=Al3++3H2O,故A符合;
B、硫酸铝溶液中滴入氢氧化钡溶液过程中一定有硫酸沉淀生成,会出现沉淀减少但不会出现沉淀全部溶解消失的现象,故B不符合;
C、氢氧化钠溶液中滴入Al2(SO4)3溶液,开始无沉淀生成,继续滴加生成沉淀氢氧化铝,反应的离子方程式为,Al3++4OH-=AlO2-+H2O,3AlO2-+Al3++6H2O=4Al(OH)3↓,故C不符合;
D、Al2(SO4)3溶液中滴入氨水溶液,过程中有沉淀生成,氢氧化铝不溶于过量氨水,反应的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;故D不符合;
故选A.
点评 本题考查了物质性质的分析应用,物质反应滴加顺序不同产物可能不同,反应现象不同,掌握物质性质和基础是关键,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 10mL 1mol/L FeCl3溶液 | B. | 50mL 0.3mol/L NaCl溶液 | ||
| C. | 10mL 0.2mol/L CaCl2溶液 | D. | 200mL 0.1mol/L NH4Cl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若电键K与N连接,铁被保护不会腐蚀 | |
| B. | 若电键K与N连接,正极反应式是4OH--4e-═2H2O+O2↑ | |
| C. | 若电键K与M连接,将石墨棒换成铜棒,可实现铁棒上镀铜 | |
| D. | 若电键K与M连接,当两极共产生22.4L(标准状况)气体时,生成了1mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气可使湿的红布条褪色,所以氯气具有漂白性 | |
| B. | 氯气没有漂白性,但通入品红溶液中,品红褪色 | |
| C. | 氯气不跟非金属反应 | |
| D. | 氯气有毒,闻其气味时要小心将集气瓶放在鼻孔下直接闻其气味 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .第一电离能最小的元素是Cu(填元素符号).
.第一电离能最小的元素是Cu(填元素符号).
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题:
常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
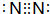 .试写出由上述元素组成的分子中含有4个原子核且为18电子结构的物质的化学式H2O2.
.试写出由上述元素组成的分子中含有4个原子核且为18电子结构的物质的化学式H2O2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com