
甲、乙两同学进行化学研究性学习:测定某次雨水的pH并判断某次雨水是否酸雨。
甲同学取pH试纸用蒸馏水湿润后置于表面皿中,取雨水少量并滴几滴雨水到pH试纸上,稍许,与标准比色卡对照,测得pH为6。由此,甲同学得出这次雨水不是酸雨的结论。
乙同学用烧杯取雨水少许,露置于教室中一段时间后,再用pH试纸正确测定该雨水的pH,测得pH为5。由此,乙同学得出这次雨水是酸雨的结论。
请回答下列问题:
⑴甲、乙两同学上述化学研究性学习思路的可取之处是 。
⑵请你对甲同学的结论进行评价并说明你的理由 。
⑶请你对乙同学的结论进行评价并说明你的理由 。
⑷如果请你测定某次雨水的pH,你的操作方法是 。
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:阅读理解
 (2011?绵阳模拟)某化学兴趣小组为探究
(2011?绵阳模拟)某化学兴趣小组为探究
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖南省长沙市高三第四次月考化学试卷(解析版) 题型:实验题
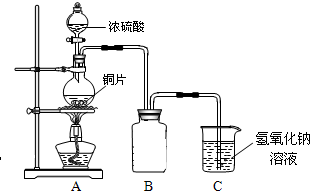
某化学课外兴趣小组探究铜与浓硫酸的反应情况及某些产物的性质。
(Ⅰ)甲、乙两同学进行了下列实验:取一定量的铜片和20 mL 18 mol/L的浓硫酸放在圆底烧瓶中共热,直至反应完毕,最后发现烧瓶中还有铜片剩余,同时根据所学的知识认为还有较多硫酸剩余。
(1)铜与浓硫酸反应的化学方程式是:
可以证明有余酸的实验方案是_ (填字母)。
a.再加入适量NaNO3固体B.再滴入BaCl2溶液 C.再加入银 D.再滴入Na2CO3溶液
(2)甲同学设计求余酸浓度的实验方案是测定产生气体的量。下列方案中不可行的是 (填字母)。
a.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,反应结束后再次称量
b.将产生的气体缓缓通入酸性高锰酸钾溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀
c.用排水法测定其产生气体的体积(折算成标准状况)
d.用排饱和NaHSO3溶液的方法测出其产生气体的体积(折算成标准状况)
(3)乙同学设计测定余酸浓度的实验方案是:测定反应后的混合液中Cu2+的量。在反应后的溶液中加入足量Na2S溶液,充分反应后,过滤、洗涤、干燥、称量沉淀的质量为W g,测得反应后溶液的体积为V mL。则剩余硫酸的物质的量浓度为 mol/L(用含W、V的代数式表示)。
(Ⅱ)丙同学探究SO2与BaCl2溶液能否反应生成白色BaSO3沉淀。
丙同学先将产生的气体通过盛有饱和NaHSO3溶液的洗气瓶,再缓缓通入BaCl2溶液中,观察到有少量白色沉淀生成,检验白色沉淀,发现沉淀全部不溶于稀盐酸,该沉淀的生成表明SO2具有 性。用一个离子方程式解释生成此沉淀的原因 。
查看答案和解析>>
科目:高中化学 来源:0119 月考题 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)甲、乙两同学进行化学研究性学习:测定某次雨水的pH并判断某次雨水是否酸雨。
甲同学取pH试纸用蒸馏水湿润后置于表面皿中,取雨水少量并滴几滴雨水到pH试纸上,
稍许,与标准比色卡对照,测得pH为6。由此,甲同学得出这次雨水不是酸雨的结论。
乙同学用烧杯取雨水少许,露置于教室中一段时间后,再用pH试纸正确测定该雨水的pH,测得pH为5。由此,乙同学得出这次雨水是酸雨的结论。
请回答下列问题:
⑴甲、乙两同学上述化学研究性学习思路的可取之处是 ▲ 。
⑵请你对甲同学的结论进行评价并说明你的理由 ▲ 。
⑶请你对乙同学的结论进行评价并说明你的理由 ▲ 。
⑷如果请你测定某次雨水的pH,你的操作方法是 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com