
���� ��1��Ԫ�ش������ֻ̬���������ԣ���Ԫ�ش����м��̬�Ⱦ���������Ҳ���л�ԭ�ԣ�������ͼ�ֻ̬���л�ԭ�ԣ�
��2��ά����C��ʹʳ���е�Fe3+ת��ΪFe2+���ڴ˹���������������������˵��ά����C���л�ԭ�ԣ�
��3������������θ���������ת���������Σ�
��4��FeSO4�ױ����������ʣ�����������Fe3+��
��� �⣺��1��A��Feֻ�л�ԭ�ԣ� B��Fe2+�Ⱦ���������Ҳ���л�ԭ�ԣ�C��Fe3+ֻ�������ԣ���ѡB��
��2��ά����C��ʹʳ���е�Fe3+ת��ΪFe2+���ڴ˹���������������������˵��ά����C���л�ԭ�ԣ��ʴ�Ϊ��Fe3+����ԭ��
��3������������θ���������ת���������Σ����ӷ���ʽΪFe+2H+=Fe2++H2�����ʴ�Ϊ��Fe+2H+=Fe2++H2����
��4��FeSO4�ױ����������ʣ����¿�����FeSO4���������е������������ʴ�Ϊ����ֹFe2+��������
���� ���⿼����Ԫ�ض����彡������Ҫ�����Լ�������ԭ��Ӧ�������ڻ�ѧ����������Ŀ��飬ע���Ԫ�ػ��ϼ۵ĽǶ�������ظ�������ʵ����ʣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mol C2H6O�����к���C-H����Ϊ0.5NA | |
| B�� | ��״���£�11.2 L CH3CH2OH�к��еķ�����ĿΪ0.5NA | |
| C�� | 3.0 g��ȩ��HCHO��������Ļ�����к��е�ԭ������Ϊ0.4NA | |
| D�� | ���³�ѹ�£�12 g�������ܽ���ˮ������������������Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CaO+H2O�TCa��OH��2 | B�� | CH4+2O2$\frac{\underline{\;��ȼ\;}}{\;}$2H2O+CO2 | ||
| C�� | CaCO3$\frac{\underline{\;����\;}}{\;}$CaO+CO2�� | D�� | Na2SiO3+2HCl�T2NaCl+H2SiO3�����壩 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡHCl��Һ | B�� | ϡNa2SO4��Һ | C�� | CuCl2��Һ | D�� | AgNO3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
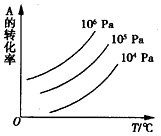 ��һ��ѧƽ��mA��g��+nB��g��?pC��g��+qD��g������ͼ��ʾ��A��ת����ͬѹǿ���¶ȵĹ�ϵ������ͼ3���Եó�����ȷ�����ǣ�������
��һ��ѧƽ��mA��g��+nB��g��?pC��g��+qD��g������ͼ��ʾ��A��ת����ͬѹǿ���¶ȵĹ�ϵ������ͼ3���Եó�����ȷ�����ǣ�������| A�� | ����Ӧ���ȣ�m+n��p+q | B�� | ����Ӧ���ȣ�m+n��p+q | ||
| C�� | ����Ӧ���ȣ�m+n��p+q | D�� | ����Ӧ���ȣ�m+n��p+q |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

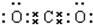

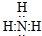 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com